Clear Sky Science · it
Coiled-coils ricchi di istidina favoriscono l’autoassemblaggio dipendente dallo zinco e l’indurimento di colle porose delle mitili
Come le mitili producono una supercolla sott’acqua
Le mitili si aggrappano alle rocce flagellate dalle onde con una colla naturale che gli scienziati cercano di imitare da decenni. Questo studio rivela che un ingrediente a lungo trascurato—piuttosto che la solita star chimica—svolge silenziosamente gran parte del lavoro pesante. Scoprendo come una proteina speciale e lo zinco aiutino le mitili a costruire una colla robusta e spugnosa, la ricerca apre nuove vie per adesivi più delicati e duraturi per la medicina, l’ingegneria e le superfici bagnate di uso quotidiano.
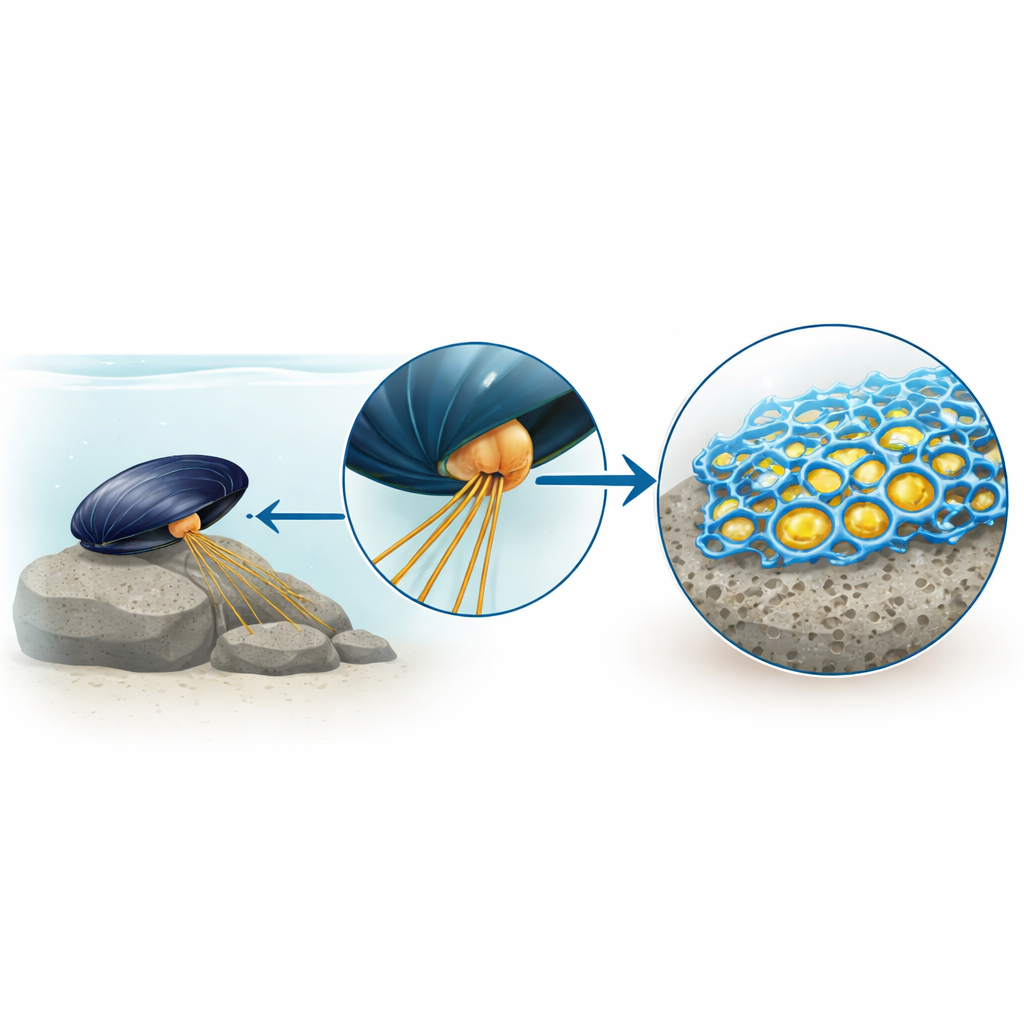
Da un mistero appiccicoso a un nuovo protagonista delle colle
Per anni la storia della colla delle mitili si è concentrata su un blocco costitutivo modificato chiamato DOPA, che aderisce fortemente a superfici e metalli. I materiali sintetici ispirati alla DOPA sono impressionanti, ma non raggiungono ancora la colla naturale delle mitili. Gli autori hanno sospettato che altre proteine non studiate nelle ghiandole produttrici di colla della mitile potessero essere pezzi mancanti del puzzle. Isolando minuscole sacche piene di colla dal piede della mitile e osservandole rompersi e solidificarsi, hanno scoperto che un sottogruppo di proteine formava un’impalcatura solida con una struttura porosa simile a una schiuma, mentre le note proteine ricche di DOPA rimanevano per lo più come un fluido all’interno dei pori.
Scoperta di una proteina strutturale nascosta
Quando il team ha disciolto solo la parte solida di questa colla in miniatura e ne ha analizzato il contenuto, è emersa una singola proteina dominante. L’hanno chiamata mefp-12 e hanno scoperto che è ricca dell’amminoacido istidina e conservata in diverse specie di mitili, suggerendo che sia importante per la sopravvivenza. L’imaging del tessuto del piede della mitile ha mostrato che le cellule nella ghiandola produttrice di colla sintetizzano questa proteina specificamente per la piastra—il cuscinetto appiattito che ancora la mitile alla roccia. Le previsioni strutturali al computer indicano che mefp-12 ha un lungo segmento centrale che tende a formare fasci filamentosi noti come coiled coils, e diversi domini compatti che somigliano a regioni leganti il metallo dette “dita di zinco”, tutti indizi che gli ioni metallici, in particolare lo zinco, potrebbero essere cruciali per il suo comportamento.
Come zinco e pH trasformano goccioline liquide in schiuma solida
Per verificare questa idea in modo semplice, i ricercatori hanno sintetizzato un frammento di 30 amminoacidi della regione centrale di mefp-12. In acqua salata a condizioni leggermente acide—simili all’ambiente di stoccaggio all’interno del piede della mitile—questo breve pezzo si aggregava in goccioline liquide quando era presente lo zinco, ma non con altri metalli come rame o nichel. L’aumento del pH verso quello dell’acqua di mare ha scatenato una trasformazione evidente: le goccioline si sono fuse, si sono diffuse sulle superfici e poi si sono “indurate” in un solido poroso a cellule aperte rigido che somigliava molto, al microscopio, alla colla naturale delle mitili. Misure spettroscopiche e di risonanza magnetica nucleare hanno mostrato che, durante questa transizione, i frammenti proteici passano da uno stato lasso e disordinato a forme più ordinate a spirale che si impacchettano insieme, mentre i gruppi laterali dell’istidina formano ponti robusti con ioni di zinco. Questi ponti metallici bloccano le strutture avvolte in una rete stabile, ma reversibile.

Una rete resistente e riutilizzabile costruita per le onde
Gli autori propongono una nuova ipotesi su come si forma la colla delle mitili. All’interno del piede, mefp-12 è immagazzinata in goccioline acide contenenti zinco insieme ad altre proteine della colla. Quando la secrezione viene rilasciata nell’acqua di mare a pH più elevato, i gruppi istidinici su mefp-12 iniziano a legare lo zinco, spingendo la proteina a riorganizzarsi in fasci avvolti che si connettono in un’impalcatura porosa. Le proteine adesive ricche di DOPA rimangono come una fase più fluida all’interno dei pori, pronte a bagnare e ri-bagnare le superfici. Successivamente, altri metalli come ferro e vanadio rafforzano i componenti contenenti DOPA, producendo una doppia rete interbloccata. Il quadro istidina–zinco probabilmente agisce come un ammortizzatore sacrificial, ma recuperabile, aiutando la piastra a dissipare l’energia delle onde in arrivo mantenendo l’adesione per lunghi periodi.
Cosa significa per le future colle in ambiente umido
Spostando l’attenzione dalla sola DOPA a una collaborazione tra proteine ricche di istidina e zinco, questo studio riscrive il manuale della colla delle mitili. Mostra che le istruzioni per formare un solido poroso autoassemblante sono codificate direttamente nella sequenza di mefp-12, attivate semplicemente da sale, ioni metallici e da un cambiamento di pH. Questi approfondimenti suggeriscono nuove regole di progetto per adesivi e materiali morbidi creati dall’uomo: usare separazione di fase controllata, ponti metallo–proteina e architetture simili a schiume per creare colle e gel che si induriscano in condizioni umide, assorbano i danni e potenzialmente autoriparino, senza fare affidamento esclusivo su un singolo gruppo chimico altamente reattivo.
Citazione: Rivard, M.D., Poulhazan, A., Renner-Rao, M.J. et al. Histidine-rich coiled-coils promote zinc-dependent self-assembly and curing of porous mussel glues. Nat Commun 17, 2809 (2026). https://doi.org/10.1038/s41467-026-69504-y
Parole chiave: adesione delle mitili, colla bioispirata, autoassemblaggio proteico, materiali coordinati ai metalli, adesivi in ambiente umido