Clear Sky Science · es
Los coiled-coils ricos en histidina favorecen la autoensamblaje dependiente del zinc y el curado de adhesivos porosos de mejillón
Cómo los mejillones fabrican una supercola bajo el agua
Los mejillones se aferran a rocas azotadas por las olas con un pegamento natural que los científicos han intentado imitar durante décadas. Este estudio revela que un ingrediente largamente pasado por alto —más que la habitual estrella química— hace silenciosamente gran parte del trabajo duro. Al desvelar cómo una proteína especial y el metal zinc ayudan a los mejillones a construir un adhesivo fuerte y con estructura esponjosa, la investigación abre nuevas vías hacia adhesivos más suaves y duraderos para la medicina, la ingeniería y las superficies húmedas cotidianas.
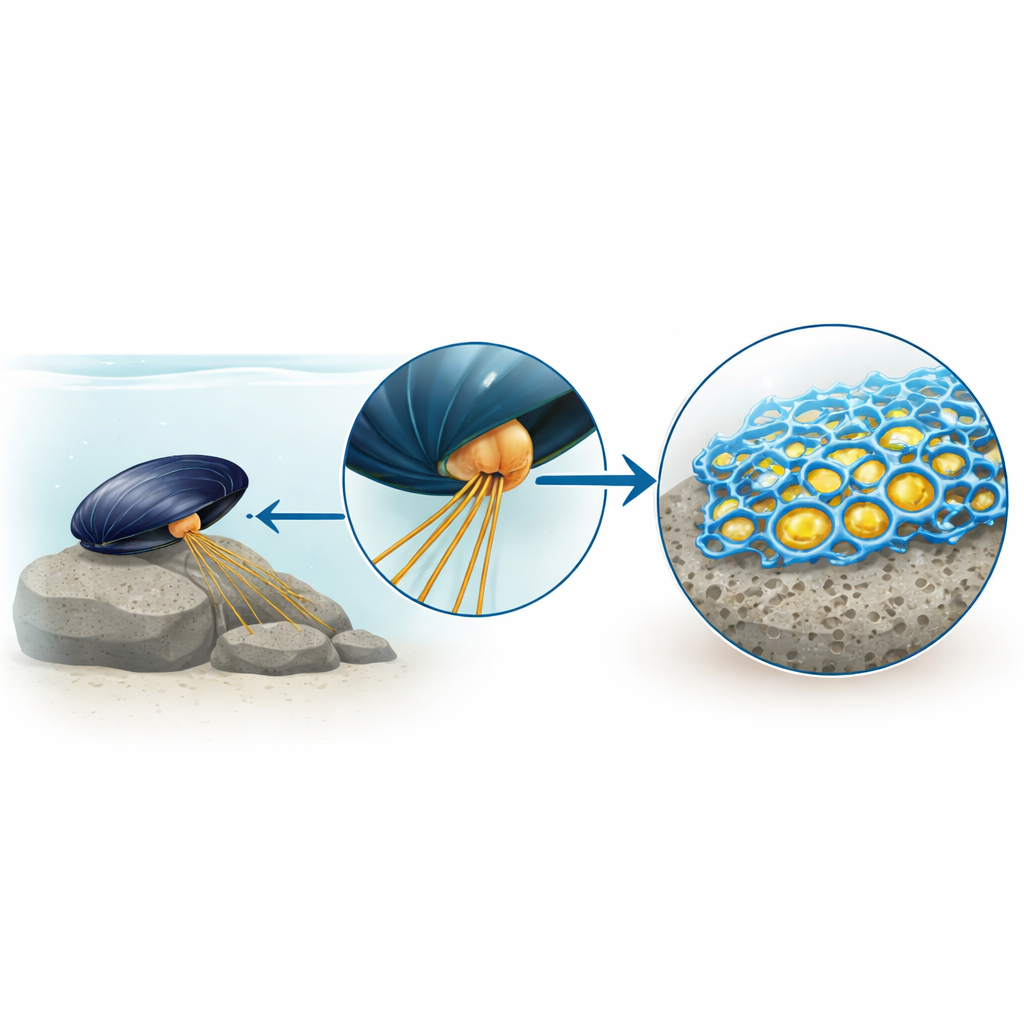
Del misterio pegajoso a un nuevo héroe del pegamento
Durante años, la historia del pegamento de mejillón se centró en un bloque de construcción modificado llamado DOPA, que se adhiere con fuerza a superficies y metales. Los materiales sintéticos inspirados en DOPA han sido impresionantes, pero aun así no alcanzan al pegamento real del mejillón. Los autores sospecharon que otras proteínas no estudiadas dentro de las glándulas productoras de pegamento del mejillón podrían ser piezas que faltaban en el rompecabezas. Al aislar pequeños sacos llenos de pegamento del pie del mejillón y observar cómo reventaban y se solidificaban, encontraron que un subconjunto de proteínas formaba un andamiaje sólido con una estructura porosa tipo espuma, mientras que las conocidas proteínas ricas en DOPA permanecían en su mayoría como un fluido dentro de los poros.
Descubrimiento de una proteína estructural oculta
Cuando el equipo disolvió solo la parte sólida de este pegamento en miniatura y analizó su contenido, destacó una proteína dominante. La llamaron mefp-12 y descubrieron que es rica en el aminoácido histidina y está conservada en varias especies de mejillón, lo que sugiere que es importante para la supervivencia. La imagen del tejido del pie del mejillón mostró que las células de la glándula productora de pegamento sintetizan esta proteína específicamente para la placa —la almohadilla aplanada que ancla el mejillón a la roca. Predicciones estructurales por ordenador indicaron que mefp-12 tiene un segmento central largo que prefiere formar haces enroscados conocidos como coiled coils, y varios dominios compactos que recuerdan regiones que se unen al metal tipo «dedo de zinc», todo lo cual sugiere que los iones metálicos, especialmente el zinc, podrían ser cruciales para su comportamiento.
Cómo el zinc y el pH transforman gotas líquidas en espuma sólida
Para probar esta idea de forma simple, los investigadores fabricaron un fragmento de 30 aminoácidos de la región central de mefp-12. En agua salada y en condiciones ligeramente ácidas —similares al ambiente de almacenamiento dentro del pie del mejillón— este pequeño fragmento se agrupó en gotas líquidas cuando había zinc presente, pero no con otros metales como cobre o níquel. Elevar el pH hacia el del agua de mar desencadenó una transformación notable: las gotas se fusionaron, se extendieron sobre las superficies y luego «curaron» hasta convertirse en un sólido rígido y poroso de celdas abiertas que se parecía mucho al pegamento natural del mejillón observado al microscopio. Mediciones espectroscópicas y de resonancia magnética nuclear mostraron que, durante esta transición, los fragmentos proteicos pasan de un estado suelto y desordenado a formas helicoidales más ordenadas que se empaquetan entre sí, mientras que los grupos laterales de histidina forman puentes firmes con iones de zinc. Estos puentes metálicos bloquean las estructuras enrolladas en una red estable, pero reversible.

Una red resistente y reutilizable diseñada para las olas
Los autores proponen una nueva imagen de cómo se forma el pegamento de mejillón. Dentro del pie, mefp-12 se almacena en gotas ácidas que contienen zinc junto con otras proteínas adhesivas. Al secretarse hacia el agua de mar de pH más alto, los grupos de histidina en mefp-12 comienzan a unirse al zinc, impulsando la reorganización de la proteína en haces enroscados que se conectan en un armazón poroso. Las proteínas adhesivas ricas en DOPA permanecen como una fase más fluida dentro de los poros, listas para humedecer y rehumedecer las superficies. Más tarde, otros metales como el hierro y el vanadio refuerzan los componentes que contienen DOPA, produciendo una red doble interbloqueada. El armazón histidina–zinc probablemente actúa como un absorbedor de impactos sacrificable, pero recuperable, ayudando a la placa a disipar la energía de las olas rompiendo mientras mantiene la adhesión durante largos periodos.
Qué implica esto para los pegamentos húmedos del futuro
Al desplazar la atención de la DOPA en solitario hacia una asociación entre proteínas ricas en histidina y zinc, este estudio reescribe el manual del pegamento de mejillón. Muestra que las instrucciones para formar un sólido poroso y autoensamblable están codificadas directamente en la secuencia de mefp-12, activadas simplemente por sal, iones metálicos y un cambio de pH. Estas ideas sugieren nuevas reglas de diseño para adhesivos y materiales blandos artificiales: usar separación de fases controlada, puentes metal–proteína y arquitecturas tipo espuma para crear colas y geles que curen en condiciones húmedas, absorban daño y potencialmente se autorreparen, sin depender únicamente de un único grupo químico altamente reactivo.
Cita: Rivard, M.D., Poulhazan, A., Renner-Rao, M.J. et al. Histidine-rich coiled-coils promote zinc-dependent self-assembly and curing of porous mussel glues. Nat Commun 17, 2809 (2026). https://doi.org/10.1038/s41467-026-69504-y
Palabras clave: adhesión de mejillón, pegamento bioinspirado, autoensamblaje de proteínas, materiales coordinados con metales, adhesivos en ambientes húmedos