Clear Sky Science · de
Histidinreic helical Bündel fördern zinkabhängige Selbstassemblierung und Aushärtung poröser Muschelklebstoffe
Wie Muscheln Unterwasser Superkleber herstellen
Muscheln haften an wellenzerklüfteten Felsen mit einem natürlichen Klebstoff, den Wissenschaftler seit Jahrzehnten zu imitieren versuchen. Diese Studie zeigt, dass eine lange übersehene Zutat – und nicht die üblichen chemischen Stars – stillschweigend einen Großteil der schweren Arbeit übernimmt. Indem sie aufdeckten, wie ein spezielles Protein und das Metall Zink den Muscheln helfen, einen starken, schwammähnlichen Klebstoff zu bauen, eröffnet die Forschung neue Wege zu schonenderen, langlebigeren Haftmitteln für Medizin, Technik und alltägliche nasse Oberflächen.
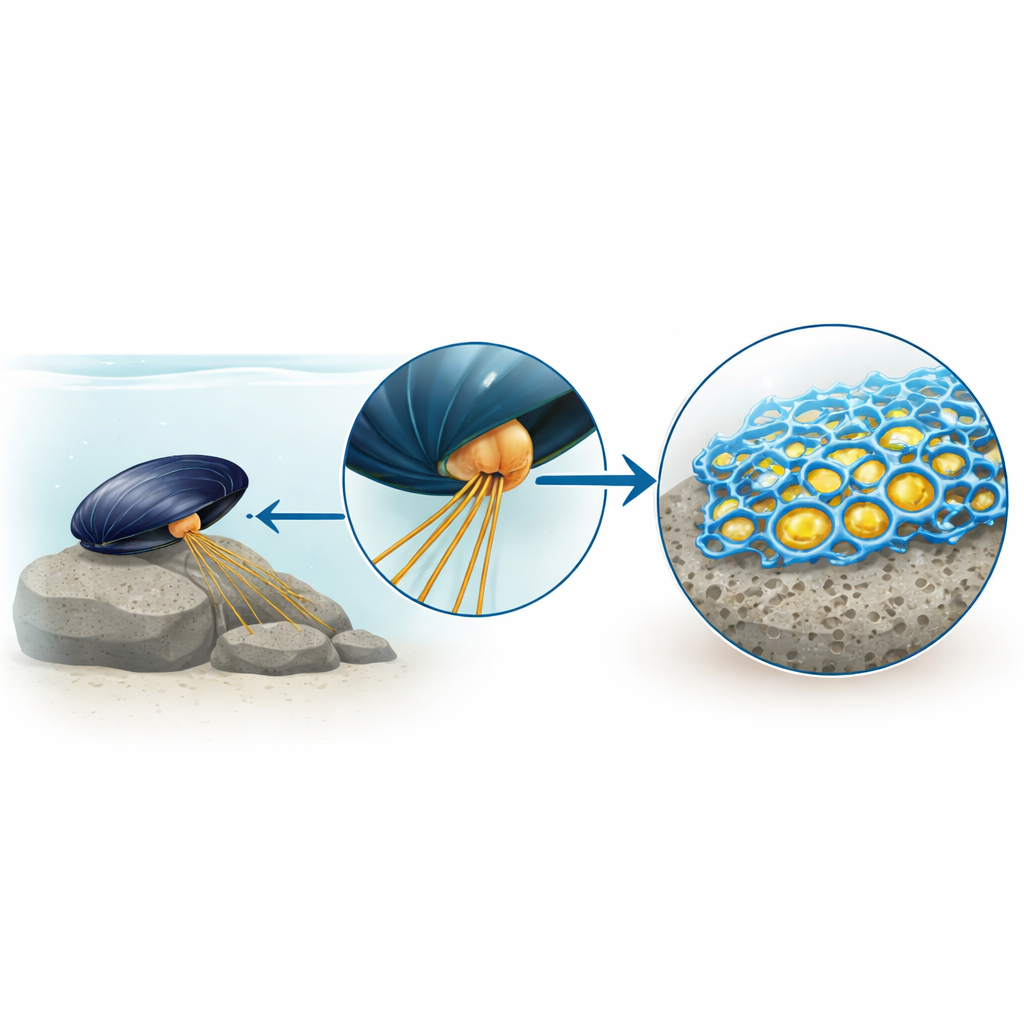
Vom klebrigen Rätsel zum neuen Klebstoffhelden
Jahrelang drehte sich die Geschichte des Muschelklebers um einen modifizierten Baustein namens DOPA, der stark an Oberflächen und Metalle bindet. Synthetische Materialien, die von DOPA inspiriert sind, waren eindrucksvoll, erreichen aber noch nicht die Leistungsfähigkeit des natürlichen Muschelklebers. Die Autoren vermuteten, dass andere, bisher nicht untersuchte Proteine in den kleberbildenden Drüsen der Muschel fehlende Puzzleteile sein könnten. Indem sie winzige, klebergefüllte Bläschen aus dem Fuß der Muschel isolierten und beobachteten, wie diese platzten und erstarrten, fanden sie, dass eine Untergruppe von Proteinen ein festes Gerüst mit poröser, schaumartiger Struktur bildete, während die bekannten DOPA‑reichen Proteine größtenteils als Flüssigkeit in den Poren verblieben.
Entdeckung eines verborgenen Strukturproteins
Als das Team nur den festen Teil dieses Miniaturklebers löste und dessen Inhalt analysierte, trat ein einzelnes dominantes Protein hervor. Sie nannten es mefp‑12 und entdeckten, dass es reich an der Aminosäure Histidin ist und über mehrere Muschelarten hinweg konserviert vorkommt, was auf seine Überlebensbedeutung hindeutet. Bildgebende Untersuchungen des Muschelfußgewebes zeigten, dass Zellen in der kleberproduzierenden Drüse dieses Protein gezielt für die Plaque herstellen – die abgeflachte Platte, mit der die Muschel am Felsen verankert ist. Computergestützte Strukturvorhersagen deuteten darauf hin, dass mefp‑12 ein langes zentrales Segment besitzt, das dazu neigt, seilartige Bündel zu bilden, bekannt als coiled coils, sowie mehrere kompakte Domänen, die metallbindenden „Zinkfingern“ ähneln, was alles darauf hindeutet, dass Metallionen, besonders Zink, für sein Verhalten entscheidend sein könnten.
Wie Zink und pH flüssige Tröpfchen in festen Schaum verwandeln
Um diese Idee einfach zu testen, stellten die Forscher ein 30‑Aminosäuren‑Fragment des zentralen Bereichs von mefp‑12 her. In salzhaltigem Wasser unter leicht sauren Bedingungen – ähnlich der Speicherumgebung im Muschelfuß – sammelte sich dieses kurze Stück zu flüssigen Tröpfchen, wenn Zink vorhanden war, jedoch nicht bei anderen Metallen wie Kupfer oder Nickel. Eine Erhöhung des pH‑Werts in Richtung Meerwasser löste eine auffällige Umwandlung aus: Die Tröpfchen verschmolzen, verteilten sich auf Oberflächen und „härteten“ dann zu einem starren, offenporigen Feststoff aus, der unter dem Mikroskop dem natürlichen Muschelkleber sehr ähnelte. Spektroskopische Messungen und Kernspinresonanz zeigten, dass sich die Proteinsegmente während dieses Übergangs von einem lockeren, ungeordneten Zustand in geordnetere spiralige Formen umwandeln, die dicht zusammenpacken, während Histidin‑Seitenketten stabile Brücken zu Zinkionen bilden. Diese Metallbrücken verriegeln die schraubenförmigen Strukturen zu einem stabilen, aber reversiblen Netzwerk.

Ein robustes, wiederverwendbares Netzwerk für die Brandung
Die Autoren schlagen ein neues Bild dafür vor, wie Muschelkleber entsteht. Im Fuß wird mefp‑12 in sauren, zinkhaltigen Tröpfchen zusammen mit anderen Kleberproteinen gespeichert. Wenn die Sekretion ins höher pH‑wertige Meerwasser freigesetzt wird, beginnen die Histidingruppen von mefp‑12, Zink zu binden, wodurch das Protein sich in coiled‑Bündel umorganisiert, die sich zu einem porösen Gerüst verbinden. DOPA‑reiche Haftproteine bleiben als flüssigere Phase innerhalb der Poren und können Oberflächen benetzen und erneut benetzen. Später verstärken andere Metalle wie Eisen und Vanadium die DOPA‑haltigen Komponenten und erzeugen ein ineinandergreifendes Doppelnetzwerk. Das Histidin‑Zink‑Gerüst wirkt wahrscheinlich als opferbereiter, aber wiederherstellbarer Stoßdämpfer, der der Plaque hilft, die Energie brechender Wellen zu dissipieren und gleichzeitig die Haftung über lange Zeiträume zu erhalten.
Was das für künftige Nasskleber bedeutet
Indem die Aufmerksamkeit von DOPA allein auf eine Partnerschaft zwischen histidinreichen Proteinen und Zink verschoben wird, schreibt diese Studie das Lehrbuch für Muschelkleber neu. Sie zeigt, dass die Anleitung zur Bildung eines selbstassemblierenden, porösen Festkörpers direkt in der Sequenz von mefp‑12 kodiert ist und einfach durch Salz, Metallionen und eine pH‑Änderung aktiviert wird. Diese Erkenntnisse legen neue Gestaltungsprinzipien für synthetische Klebstoffe und weiche Materialien nahe: kontrollierte Phasentrennung, Metall‑Protein‑Brücken und schaumartige Architekturen zu verwenden, um Kleber und Gele zu schaffen, die in nassen Bedingungen aushärten, Schäden absorbieren und potenziell selbstheilen können, ohne sich ausschließlich auf eine hochreaktive chemische Gruppe zu stützen.
Zitation: Rivard, M.D., Poulhazan, A., Renner-Rao, M.J. et al. Histidine-rich coiled-coils promote zinc-dependent self-assembly and curing of porous mussel glues. Nat Commun 17, 2809 (2026). https://doi.org/10.1038/s41467-026-69504-y
Schlüsselwörter: Muschelhaftung, bioinspirierter Klebstoff, Protein‑Selbstassemblierung, metallkoordinierte Materialien, Nassklebeflächen