Clear Sky Science · fr
Les coiled-coils riches en histidine favorisent l’auto-assemblage dépendant du zinc et le durcissement des colles poreuses des moules
Comment les moules fabriquent une super colle sous l’eau
Les moules s’accrochent aux rochers battus par les vagues grâce à une colle naturelle que les scientifiques tentent d’imiter depuis des décennies. Cette étude révèle qu’un ingrédient longtemps négligé — plutôt que l’acteur chimique habituellement mis en avant — effectue en réalité une grande partie du travail difficile. En montrant comment une protéine particulière et le métal zinc aident les moules à construire une colle solide et poreuse, les chercheurs ouvrent de nouvelles voies vers des adhésifs plus doux et plus durables pour la médecine, l’ingénierie et les surfaces humides du quotidien.
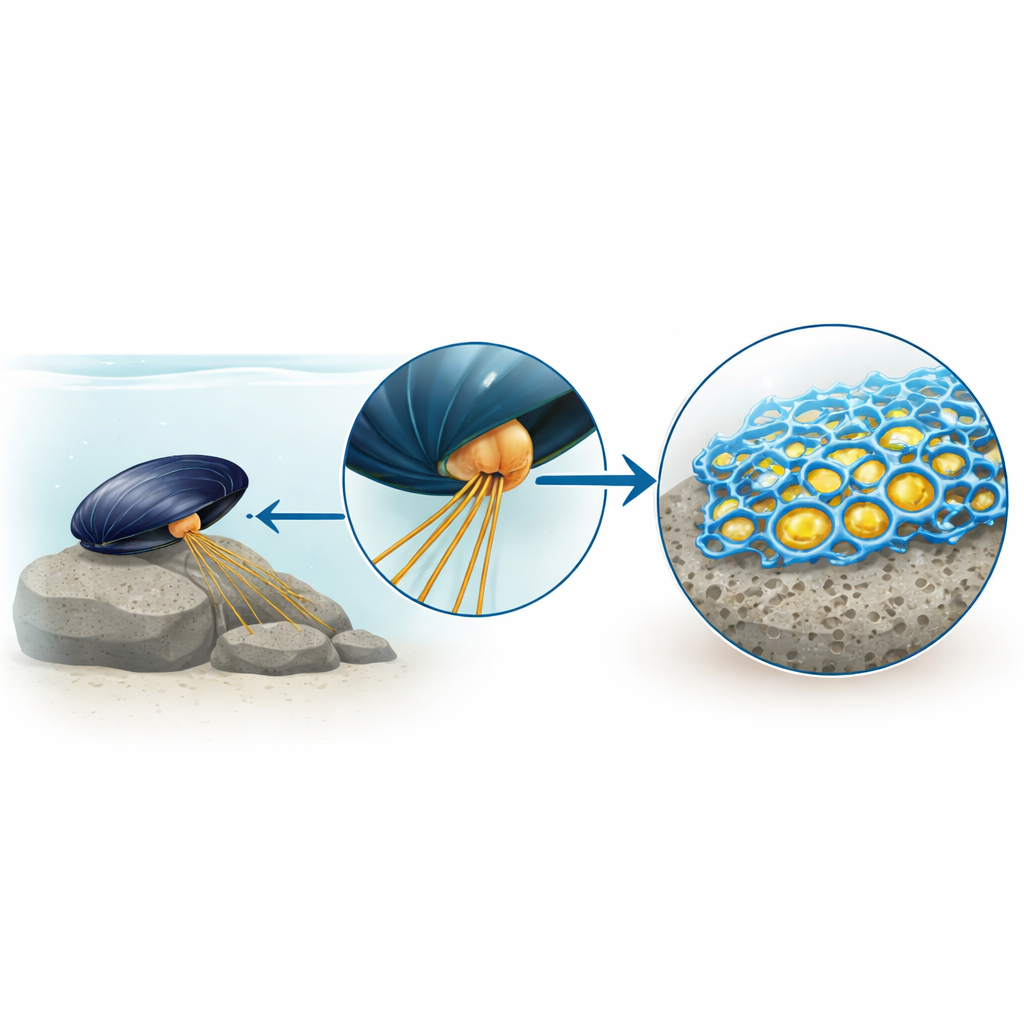
Du mystère collant à un nouveau héros de la colle
Pendant des années, l’histoire de la colle de moule a tourné autour d’un bloc de construction modifié appelé DOPA, qui adhère fortement aux surfaces et aux métaux. Les matériaux synthétiques inspirés de la DOPA ont été impressionnants, mais restent en deçà de la colle naturelle. Les auteurs ont émis l’hypothèse que d’autres protéines peu étudiées, présentes dans les glandes productrices de colle de la moule, pourraient manquer à l’appel. En isolant de minuscules sacs remplis de colle issus du pied de la moule et en observant leur éclatement et leur solidification, ils ont trouvé qu’un sous-ensemble de protéines formait un échafaudage solide à structure poreuse, semblable à une mousse, tandis que les protéines riches en DOPA restaient majoritairement sous forme fluide à l’intérieur des pores.
Découverte d’une protéine structurelle cachée
Quand l’équipe a dissous uniquement la partie solide de cette colle miniature et analysé son contenu, une seule protéine dominante a émergé. Ils l’ont nommée mefp-12 et ont découvert qu’elle est riche en l’acide aminé histidine et conservée chez plusieurs espèces de moules, ce qui suggère une importance pour la survie. L’imagerie des tissus du pied de la moule a montré que des cellules de la glande productrice de colle synthétisent cette protéine spécifiquement pour la plaque — le coussinet aplati qui ancre la moule au rocher. Les prédictions structurelles informatiques indiquent que mefp-12 possède un long segment central prédisposé à former des faisceaux enroulés appelés coiled-coils, et plusieurs domaines compacts rappelant des régions de liaison au métal de type « doigt de zinc », suggérant que des ions métalliques, en particulier le zinc, pourraient être cruciaux pour son comportement.
Comment le zinc et le pH transforment des gouttelettes liquides en mousse solide
Pour tester cette idée de manière simple, les chercheurs ont synthétisé un fragment de 30 acides aminés de la région centrale de mefp-12. Dans de l’eau salée et légèrement acide — conditions proches de l’environnement de stockage à l’intérieur du pied de la moule — ce petit fragment s’assemblait en gouttelettes liquides en présence de zinc, mais pas avec d’autres métaux comme le cuivre ou le nickel. L’augmentation du pH vers celui de l’eau de mer déclenchait une transformation spectaculaire : les gouttelettes fusionnaient, s’étalaient sur les surfaces, puis « durcissaient » en un solide poreux à cellules ouvertes, rigide et très semblable, au microscope, à la colle naturelle de la moule. Des mesures spectroscopiques et de résonance magnétique nucléaire ont montré que, au cours de cette transition, les fragments protéiques passent d’un état lâche et désordonné à des formes spiralées plus ordonnées qui s’assemblent, tandis que les groupements latéraux d’histidine forment des ponts solides avec les ions zinc. Ces ponts métalliques verrouillent les structures enroulées dans un réseau stable mais réversible.

Un réseau résistant et réutilisable conçu pour les vagues
Les auteurs proposent une nouvelle image de la formation de la colle de moule. À l’intérieur du pied, mefp-12 est stockée dans des gouttelettes acides contenant du zinc, aux côtés d’autres protéines de colle. Lorsque la sécrétion est libérée dans l’eau de mer, au pH plus élevé, les groupements histidine de mefp-12 commencent à se lier au zinc, poussant la protéine à se réorganiser en faisceaux enroulés qui se relient en un cadre poreux. Les protéines adhésives riches en DOPA restent dans une phase plus fluide à l’intérieur des pores, prêtes à humecter et ré-humecter les surfaces. Par la suite, d’autres métaux comme le fer et le vanadium renforcent les composants contenant de la DOPA, produisant un réseau double emboîté. Le cadre histidine–zinc joue probablement le rôle d’amortisseur sacrificiel mais récupérable, aidant la plaque à dissiper l’énergie des vagues tout en maintenant l’adhérence sur de longues périodes.
Ce que cela signifie pour les futures colles en milieu humide
En déplaçant l’attention de la seule DOPA vers un partenariat entre protéines riches en histidine et zinc, cette étude réécrit le manuel de la colle de moule. Elle montre que les instructions pour former un solide poreux auto-assemblé sont encodées directement dans la séquence de mefp-12, activées simplement par le sel, les ions métalliques et un changement de pH. Ces connaissances suggèrent de nouvelles règles de conception pour des adhésifs et matériaux mous fabriqués par l’homme : utiliser une séparation de phases contrôlée, des ponts métal–protéine et des architectures semblables à une mousse pour créer des colles et gels qui durcissent en conditions humides, absorbent les dommages et peuvent potentiellement s’auto-réparer, sans dépendre uniquement d’un groupe chimique hautement réactif.
Citation: Rivard, M.D., Poulhazan, A., Renner-Rao, M.J. et al. Histidine-rich coiled-coils promote zinc-dependent self-assembly and curing of porous mussel glues. Nat Commun 17, 2809 (2026). https://doi.org/10.1038/s41467-026-69504-y
Mots-clés: adhésion des moules, colle bioinspirée, auto-assemblage des protéines, matériaux coordonnés par des métaux, adhésifs en milieu humide