Clear Sky Science · sv
Laktatmedierad makrofagpolarisation främjar splenomegali vid akut erytroleukemi
Varför detta är viktigt för patienter och familjer
När blodcancer, som leukemi, sprider sig utanför benmärgen kan mjälten svälla kraftigt, vilket leder till smärta, anemi och livshotande komplikationer. Denna studie ställer en till synes enkel fråga: vad är det egentligen som får mjälten att bli så stor vid en sällsynt men aggressiv leukemi som akut erytroleukemi? Forskarna avslöjar en oväntad syndabock — en vanlig metabol produkt, laktat — och visar att minskad laktatproduktion hos möss kan krympa mjälten och förlänga överlevnaden.
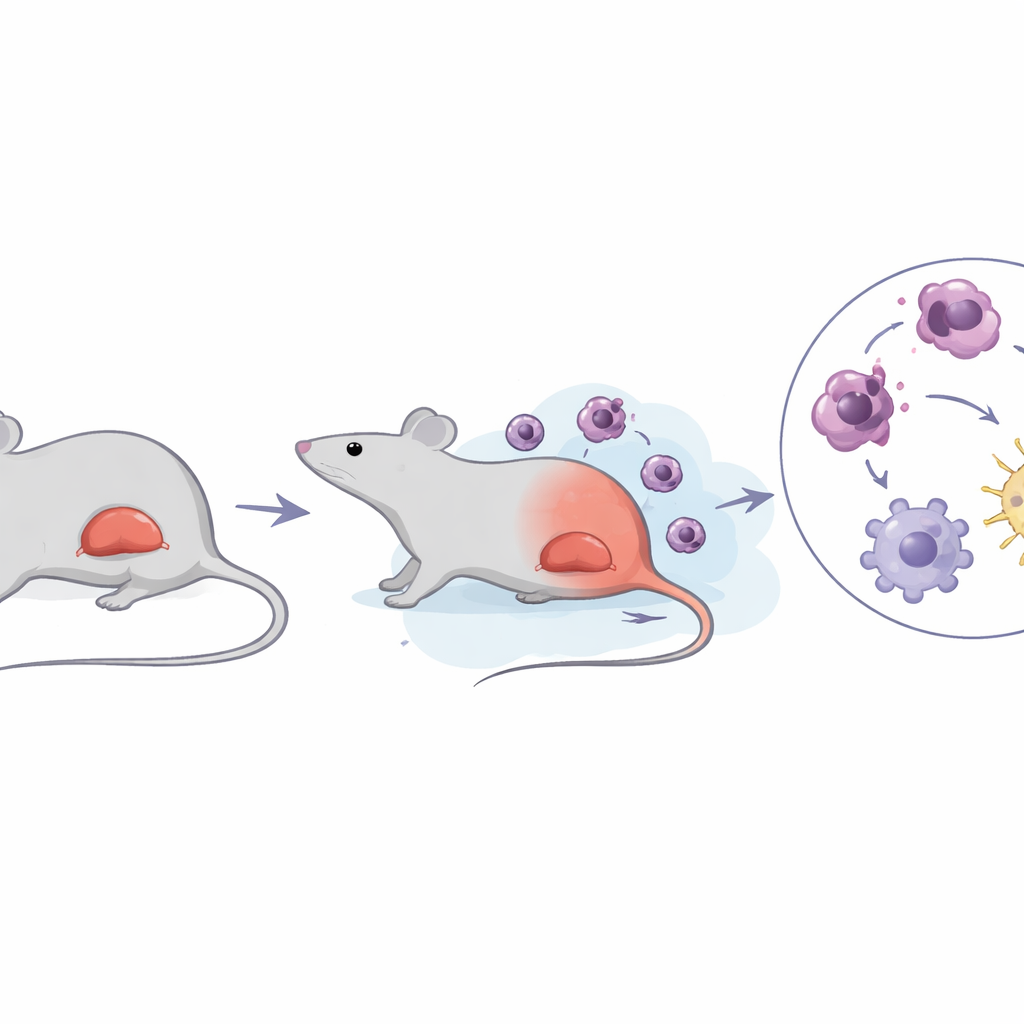
En farlig svullnad av mjälten
Akut erytroleukemi är en ovanlig undergrupp av akut myeloisk leukemi som kännetecknas av explosiv tillväxt av omogna förstadier till röda blodkroppar och en mycket dålig prognos, med genomsnittlig överlevnad mätt i månader. Många patienter utvecklar splenomegali, där mjälten sväller och blir full av leukemiceller. Genom att använda en väl etablerad musmodell infekterad med Friend murint leukemivirus följde författarna noggrant sjukdomsutvecklingen. De bekräftade att mössen utvecklade anemi, mycket höga vita blodkroppssiffror och kraftigt förstorade mjältar, vilket nära speglade människans tillstånd. Viktigt var att de fann att mjältförstoring uppstod först; först senare steg laktatnivåerna — ett nedbrytningsprodukt av sockeromsättning — kraftigt inom mjälten.
När sockerförbränningen hamnar i obalans
Cancer-celler föredrar ofta ett snabbt men ineffektivt sätt att bränna socker, känt som glykolys, vilket producerar laktat även när syre finns. Proteomisk (storskalig protein) analys av sjuka musmjältar visade att nyckelenzymer som styr sockeranvändning och produktion var i obalans. Enzymer som omvandlar pyruvat till laktat var uppreglerade, medan de som återvinner laktat tillbaka till glukos var nedreglerade. Transportörer som pumpar in laktat i celler var också mer aktiva. Tillsammans skapade dessa förändringar en metabolisk fälla: socker flödade in i mjälten, drevs snabbt mot laktat, och det laktatet behölls snarare än rensades bort, vilket ledde till en miljö med hög laktathalt i det förstorade organet.
Immunförsvaret ställs i ett inflammatoriskt läge
Mjälten är inte bara ett filter för blodceller; den är också ett livligt immunologiskt centrum. Teamet upptäckte att höga laktatnivåer förändrade beteendet hos immunceller, särskilt makrofager — mångsidiga celler som antingen kan elda på inflammationen (ofta kallat ett M1-liknande tillstånd) eller hjälpa till att reparera skada och återställa balans (ett M2-liknande tillstånd). I de leukemiska mjältarna minskade det totala antalet makrofager, men de kvarvarande cellerna var starkt förskjutna mot det inflammatoriska M1-liknande tillståndet. Proteiner inne i dessa makrofager visade ökad ”laktylering”, en kemisk märkning härledd från laktat, vilket antyder att överskott av laktat direkt omprogrammerade hur dessa celler fungerade. Samtidigt rubbades balansen hos andra immuncellstyper, med färre T‑celler och fler myeloida celler, vilket signalerar en bredare ombyggnad av mjältens immunologiska landskap.
En självförstärkande loop driven av laktat
För att undersöka orsak och verkan vände sig forskarna till cellkulturer. När de utsatte musmakrofager för det leukemiframkallande viruset ökade cellerna sin sockeranvändning, släppte ut laktat och antog en M1-liknande inflammatorisk profil. Blockering av två signalvägar inne i cellerna, kallade STAT1 och mTOR, förhindrade både ökningen av laktat och skiftet mot det inflammatoriska tillståndet. Slående nog var det tillräckligt att exponera makrofager enbart för laktat för att driva dem in i det M1-liknande tillståndet och få dem att producera ännu mer laktat, vilket skapade en ond cirkel. Vätska från dessa laktat‑konditionerade makrofager fick mänskliga erytroleukemiceller att växa snabbare, vilket visar att de förändrade immuncellerna aktivt hjälpte cancern.
Att bryta cirkeln för att skydda mjälten
Slutligen frågade teamet om avbrott i laktatproduktionen i levande djur kunde påverka sjukdomens förlopp. De behandlade leukemiska möss med oxamat, ett läkemedel som hämmar enzymet som tillverkar laktat. Jämfört med obehandlade djur hade oxamat‑behandlade möss mindre mjältar och andra organ, förbättrade blodvärden, mindre vävnadsskada och längre överlevnad. Deras spleniska makrofager skiftade tillbaka mot en mer balanserande, M2‑liknande profil, och de totala laktatnivåerna i mjälten sjönk. Tillsats av extra laktat gav motsatt effekt och förstärkte mjältförstoring. För en lekmannabetraktare är budskapet tydligt: i denna leukemimodell är laktat inte bara en metabol avfallsprodukt — det är en kraftfull signal som låser immunceller i ett inflammatoriskt, tumörstödjande läge och bidrar till organsvullnad.
Vad detta kan innebära för framtida vård
Detta arbete omformulerar splenomegali vid akut erytroleukemi som en aktiv process som drivs av en återkopplingsslinga mellan cancerens metabolism och immunsystemet. Genom att visa att blockering av laktatproduktion kan reversera skadliga immuna förändringar och minska mjältförstoringen hos möss pekar studien mot en ny klass av »metabol‑immunologiska« behandlingar. Mycket mer forskning behövs för att testa säkerhet, timing och kombinationer med standardleukemiläkemedel, men att rikta in sig på denna laktatdrivna krets kan en dag hjälpa till att skydda patienter från smärtsam, farlig mjältförstoring och bromsa framfarten hos denna aggressiva blodcancer.
Citering: Yang, M., Xie, D., Zhang, Y. et al. Lactate-mediated macrophage polarization promotes splenomegaly in acute erythroleukemia. Cell Death Dis 17, 373 (2026). https://doi.org/10.1038/s41419-026-08612-5
Nyckelord: akut erytroleukemi, laktatmetabolism, makrofagpolarisation, splenomegali, tumörmikromiljö