Clear Sky Science · pt
Polarização de macrófagos mediada por lactato promove esplenomegalia na eritroleucemia aguda
Por que isso importa para pacientes e familiares
Quando cânceres do sangue como a leucemia se espalham além da medula óssea, eles podem causar um aumento dramático do baço, levando a dor, anemia e complicações potencialmente fatais. Este estudo faz uma pergunta aparentemente simples: o que, exatamente, faz o baço crescer tanto em uma leucemia rara e agressiva chamada eritroleucemia aguda? Os pesquisadores identificam um culpado inesperado — um subproduto metabólico comum chamado lactato — e mostram que reduzir a produção de lactato em camundongos pode encolher o baço e prolongar a sobrevivência.
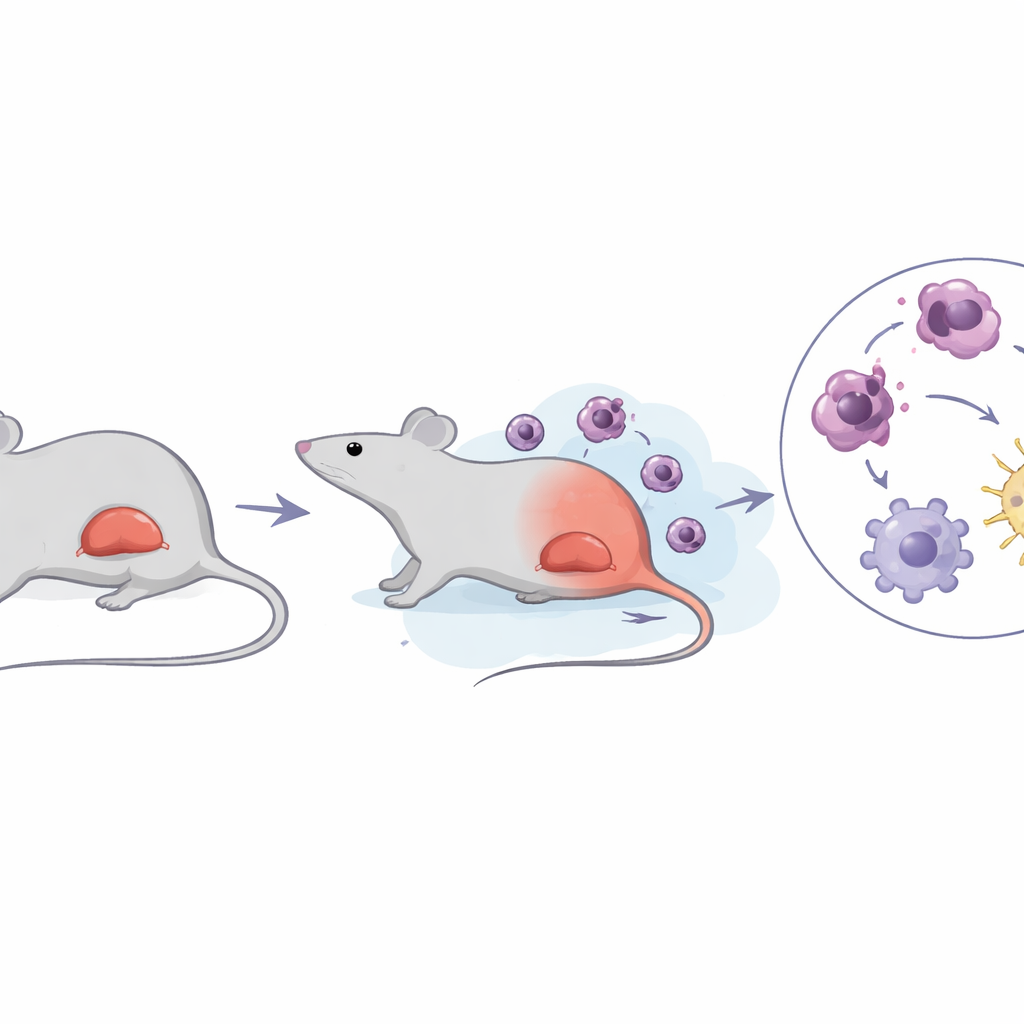
Um inchaço perigoso do baço
A eritroleucemia aguda é um subtipo incomum da leucemia mieloide aguda, caracterizado por crescimento explosivo de precursores imaturos de glóbulos vermelhos e prognóstico muito ruim, com sobrevida média medida em meses. Muitos pacientes desenvolvem esplenomegalia, em que o baço aumenta de tamanho e fica repleto de células leucêmicas. Usando um modelo bem estabelecido de camundongo infectado com o vírus Friend da leucemia murina, os autores acompanharam cuidadosamente a progressão da doença. Eles confirmaram que os camundongos desenvolveram anemia, contagens de glóbulos brancos muito altas e baços severamente aumentados, espelhando de perto a condição humana. Importante, eles observaram que o aumento do baço ocorreu primeiro; somente mais tarde os níveis de lactato — um produto da quebra do açúcar — aumentaram acentuadamente dentro do baço.
Quando a queima de açúcar sai do equilíbrio
As células cancerosas frequentemente preferem uma forma rápida, porém ineficiente, de quebrar o açúcar conhecida como glicólise, que produz lactato mesmo quando há oxigênio disponível. A análise proteômica (em larga escala de proteínas) de baços de camundongos doentes revelou que enzimas-chave que controlam o uso e a produção de açúcar estavam desequilibradas. Enzimas que convertem piruvato em lactato estavam aumentadas, enquanto aquelas que reciclam lactato de volta para glicose estavam diminuídas. Transportadores que captam lactato nas células também estavam mais ativos. Juntas, essas mudanças criaram uma armadilha metabólica: o açúcar fluía para o baço, era rapidamente direcionado para lactato, e esse lactato era retido em vez de ser eliminado, levando a um ambiente interno do órgão altamente rico em lactato.
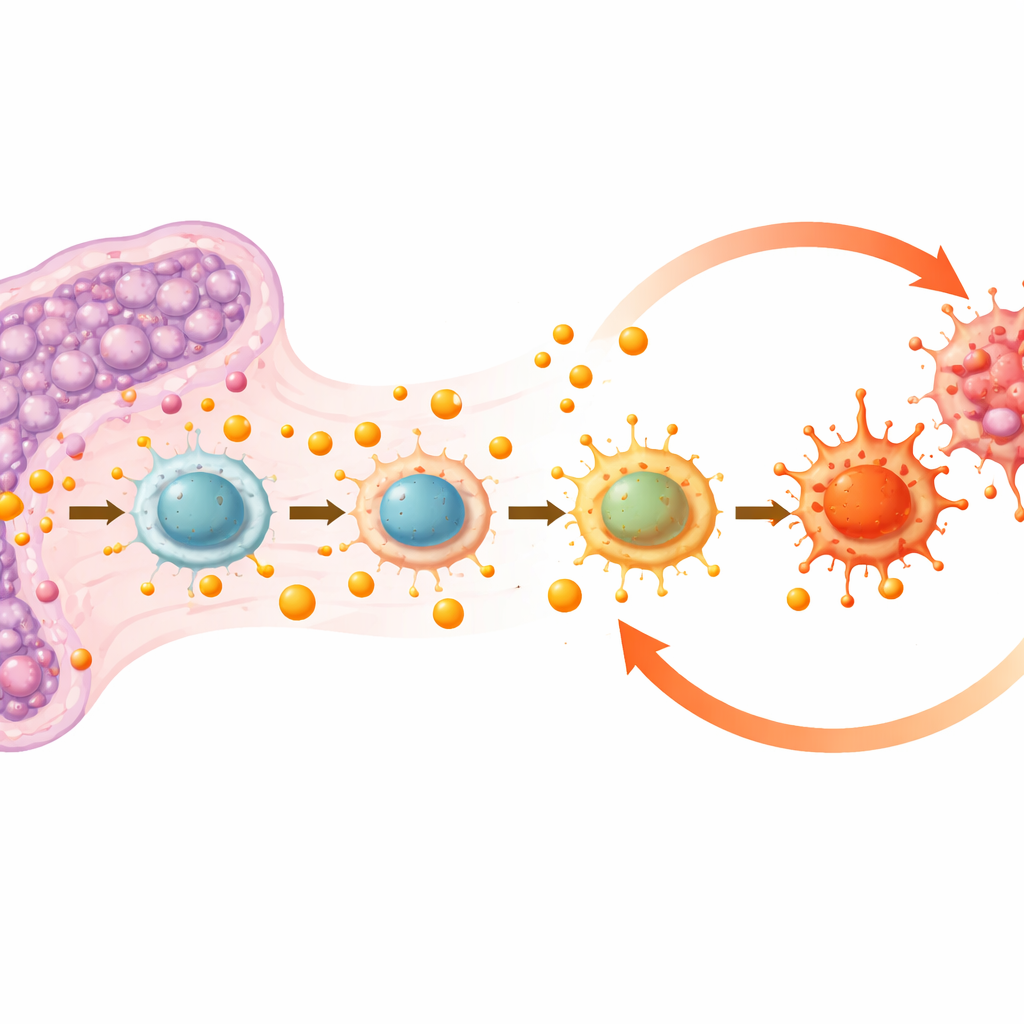
Células imunes empurradas para um estado inflamatório
O baço não é apenas um filtro para células sanguíneas; é também um importante centro imunológico. A equipe descobriu que altos níveis de lactato estavam alterando o comportamento das células imunes, especialmente dos macrófagos — células versáteis que podem tanto inflamar (frequentemente chamado de estado semelhante a M1) quanto ajudar a resolver danos e restaurar o equilíbrio (estado semelhante a M2). Nos baços leucêmicos, o número total de macrófagos caiu, mas as células remanescentes estavam fortemente inclinadas para o estado inflamatório semelhante a M1. Proteínas dentro desses macrófagos mostraram aumento de “lactilação”, uma marca química derivada do lactato, sugerindo que o excesso de lactato estava diretamente reprogramando o funcionamento dessas células. Ao mesmo tempo, outros tipos de células imunes ficaram fora de equilíbrio, com menos células T e mais células mieloides, sinalizando uma remodelação mais ampla do panorama imunológico do baço.
Um ciclo autorreforçador impulsionado pelo lactato
Para investigar causa e efeito, os pesquisadores recorreram a experimentos em cultura celular. Quando expuseram macrófagos de camundongo ao vírus causador da leucemia, as células aumentaram o uso de açúcar, liberaram lactato e adotaram um perfil inflamatório semelhante a M1. Bloquear dois interruptores de sinalização dentro das células, chamados STAT1 e mTOR, impediu tanto o aumento do lactato quanto a mudança para o estado inflamatório. De forma marcante, banhar macrófagos apenas com lactato foi suficiente para empurrá‑los ao estado semelhante a M1 e fazê‑los gerar ainda mais lactato, criando um ciclo vicioso. O fluido retirado desses macrófagos condicionados por lactato fez células humanas de eritroleucemia crescerem mais rápido, mostrando que as células imunes alteradas estavam ativamente ajudando o câncer.
Quebrando o ciclo para proteger o baço
Por fim, a equipe investigou se interromper a produção de lactato em animais vivos poderia alterar o curso da doença. Eles trataram camundongos leucêmicos com oxamato, um fármaco que inibe a enzima que produz lactato. Em comparação com animais não tratados, os camundongos tratados com oxamato apresentaram baços e outros órgãos menores, contagens sanguíneas melhores, menos danos teciduais e viveram mais tempo. Seus macrófagos esplênicos voltaram a um perfil mais equilibrado, semelhante a M2, e os níveis gerais de lactato no baço diminuíram. Administrar lactato extra teve o efeito oposto, ampliando ainda mais o baço. Para um observador leigo, a mensagem é clara: neste modelo de leucemia, o lactato não é apenas um resíduo metabólico — é um sinal poderoso que prende as células imunes em um estado inflamatório que sustenta o tumor e ajuda a impulsionar o aumento do órgão.
O que isso pode significar para cuidados futuros
Este trabalho redefine a esplenomegalia na eritroleucemia aguda como um processo ativo alimentado por um ciclo de retroalimentação entre o metabolismo do câncer e o sistema imune. Ao mostrar que bloquear a produção de lactato pode reverter mudanças imunes nocivas e reduzir o inchaço do baço em camundongos, o estudo aponta para uma nova classe de terapias “metabólico‑imunes”. Embora muito mais pesquisas sejam necessárias para testar segurança, cronograma e combinações com drogas padrão para leucemia, mirar esse circuito conduzido pelo lactato pode um dia ajudar a proteger pacientes do aumento doloroso e perigoso do baço e retardar a progressão desta agressiva neoplasia sanguínea.
Citação: Yang, M., Xie, D., Zhang, Y. et al. Lactate-mediated macrophage polarization promotes splenomegaly in acute erythroleukemia. Cell Death Dis 17, 373 (2026). https://doi.org/10.1038/s41419-026-08612-5
Palavras-chave: eritroleucemia aguda, metabolismo do lactato, polarização de macrófagos, esplenomegalia, microambiente tumoral