Clear Sky Science · fr
La polarisation macrophagique médiée par le lactate favorise la splénomégalie dans laérythroleucémie aiguë
Pourquoi cela compte pour les patients et leurs familles
Lorsque des cancers du sang comme la leucémie s’étendent au‑delà de la moelle osseuse, ils peuvent provoquer un gonflement spectaculaire de la rate, entraînant douleur, anémie et complications potentiellement mortelles. Cette étude pose une question apparemment simple : qu’est‑ce qui, précisément, fait tant grossir la rate dans une forme rare mais agressive de leucémie appelée érythroleucémie aiguë ? Les chercheurs mettent en évidence un coupable inattendu — un sous‑produit métabolique courant appelé lactate — et montrent que réduire la production de lactate chez la souris peut réduire la taille de la rate et prolonger la survie.
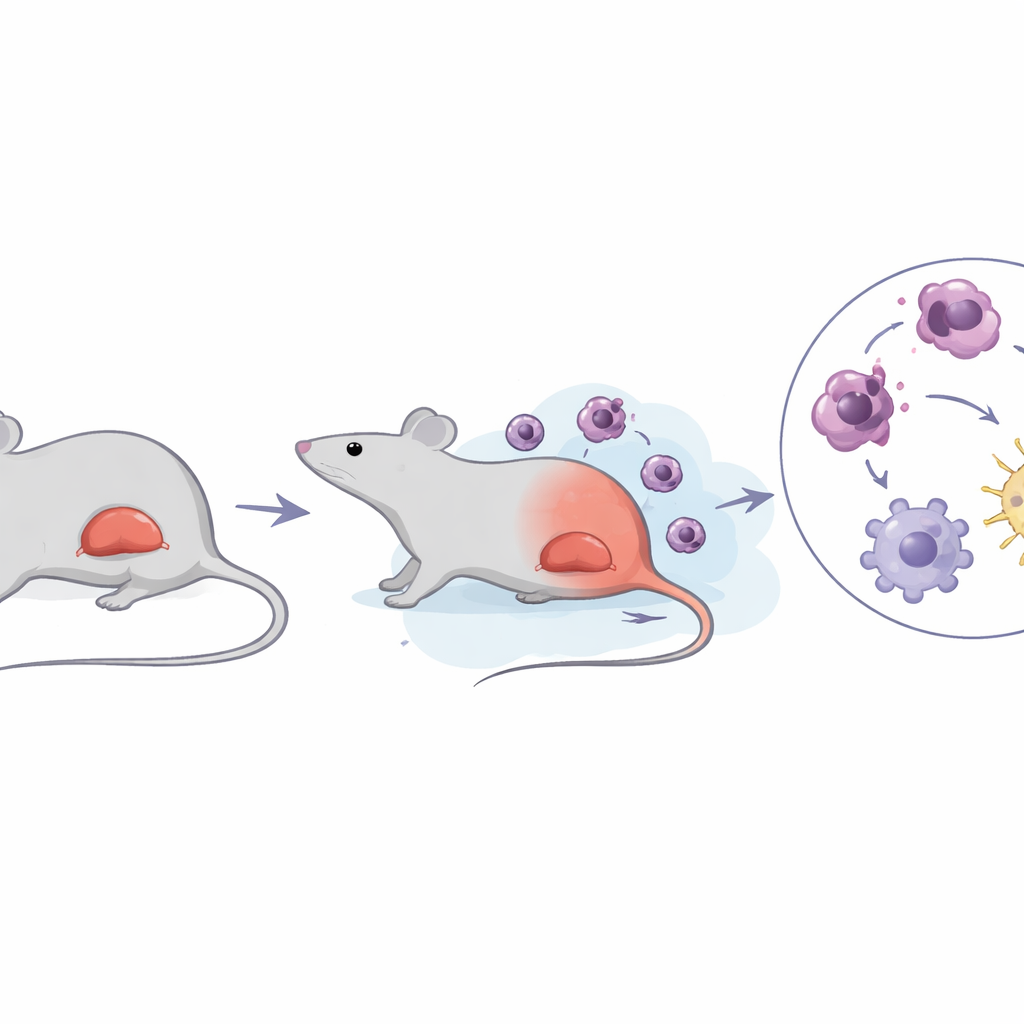
Un gonflement dangereux de la rate
L’érythroleucémie aiguë est un sous‑type peu fréquent de leucémie myéloïde aiguë caractérisé par une prolifération explosive de précurseurs immatures des globules rouges et un pronostic très sombre, avec une survie moyenne mesurée en mois. De nombreux patients développent une splénomégalie, où la rate prend une taille importante et se remplit de cellules leucémiques. En utilisant un modèle murin bien établi infecté par le virus de la leucémie murine de Friend, les auteurs ont suivi avec soin la progression de la maladie. Ils ont confirmé que les souris développaient une anémie, des numérations leucocytaires très élevées et des rates fortement agrandies, reflétant de près la condition humaine. Fait important, ils ont observé que l’augmentation de la taille de la rate survenait en premier ; ce n’est que plus tard que les niveaux de lactate — un produit de dégradation du métabolisme des sucres — augmentaient fortement dans la rate.
Quand la combustion du sucre se dérègle
Les cellules cancéreuses favorisent souvent une manière rapide mais inefficace de brûler le sucre, connue sous le nom de glycolyse, qui produit du lactate même lorsque l’oxygène est disponible. L’analyse protéomique (à grande échelle des protéines) des rates malades de souris a révélé que des enzymes clés contrôlant l’utilisation et la production des sucres étaient déséquilibrées. Les enzymes convertissant le pyruvate en lactate étaient suractivées, tandis que celles recyclant le lactate en glucose étaient diminuées. Les transporteurs qui importent le lactate dans les cellules étaient également plus actifs. Ensemble, ces modifications ont créé un piège métabolique : le sucre affluait dans la rate, était rapidement orienté vers le lactate, et ce lactate était retenu plutôt que d’être éliminé, conduisant à un environnement riche en lactate à l’intérieur de l’organe gonflé.
Des cellules immunitaires poussées vers un profil inflammatoire
La rate n’est pas seulement un filtre pour les cellules sanguines ; c’est aussi un carrefour immunitaire actif. L’équipe a découvert que des niveaux élevés de lactate modifiaient le comportement des cellules immunitaires, en particulier des macrophages — des cellules polyvalentes qui peuvent soit entretenir l’inflammation (souvent qualifié d’état de type M1), soit aider à résoudre les dommages et rétablir l’équilibre (état de type M2). Dans les rates leucémiques, le nombre total de macrophages diminuait, mais les cellules restantes étaient fortement orientées vers l’état inflammatoire de type M1. Les protéines à l’intérieur de ces macrophages présentaient une augmentation de la « lactylation », une marque chimique dérivée du lactate, suggérant que l’excès de lactate reprogrammait directement le fonctionnement de ces cellules. Parallèlement, d’autres types cellulaires immunitaires étaient déséquilibrés, avec moins de lymphocytes T et davantage de cellules myéloïdes, témoignant d’un remodelage plus large du paysage immunitaire splénique.
Une boucle autorenforçante conduite par le lactate
Pour établir la relation de cause à effet, les chercheurs sont passés à des expériences en culture cellulaire. Lorsqu’ils exposaient des macrophages de souris au virus causant la leucémie, les cellules augmentaient leur consommation de sucre, produisaient du lactate et adoptaient un profil inflammatoire de type M1. Bloquer deux interrupteurs de signalisation à l’intérieur des cellules, appelés STAT1 et mTOR, empêchait à la fois l’augmentation du lactate et la bascule vers l’état inflammatoire. Fait marquant, baigner des macrophages dans du lactate seul suffisait à les pousser vers l’état de type M1 et à les faire produire encore plus de lactate, créant un cercle vicieux. Le fluide prélevé sur ces macrophages conditionnés par le lactate faisait proliférer plus rapidement des cellules d’érythroleucémie humaine, montrant que les cellules immunitaires altérées soutenaient activement la tumeur.
Rompre le cercle pour protéger la rate
Enfin, l’équipe a demandé si interrompre la production de lactate chez des animaux vivants pouvait modifier le cours de la maladie. Ils ont traité des souris leucémiques avec l’oxamate, un médicament qui inhibe l’enzyme responsable de la production de lactate. Par rapport aux animaux non traités, les souris traitées par oxamate avaient des rates et d’autres organes de plus petite taille, des numérations sanguines améliorées, moins de lésions tissulaires et une survie prolongée. Leurs macrophages spléniques revenaient vers un profil plus équilibrant, de type M2, et les niveaux globaux de lactate dans la rate diminuaient. L’administration de lactate supplémentaire produisait l’effet inverse, augmentant encore la taille de la rate. Pour un observateur non spécialiste, le message est clair : dans ce modèle de leucémie, le lactate n’est pas qu’un déchet métabolique — c’est un signal puissant qui enferme les cellules immunitaires dans un mode inflammatoire et pro‑tumeur et contribue à l’agrandissement de l’organe.
Ce que cela pourrait signifier pour les soins futurs
Ce travail revoit la splénomégalie dans l’érythroleucémie aiguë comme un processus actif alimenté par une boucle de rétroaction entre le métabolisme tumoral et le système immunitaire. En montrant que bloquer la production de lactate peut inverser des changements immunitaires nocifs et atténuer le gonflement de la rate chez la souris, l’étude ouvre la voie à une nouvelle classe de thérapies « métabo‑immunes ». Si des recherches supplémentaires sont nécessaires pour évaluer la sécurité, le calendrier et les combinaisons avec les traitements standard de la leucémie, cibler ce circuit entraîné par le lactate pourrait un jour aider à protéger les patients contre une splénomégalie douloureuse et dangereuse et ralentir la progression de ce cancer du sang agressif.
Citation: Yang, M., Xie, D., Zhang, Y. et al. Lactate-mediated macrophage polarization promotes splenomegaly in acute erythroleukemia. Cell Death Dis 17, 373 (2026). https://doi.org/10.1038/s41419-026-08612-5
Mots-clés: érythroleucémie aiguë, métabolisme du lactate, polarisation des macrophages, splénomégalie, microenvironnement tumoral