Clear Sky Science · sv
MARCO främjar kolangiokarcinogenes genom att inducera immunsuppression och dess riktade blockering minskar tumörtillväxt
Varför detta betyder något för framtida cancerbehandlingar
Intrahepatisk kolangiokarcinom är en sällsynt men dödlig cancer i leverns små gallgångar. De flesta patienter upptäcks sent, dagens behandlingar är till stor del palliativa och överlevnaden är fortsatt dålig. Denna studie avslöjar hur en specifik typ av immuncell i tumören hjälper cancern att växa, sprida sig och motstå behandling — och visar att blockering av en enda molekyl på dessa celler kan bromsa sjukdomen i experimentella modeller. Arbetet pekar på ett nytt sätt att "omprogrammera" tumörmiljön så att kroppens egna försvar bättre kan bekämpa denna cancer.
En seglivad levercancer med få alternativ
Kolangiokarcinom är den näst vanligaste primära levercancern och är vanligtvis tystlåten tills den nått ett avancerat stadium. Kirurgi är ofta inte längre möjlig, och även när tumörer kan avlägsnas återkommer de hos de flesta patienter. Standardbehandling för avancerad sjukdom kombinerar kemoterapi med hämmare av immunkontrollpunkter, men detta förlänger livet bara måttligt och endast en minoritet av patienterna svarar väl. Många intrahepatisk kolangiokarcinom beter sig som så kallade "kalla" tumörer: de innehåller få cancerdödande T‑celler och är istället fyllda med celler som dämpar immunsvaret. Bland de mest rikliga av dessa finns tumörassocierade makrofager, immunceller som antingen kan angripa eller hjälpa tumörer beroende på hur de är "programmerade".
En makrofagreceptor kommer i fokus
Med hjälp av stora single‑cell RNA‑sekvenseringsdataset från friska, cirrotiska och cancerösa mänskliga leverceller fann forskarna att en scavenger‑receptor kallad MARCO främst finns på makrofager. I intrahepatisk kolangiokarcinom verkar MARCO nästan uteslutande finnas på tumörassocierade makrofager snarare än på själva cancercellerna. Patienter vars tumörer innehöll fler MARCO‑positiva makrofager hade sämre överlevnad i flera oberoende kohorter. Detaljerad genanalys visade att MARCO‑bärande makrofager uppvisar en immunsuppressiv profil: de kopplas till signalsystem som dämpar immunsvar, främjar aktivitet hos så kallade TH2‑typ immunsvar och deltar i ombyggnad av den vävnadsmatris som omger tumörcellerna.
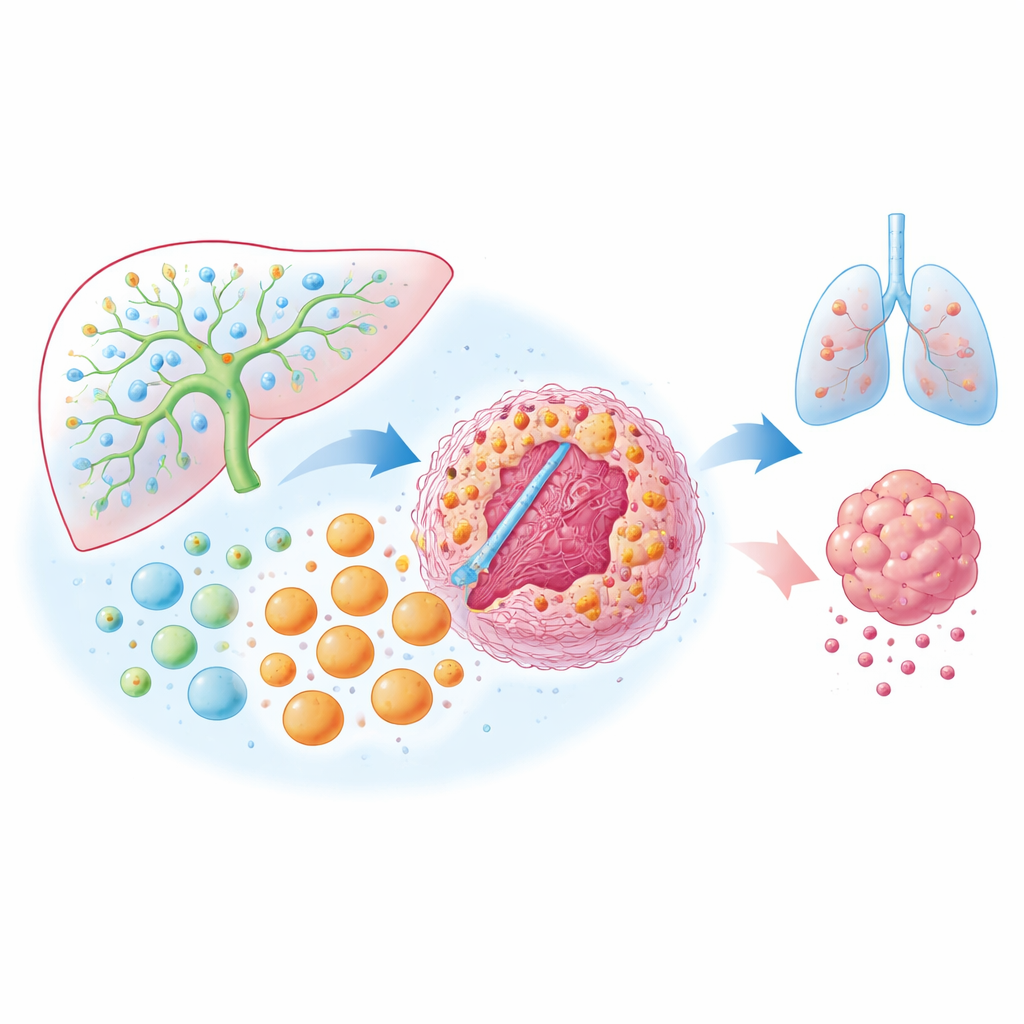
Hur tumörmiljön omformas
Gruppen undersökte därefter vad som driver MARCO‑uttryck och vad dessa makrofager gör inne i tumören. De fann att cytokiner associerade med TH2‑svar, särskilt IL‑4 och IL‑13 producerade av T‑celler, starkt ökar MARCO‑nivåer i makrofager. I tumörprover var MARCO‑rika områden också rika på kollagen och aktiverade fibroblaster, kännetecken för en tät fibrotisk stroma som kan avskärma tumörer och hindra immuncellers inträde. Spatial proteinprofilering visade att regioner med MARCO‑positiva makrofager hade högre nivåer av kontrollpunktsmolekyler såsom PD‑L1 på immunceller och PD‑1 på T‑celler, i linje med ett starkt nedreglerat lokalt immunsvar. Tillsammans framställer dessa fynd MARCO‑positiva makrofager som centrala organisatörer av en stel, ärrliknande och immunologiskt tyst nisch runt tumören.
Lärdomar från musmodeller
För att testa om MARCO endast är en markör eller en aktiv drivkraft i sjukdomen använde forskarna flera musmodeller av intrahepatisk kolangiokarcinom. Möss som konstruerats för att sakna MARCO utvecklade färre och mindre gallgångstumörer, uppvisade mindre leverfibros och behöll bättre leverfunktion än sina normala motsvarigheter. Deras tumörer innehöll färre makrofager med fibrotiska eller immunsuppressiva drag, färre celler associerade med TH2‑typ svar och cytotoxiska T‑celler som var mindre "uttömda" baserat på uttryck av kontrollpunktsmarkörer. I en ortotop modell — där gallgångscancerceller implanteras direkt i levern — överlevde MARCO‑deficienta möss längre och utvecklade färre lungmetastaser. I cellkulturförsök blev tumörceller som exponerades för MARCO‑deficienta makrofager mindre rörliga, vilket tyder på att dessa makrofager direkt påverkar cancerstammens förmåga att migrera. Viktigt är att behandling av normala möss med en antikropp som blockerar MARCO minskade tumörvolymen och efterliknade många av de fördelar som sågs hos MARCO‑utsläckta djur.
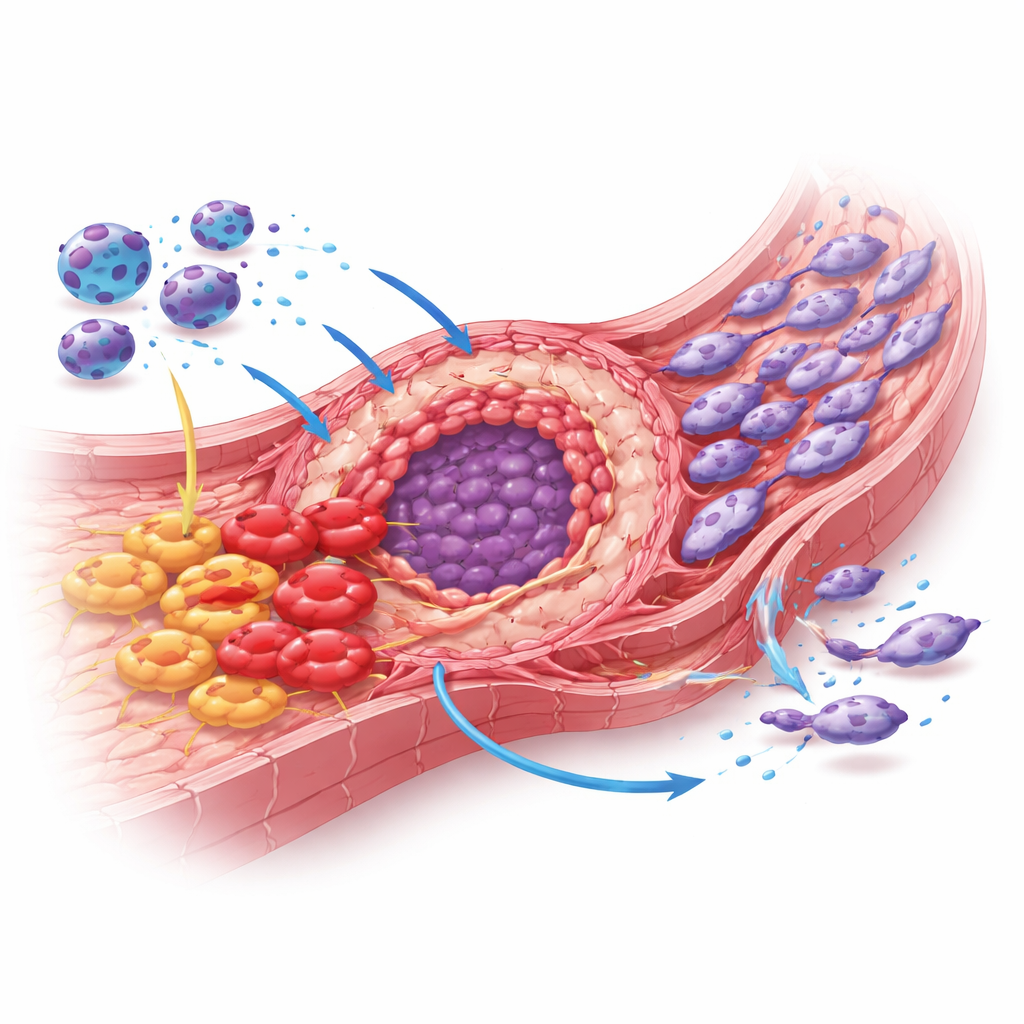
Mot makrofagriktad immunterapi
Tillsammans tyder de mänskliga uppgifterna och musexperimenten på att MARCO‑positiva makrofager både skyddar intrahepatisk kolangiokarcinom från immunangrepp och fysiskt omformar tumörmiljön för att gynna tillväxt och spridning. Genom att vårda en TH2‑förskjuten, fibrotisk och kontrollpunktsrik miljö bidrar dessa celler till att omvandla tumören till en starkt skyddad nisch. Upptäckten att en MARCO‑blockerande antikropp kan krympa tumörer hos möss öppnar för möjligheten till en ny klass behandlingar som specifikt omställer makrofager istället för att rikta in sig direkt på cancerceller. För patienter med denna svårbehandlade cancer skulle terapier riktade mot MARCO en dag kunna komplettera befintlig kemoterapi och kontrollpunktshämmare, och omvandla "kalla" tumörer till sådana som är mer sårbara för kroppens egna immunsvar.
Citering: Agirre-Lizaso, A., Huici-Izagirre, M., O’Rourke, C.J. et al. MARCO promotes cholangiocarcinogenesis by inducing immunosuppression and its targeting reduces tumor growth. Sig Transduct Target Ther 11, 158 (2026). https://doi.org/10.1038/s41392-026-02657-w
Nyckelord: kolangiokarcinom, tumörmikromiljö, tumörassocierade makrofager, immunterapi, fibros