Clear Sky Science · it
MARCO promuove la colangiocarcinogenesi inducendo immunosoppressione e il suo bersaglio riduce la crescita tumorale
Perché questo conta per i trattamenti oncologici futuri
Il colangiocarcinoma intraepatico è un tumore raro ma letale dei piccoli dotti biliari all'interno del fegato. La maggior parte dei pazienti viene diagnosticata in fase avanzata, i trattamenti attuali sono per lo più palliativi e la sopravvivenza resta scarsa. Questo studio svela come un tipo specifico di cellula immunitaria presente nel tumore favorisca la crescita, la diffusione e la resistenza alla terapia—e mostra che bloccare una singola molecola su queste cellule può rallentare la malattia in modelli sperimentali. Il lavoro indica una nuova strategia per “riprogrammare” l'ambiente tumorale affinché le difese dell'organismo possano combattere meglio questo tumore.
Un tumore epatico ostinato con poche opzioni
Il colangiocarcinoma è il secondo tumore primario del fegato più comune e di solito è silente fino allo stadio avanzato. La chirurgia spesso non è più possibile e, anche quando i tumori possono essere rimossi, recidivano nella maggior parte dei pazienti. Il trattamento standard per la malattia avanzata combina chemioterapia e inibitori dei checkpoint immunitari, ma questo allunga la vita solo modestamente e solo una minoranza di pazienti risponde bene. Molti colangiocarcinomi intraepatici si comportano come tumori “freddi”: contengono pochi linfociti T in grado di uccidere le cellule tumorali e sono invece pieni di cellule che attenuano le risposte immunitarie. Tra le più abbondanti vi sono i macrofagi associati al tumore, cellule immunitarie che possono attaccare o assistere il tumore a seconda di come siano “programmate”.
Un recettore dei macrofagi al centro dell'attenzione
Analizzando ampi dataset di RNAseq a cellula singola provenienti da fegati umani sani, cirrotici e cancerosi, i ricercatori hanno rilevato che un recettore scavenger chiamato MARCO è presente principalmente sui macrofagi. Nel colangiocarcinoma intraepatico, MARCO sembra comparire quasi esclusivamente sui macrofagi associati al tumore piuttosto che sulle cellule tumorali stesse. I pazienti i cui tumori contenevano un maggior numero di macrofagi MARCO‑positivi avevano una sopravvivenza globale peggiore in diversi coorti indipendenti. Un'analisi genica dettagliata ha mostrato che i macrofagi che esprimono MARCO presentano un profilo immunosoppressivo: sono collegati a vie di segnalazione che smorzano l'attacco immunitario, favoriscono l'attività di risposte immunitarie di tipo TH2 e partecipano al rimodellamento della matrice tissutale che circonda le cellule tumorali.
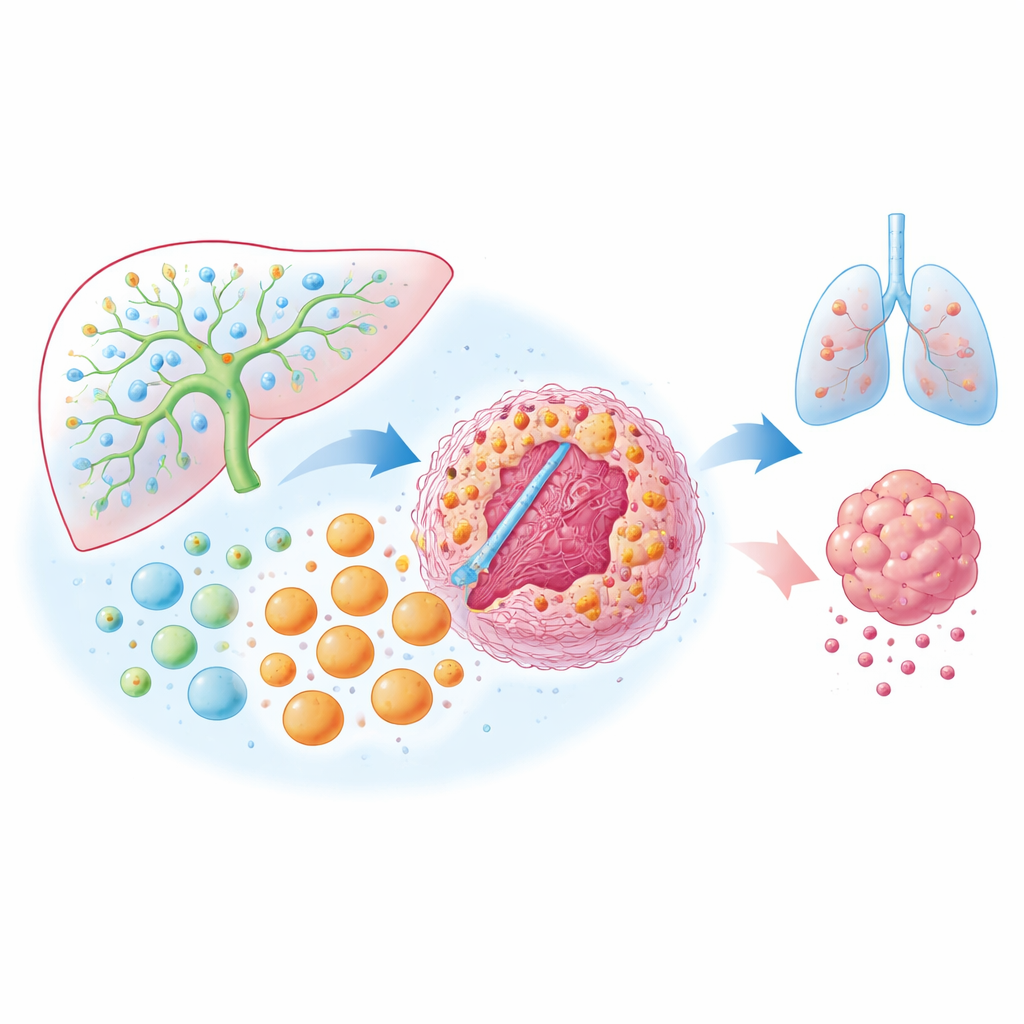
Come viene rimodellato l'ambiente tumorale
Il gruppo ha quindi indagato cosa induca l'espressione di MARCO e cosa facciano questi macrofagi all'interno del tumore. Hanno scoperto che citochine associate alle risposte TH2, in particolare IL‑4 e IL‑13 prodotte dai linfociti T, aumentano fortemente i livelli di MARCO nei macrofagi. Nei campioni tumorali, le aree ricche di MARCO risultavano anche ricche di collagene e fibroblasti attivati, segni distintivi di uno stroma fibrotico denso che può isolare i tumori e ostacolare l'ingresso delle cellule immunitarie. Il profilo spaziale delle proteine ha mostrato che le regioni contenenti macrofagi MARCO‑positivi avevano livelli più alti di molecole di checkpoint come PD‑L1 sulle cellule immunitarie e PD‑1 sui linfociti T, coerente con una risposta immunitaria locale fortemente soppressa. Nel loro insieme, questi risultati dipingono i macrofagi MARCO‑positivi come organizzatori centrali di una nicchia rigida, cicatriziale e immunologicamente silente attorno al tumore.
Lezioni dai modelli murini
Per verificare se MARCO sia solo un marcatore o un vero e proprio driver della malattia, i ricercatori si sono rivolti a diversi modelli murini di colangiocarcinoma intraepatico. I topi ingegnerizzati per non esprimere MARCO hanno sviluppato meno tumori dei dotti biliari e di dimensioni più piccole, hanno mostrato meno fibrosi epatica e mantenuto una funzione epatica migliore rispetto ai controlli normali. I loro tumori contenevano meno macrofagi con caratteristiche fibrotiche o immunosoppressive, meno cellule associate a risposte di tipo TH2 e linfociti T citotossici meno “esausti” valutati tramite l'espressione di marker di checkpoint. In un modello ortotopico—dove le cellule tumorali dei dotti biliari sono impiantate direttamente nel fegato—i topi privi di MARCO sono sopravvissuti più a lungo e hanno sviluppato meno metastasi polmonari. In esperimenti in coltura cellulare, le cellule tumorali esposte a macrofagi privi di MARCO sono diventate meno mobili, suggerendo che questi macrofagi influenzano direttamente la capacità migratoria del cancro. Importante, il trattamento di topi normali con un anticorpo che blocca MARCO ha ridotto il volume tumorale, imitando molti dei benefici osservati negli animali knockout per MARCO.
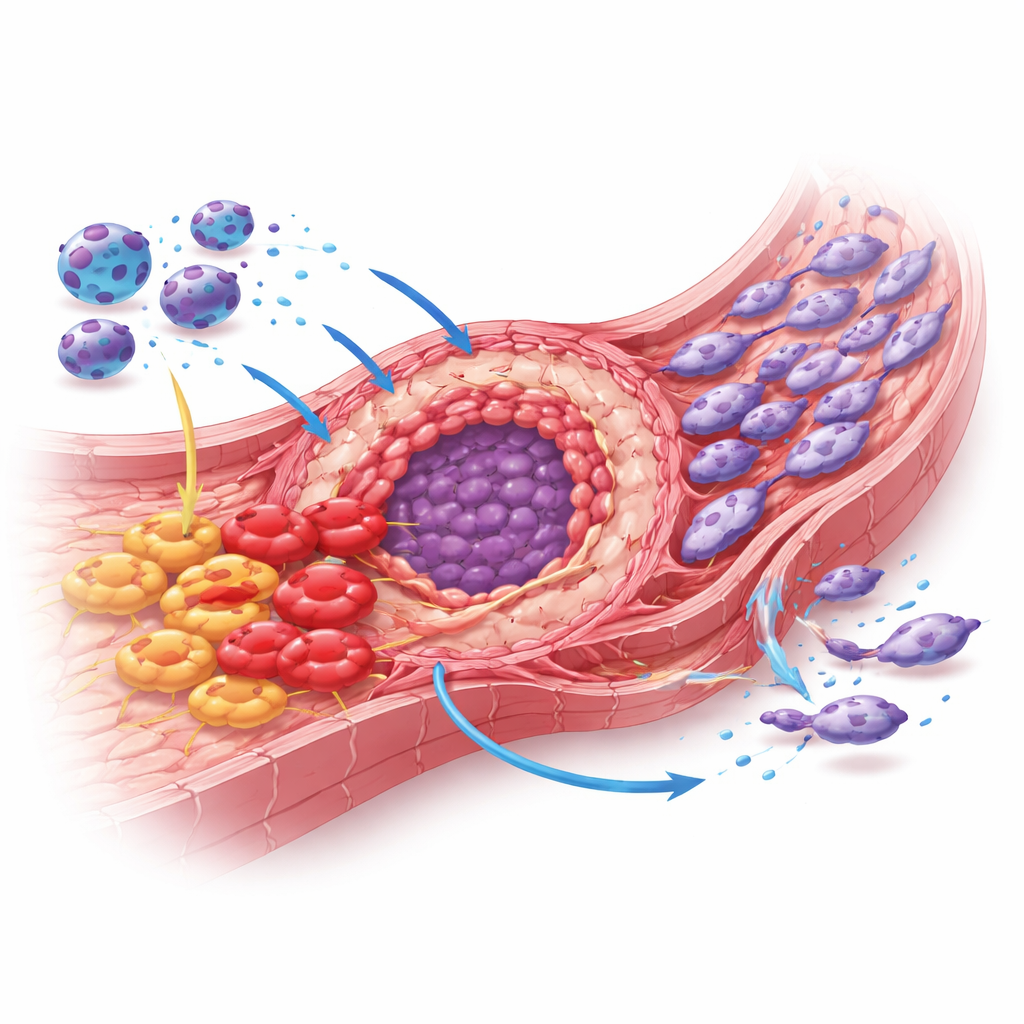
Verso un'immunoterapia mirata sui macrofagi
Considerati insieme, i dati umani e gli esperimenti murini suggeriscono che i macrofagi MARCO‑positivi sia proteggono il colangiocarcinoma intraepatico dall'attacco immunitario sia rimodellano fisicamente l'ambiente tumorale a favore della crescita e della diffusione. Nutrendo un ambiente orientato al TH2, fibrotico e ricco di checkpoint, queste cellule contribuiscono a convertire il tumore in una nicchia altamente protettiva. Il fatto che un anticorpo anti‑MARCO possa ridurre i tumori nei topi apre la possibilità di una nuova classe di terapie che ritunano specificamente i macrofagi invece di colpire direttamente le cellule tumorali. Per i pazienti affetti da questo tumore difficile da trattare, terapie mirate a MARCO potrebbero un giorno integrare la chemioterapia e gli inibitori dei checkpoint attuali, trasformando i tumori “freddi” in bersagli più vulnerabili alle difese immunitarie dell'organismo.
Citazione: Agirre-Lizaso, A., Huici-Izagirre, M., O’Rourke, C.J. et al. MARCO promotes cholangiocarcinogenesis by inducing immunosuppression and its targeting reduces tumor growth. Sig Transduct Target Ther 11, 158 (2026). https://doi.org/10.1038/s41392-026-02657-w
Parole chiave: colangiocarcinoma, microambiente tumorale, macrofagi associati al tumore, immunoterapia, fibrosi