Clear Sky Science · ru
Проблемы стандартизации in vitro тестов на цитотоксичность для сравнительной оценки риска устройств холодной атмосферы плазмы
Почему это важно для будущих методов лечения ран
Холодная атмосферная плазма — по сути возбужденный газ при комнатной температуре — испытывается как новый метод помощи трудно заживающим ранам и борьбы с микроорганизмами. Несколько медицинских устройств на этой технологии уже доступны на рынке, но они существенно различаются по способу генерации и доставки плазмы. В исследовании поставлен, на первый взгляд, простой вопрос с существенными последствиями: можно ли лабораторными тестами справедливо сравнить безопасность и эффективность разных устройств, или мы непроизвольно сравниваем «яблоки и апельсины»?
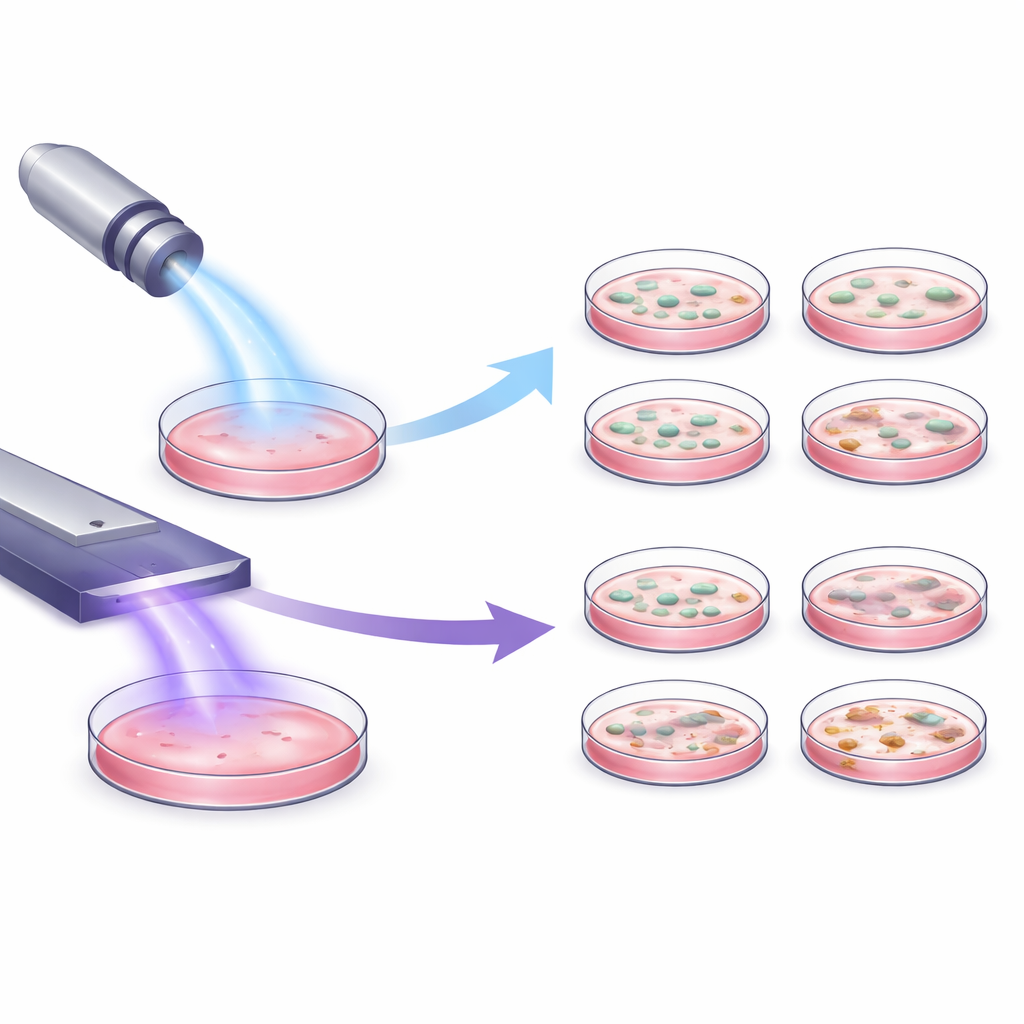
Разные приборы — разное воздействие на клетки
Исследователи изучили два медицински одобренных плазменных устройства с принципиально разными способами работы: ручкоподобный джет, направляющий сфокусированный поток плазмы, и плоское устройство, создающее плазму непосредственно над обрабатываемой поверхностью. На трех типах клеток, связанных с кожей, выращенных в чашках, их подвергали воздействию каждого устройства при кажущихся одинаковыми лабораторных настройках. Несмотря на общие условия, реакция клеток оказалась очень различной. Плоское устройство вызывало минимальную или отсутствующую потерю жизнедеятельности клеток, тогда как джет последовательно снижал метаболизм клеток в зависимости от времени — чем дольше экспозиция, тем сильнее эффект. Даже поток инертного газа от джета без активной плазмы заметно влиял на здоровье клеток, что показывает: движение газа само по себе может вызывать стресс у клеток.
То, как вы перемещаете прибор, меняет результат
Чтобы исследовать значение геометрии обработки, команда варьировала траекторию движения плазменного джета над чашкой. Они сравнили узкую круговую траекторию возле центра с большей окружностью, покрывающей большую площадь поверхности чашки. Обе схемы с течением времени снижали активность клеток, но большая окружность делала это значительно быстрее. Иными словами, размер области, фактически охваченной джетом — деталь, которая может не указываться подробно — драматично менял силу воздействия на клетки, даже при одинаковом времени экспозиции и настройках устройства. Это подчеркивает, что простые лабораторные параметры, такие как «время обработки», могут скрывать важные различия в истинном взаимодействии плазмы с клетками.
Попытка обойти проблему с помощью плазмено обработанной жидкости
Поскольку прямое облучение клеток плазменными джетами сопровождается сложностями — например, перемещением жидкости потоками газа и несоответствием размеров прибора и чашки — исследователи также проверили косвенный подход. Они использовали металлическую сетку и буферный раствор (PBS) для создания «плазмено кондиционированной» жидкости, которую затем переносили на клетки. На первый взгляд это выглядело перспективно: обработка небольшого объема жидкости через сетку давала раствор, который явно снижал активность клеток при применении. Но когда они обработали значительно больший объем при почти тех же условиях и затем использовали только небольшую его часть на клетках, эффект в значительной мере исчезал. Команда расширила исследование, применив различные по размеру лунки для культуры с разной глубиной жидкости и временем обработки, и снова обнаружила, что простое масштабирование времени обработки пропорционально объему не восстанавливает равную силу воздействия.
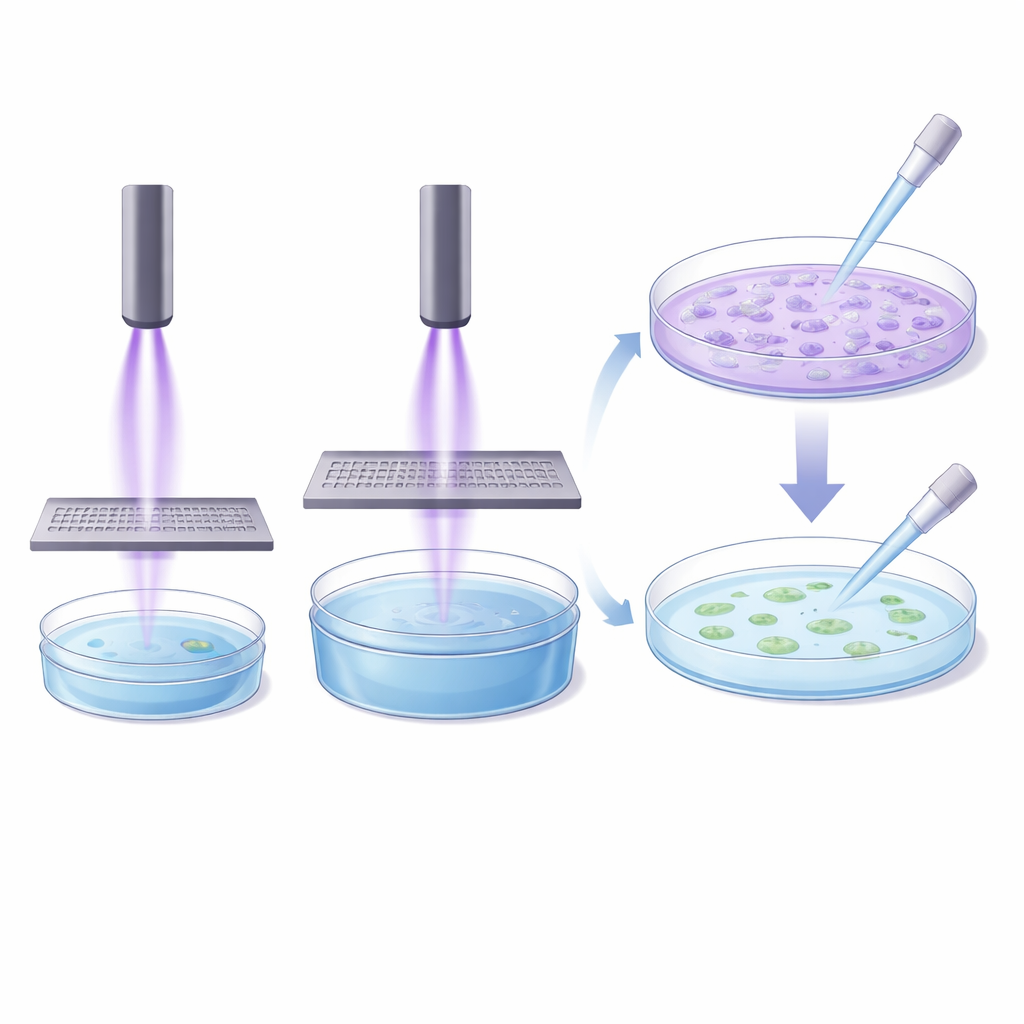
Почему простое масштабирование терпит неудачу в лаборатории
Косвенные эксперименты показали, что связь между объемом обрабатываемой жидкости, временем экспозиции и силой воздействия на клетки не является тривиальной. Для больших объемов требовалось не просто пропорционально больше времени; зачастую требовалось существенно дольше, и даже тогда они часто не достигали эффекта, наблюдаемого для меньших объемов. Авторы отмечают, что косвенные методы также упускают короткоживущие реактивные компоненты плазмы, а также электрические и электромагнитные эффекты, которые, вероятно, вносят вклад в биологическое действие плазмы. Вкупе с результатами прямых обработок это показывает: нет единого «универсального» лабораторного протокола, который надежно сравнивал бы все плазменные устройства.
Что это значит для пациентов и исследователей
Для тех, кто надеется, что плазма станет рутинным, безопасным и эффективным методом лечения ран или инфекций, послание осторожное, но конструктивное. Исследование демонстрирует, что небольшие различия в конструкции устройства и обращении в лаборатории могут приводить к большим различиям в реакции клеток, делая прямые сопоставления вводящими в заблуждение, если эти детали игнорировать. Вместо того чтобы принуждать все устройства к одному жесткому тесту, авторы предлагают, чтобы исследователи тщательно и прозрачно сообщали ключевые технические и экспериментальные детали при каждом запуске эксперимента. С таким более полным контекстом результаты разных лабораторий и устройств можно по-прежнему сопоставлять и объединять, создавая более надежную базу доказательств перед тем, как новые плазменные инструменты будут проверены в строгих клинических испытаниях.
Цитирование: Boeckmann, L., Ficht, PK., Bernhardt, T. et al. Challenges in the standardization of in vitro cytotoxicity assays for comparative risk assessment of cold atmospheric pressure plasma devices. Sci Rep 16, 10503 (2026). https://doi.org/10.1038/s41598-026-45037-8
Ключевые слова: холодная атмосферная плазма, заживление ран, культура клеток / анализы, сравнение медицинских устройств, параметры обработки