Clear Sky Science · fr
Défis de la standardisation des tests de cytotoxicité in vitro pour l’évaluation comparative des risques des dispositifs plasma à pression atmosphérique froide
Pourquoi cela compte pour les traitements futurs des plaies
Le plasma à pression atmosphérique froide — essentiellement un gaz énergisé à température ambiante — est à l’essai comme nouvelle méthode pour aider les plaies rebelles à cicatriser et lutter contre les germes. Plusieurs dispositifs médicaux utilisant cette technologie sont déjà commercialisés, mais ils diffèrent fortement dans leur mode de production et de délivrance du plasma. Cette étude pose une question apparemment simple mais aux grandes implications : les tests de laboratoire peuvent‑ils comparer équitablement la sécurité et l’efficacité de ces différents dispositifs, ou bien confondons‑nous des pommes et des oranges sans nous en rendre compte ?
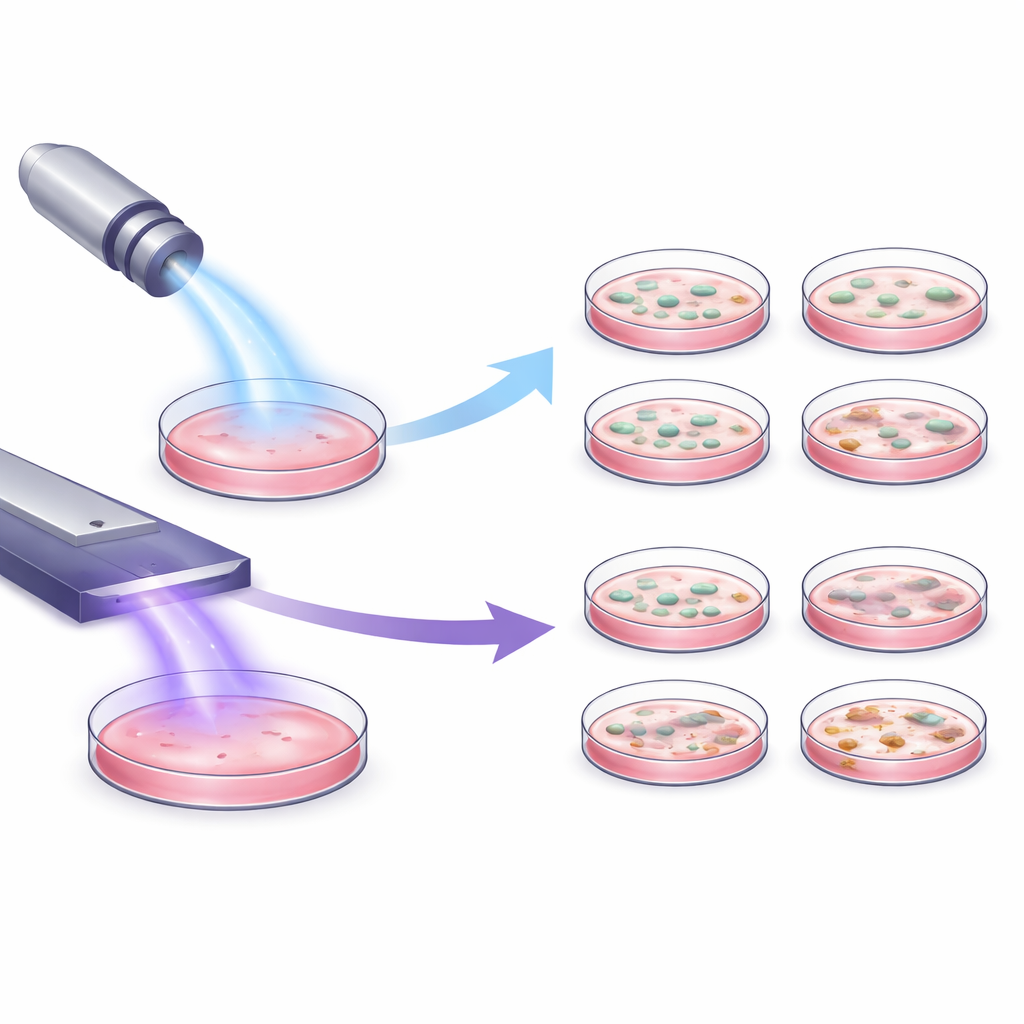
Des outils différents, des impacts cellulaires différents
Les chercheurs ont examiné deux dispositifs plasma approuvés médicalement qui fonctionnent de façon très différente : un jet en forme de stylet qui souffle un flux focalisé de plasma, et un appareil plat qui crée le plasma directement au‑dessus de la surface traitée. En utilisant trois types de cellules cutanées cultivées en boîte de Pétri, ils ont exposé les cellules à chaque dispositif dans des conditions de laboratoire qui semblaient identiques. Malgré ces conditions partagées, les cellules ont réagi de manière très différente. L’appareil plat a entraîné peu ou pas de perte d’activité cellulaire, tandis que le jet a réduit le métabolisme cellulaire de façon nette et dépendante du temps — c’est‑à‑dire que des expositions plus longues ont produit des effets plus marqués. Même le flux de gaz inerte issu du jet, en l’absence de plasma actif, a affecté de manière mesurable la santé cellulaire, montrant que le mouvement du gaz seul peut stresser les cellules.
La façon dont on déplace l’appareil change le résultat
Pour explorer l’importance de la géométrie du traitement, l’équipe a varié la manière dont le jet plasma était déplacé au‑dessus de la boîte. Ils ont comparé un trajet circulaire serré près du centre à un cercle plus large qui couvrait davantage la surface de la boîte. Les deux motifs ont réduit l’activité cellulaire avec le temps, mais le cercle plus large l’a fait beaucoup plus rapidement. En d’autres termes, la taille de la zone effectivement balayée par le jet — un paramètre qui peut ne pas être rapporté en détail — modifiait dramatiquement l’intensité de l’effet sur les cellules, même lorsque le temps d’exposition et les réglages de l’appareil étaient identiques. Cela souligne que des paramètres de laboratoire apparemment simples comme « temps de traitement » peuvent masquer des différences importantes dans l’interaction réelle du plasma avec les cellules.
Essayer un raccourci avec un liquide traité au plasma
Parce que l’exposition directe des cellules aux jets plasma entraîne des complications — comme le déplacement du liquide par le flux gazeux et l’inadéquation des tailles entre l’appareil et la boîte — les chercheurs ont testé une approche indirecte. Ils ont utilisé une grille métallique et une solution tampon (PBS) pour créer un liquide « conditionné au plasma », qui a ensuite été transféré sur les cellules. À première vue, cela semblait prometteur : traiter un petit volume de liquide à travers la grille produisait une solution qui réduisait clairement l’activité cellulaire une fois appliquée. Mais lorsqu’ils ont traité un volume beaucoup plus grand dans des conditions presque identiques puis n’ont utilisé qu’une petite portion de celui‑ci sur les cellules, l’effet a largement disparu. L’équipe a approfondi l’idée en utilisant des puits de culture de tailles différentes avec des profondeurs de liquide et des durées de traitement variées, et a de nouveau constaté que le simple fait d’adapter linéairement le temps de traitement au volume ne restituait pas la même intensité.
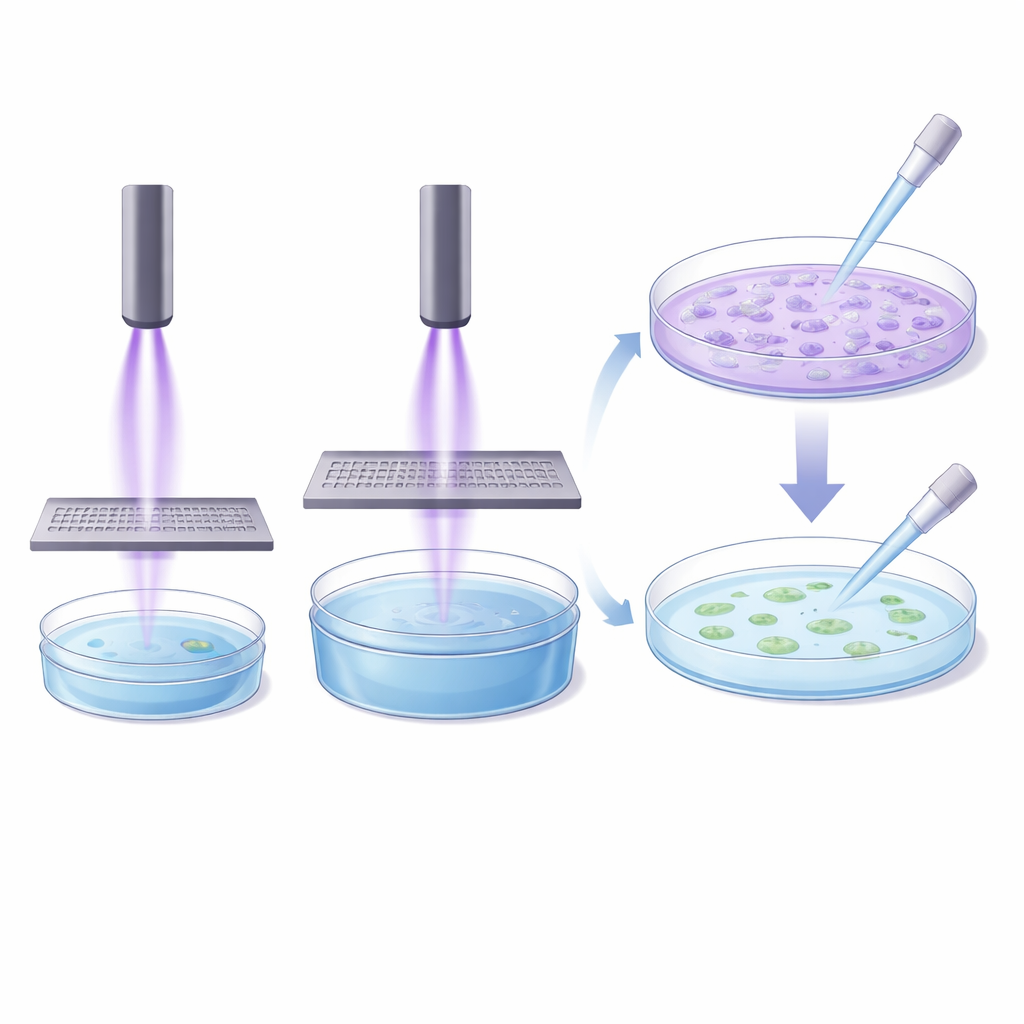
Pourquoi l’échelle simple échoue en laboratoire
Les expériences indirectes ont révélé que la relation entre la quantité de liquide traitée, la durée d’exposition et l’intensité de l’effet sur les cellules n’est pas simple. Les volumes plus importants n’avaient pas seulement besoin d’un temps proportionnellement plus long ; ils nécessitaient des durées beaucoup plus longues et, même ainsi, échouaient souvent à égaler l’impact des petits volumes. Les auteurs soulignent que les méthodes indirectes manquent aussi des composants réactifs à vie courte du plasma, ainsi que des effets électriques et électromagnétiques qui contribuent probablement à son action biologique. Avec les résultats des traitements directs, cela montre qu’aucun protocole de laboratoire « universel » ne peut comparer de manière fiable tous les dispositifs plasma.
Ce que cela signifie pour les patients et les chercheurs
Pour ceux qui espèrent que le plasma devienne un traitement routinier, sûr et efficace pour les plaies ou les infections, le message est prudent mais constructif. L’étude montre que de petites différences de conception des dispositifs et de manipulation en laboratoire peuvent entraîner de grandes variations de réponse cellulaire, rendant les comparaisons directes trompeuses si ces détails sont ignorés. Plutôt que d’imposer à tous les dispositifs un test unique et rigide, les auteurs soutiennent que les chercheurs devraient rapporter de manière exhaustive et transparente les détails techniques et expérimentaux clés à chaque expérience. Avec ce contexte plus riche, les résultats provenant de différents laboratoires et dispositifs pourront néanmoins être comparés et combinés de façon significative, construisant une base de preuves plus fiable avant que les nouveaux outils plasma ne soient évalués dans des essais cliniques rigoureux.
Citation: Boeckmann, L., Ficht, PK., Bernhardt, T. et al. Challenges in the standardization of in vitro cytotoxicity assays for comparative risk assessment of cold atmospheric pressure plasma devices. Sci Rep 16, 10503 (2026). https://doi.org/10.1038/s41598-026-45037-8
Mots-clés: plasma atmosphérique froid, cicatrisation des plaies, tests en culture cellulaire, comparaison de dispositifs médicaux, paramètres de traitement