Clear Sky Science · pl
Wyzwania w standaryzacji in vitro testów cytotoksyczności dla porównawczej oceny ryzyka urządzeń wytwarzających zimną plazmę atmosferyczną
Dlaczego to ma znaczenie dla przyszłych metod leczenia ran
Zimna plazma atmosferyczna — w istocie zjonizowany gaz w temperaturze pokojowej — jest testowana jako nowy sposób wspomagania gojenia opornych ran i zwalczania drobnoustrojów. Kilka urządzeń medycznych wykorzystujących tę technologię jest już na rynku, lecz znacząco różnią się sposobem wytwarzania i dostarczania plazmy. Badanie stawia pozornie proste pytanie o dalekosiężnych konsekwencjach: czy testy laboratoryjne mogą rzetelnie porównywać bezpieczeństwo i skuteczność tych różnych urządzeń, czy też nieświadomie mieszamy jabłka z pomarańczami?
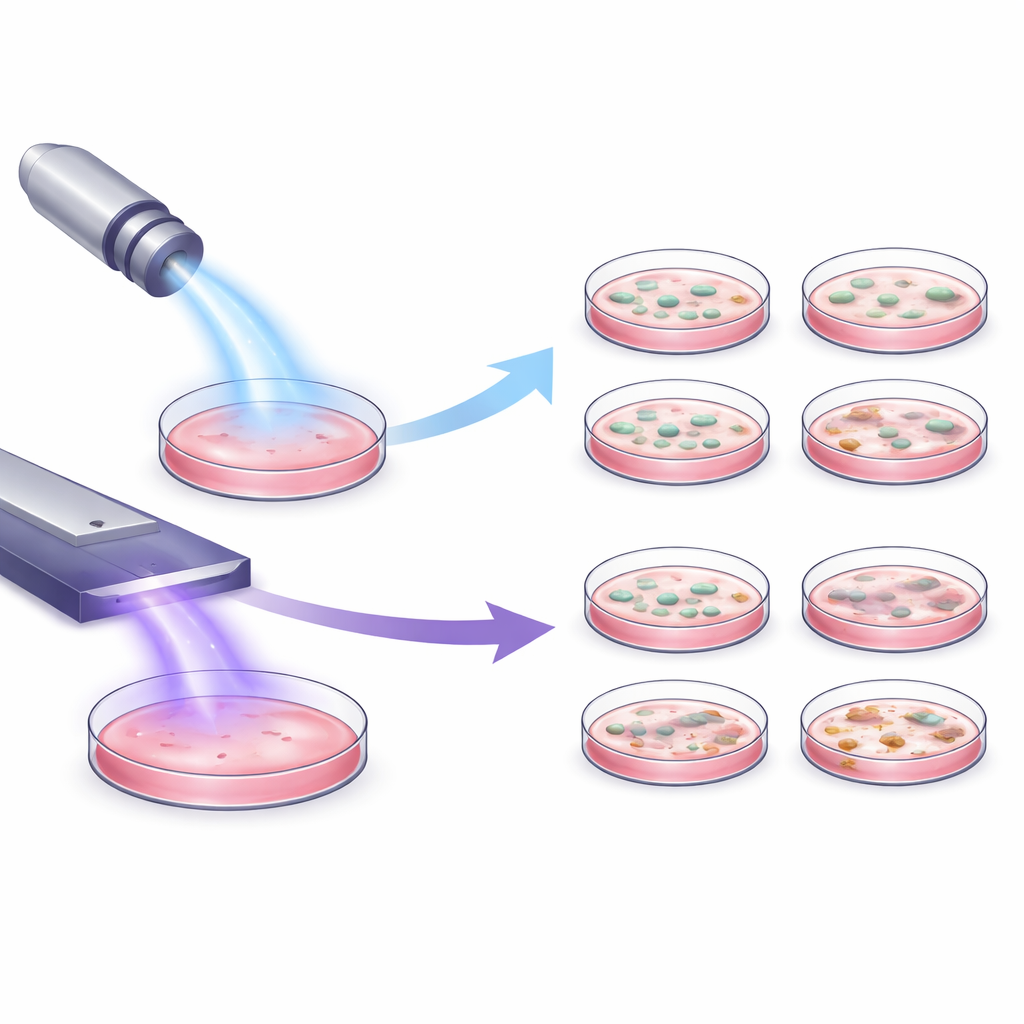
Różne narzędzia, różne oddziaływanie na komórki
Naukowcy zbadali dwa medycznie zatwierdzone urządzenia plazmowe działające na bardzo odmiennych zasadach: przypominający długopis jet, który emituje skoncentrowany strumień plazmy, oraz urządzenie płaskie, które wytwarza plazmę bezpośrednio nad powierzchnią poddawaną zabiegowi. Używając trzech typów komórek związanych ze skórą hodowanych na płytkach, eksponowali komórki na działanie każdego z urządzeń przy pozornie identycznych ustawieniach w laboratorium. Mimo tych wspólnych warunków komórki reagowały bardzo różnie. Urządzenie płaskie wywołało niewielką lub żadną utratę aktywności komórkowej, podczas gdy jet wyraźnie obniżał metabolizm komórek w sposób zależny od czasu — im dłuższa ekspozycja, tym silniejszy efekt. Nawet przepływ obojętnego gazu z jeta, bez aktywnej plazmy, mierzalnie wpływał na zdrowie komórek, co pokazuje, że samo poruszanie gazem może je stresować.
To, jak przesuwasz urządzenie, zmienia wynik
Aby zbadać znaczenie geometrii zabiegu, zespół zmieniał sposób poruszania jetem nad płytką. Porównali ciasną ścieżkę kołową blisko środka z większym okręgiem obejmującym większą powierzchnię płytki. Oba wzory zmniejszały aktywność komórek w miarę upływu czasu, ale większy okrąg działał znacznie szybciej. Innymi słowy, rozmiar obszaru faktycznie zamiatanego przez jet — coś, co może nie być szczegółowo raportowane — dramatycznie zmieniał siłę oddziaływania na komórki, nawet gdy czas ekspozycji i ustawienia urządzenia były takie same. To podkreśla, że proste parametry laboratoryjne, takie jak „czas zabiegu”, mogą maskować istotne różnice w tym, jak plazma rzeczywiście oddziałuje z komórkami.
Próba skrótu z użyciem cieczy po zabiegu plazmą
Ponieważ bezpośrednia ekspozycja komórek na strumienie plazmy wiąże się z komplikacjami — takimi jak przemieszczanie się cieczy pod wpływem przepływu gazu i niedopasowane rozmiary urządzenia i naczynia — badacze przetestowali także podejście pośrednie. Użyli metalowej siatki i buforu (PBS), aby stworzyć „płyn kondycjonowany plazmą”, który następnie przenoszono na komórki. Na pierwszy rzut oka rozwiązanie to wydawało się obiecujące: potraktowanie małej objętości cieczy przez siatkę dało roztwór, który wyraźnie obniżał aktywność komórek po zastosowaniu. Jednak gdy potraktowano znacznie większą objętość w niemal tych samych warunkach, a następnie użyto tylko niewielkiej jej części na komórkach, efekt w dużej mierze znikał. Zespół rozszerzył to podejście, stosując większe i mniejsze dołki hodowlane o różnej głębokości cieczy i czasach zabiegu, i ponownie stwierdził, że proste skalowanie czasu zabiegu proporcjonalnie do objętości nie przywraca równoważnej siły działania.
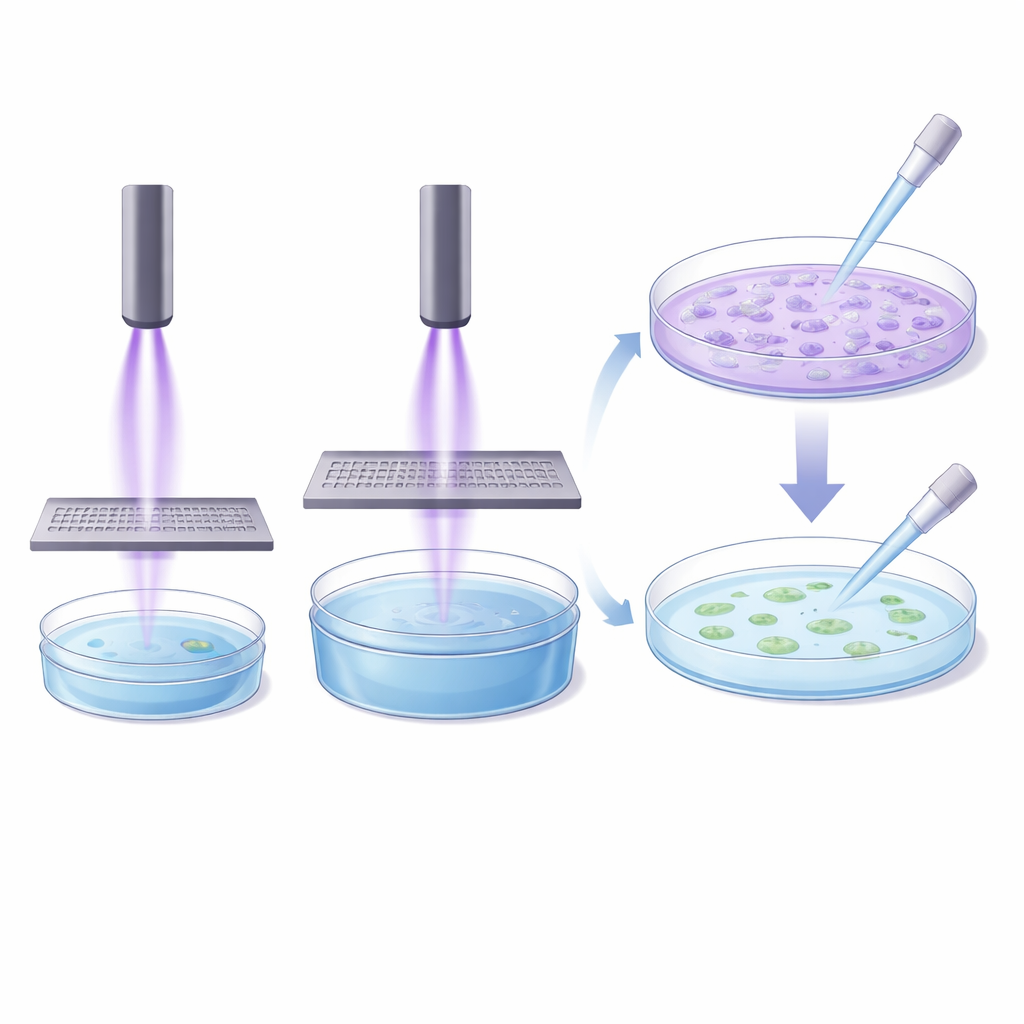
Dlaczego proste skalowanie zawodzi w laboratorium
Eksperymenty pośrednie wykazały, że zależność między ilością traktowanej cieczy, czasem ekspozycji a siłą jej działania na komórki nie jest trywialna. Większe objętości nie potrzebowały tylko proporcjonalnie więcej czasu; wymagały znacznie dłuższego działania, a i tak często nie dorównywały wpływowi mniejszych objętości. Autorzy zauważają, że metody pośrednie pomijają również krótkotrwałe, reaktywne składniki plazmy oraz efekty elektryczne i elektromagnetyczne, które prawdopodobnie przyczyniają się do jej działania biologicznego. W połączeniu z wynikami z zabiegów bezpośrednich pokazuje to, że nie istnieje jeden „uniwersalny” protokół laboratoryjny, który wiarygodnie porównałby wszystkie urządzenia plazmowe.
Co to oznacza dla pacjentów i badaczy
Dla osób liczących, że plazma stanie się rutynowym, bezpiecznym i skutecznym leczeniem ran lub infekcji, przesłanie jest ostrożne, ale konstruktywne. Badanie pokazuje, że drobne różnice w konstrukcji urządzenia i sposobie prowadzenia badań laboratoryjnych mogą prowadzić do istotnych różnic w odpowiedzi komórek, co sprawia, że bezpośrednie porównania „jeden na jednego” mogą wprowadzać w błąd, jeśli te szczegóły są pomijane. Zamiast forsować wszystkie urządzenia do jednego sztywnego testu, autorzy apelują o szczegółowe i przejrzyste raportowanie kluczowych cech technicznych i eksperymentalnych za każdym razem, gdy wykonywane jest badanie. Dzięki tak bogatszemu kontekstowi wyniki z różnych laboratoriów i urządzeń nadal można sensownie porównywać i łączyć, budując bardziej wiarygodną bazę dowodów przed wprowadzeniem nowych narzędzi plazmowych do rygorystycznych badań klinicznych.
Cytowanie: Boeckmann, L., Ficht, PK., Bernhardt, T. et al. Challenges in the standardization of in vitro cytotoxicity assays for comparative risk assessment of cold atmospheric pressure plasma devices. Sci Rep 16, 10503 (2026). https://doi.org/10.1038/s41598-026-45037-8
Słowa kluczowe: zimna plazma atmosferyczna, gojenie ran, testy na hodowlach komórkowych, porównanie urządzeń medycznych, parametry zabiegu