Clear Sky Science · de
Herausforderungen bei der Standardisierung in-vitro-Zytotoxizitätsassays für die vergleichende Risikobewertung von atmosphärischen Kaltplasmageräten
Warum das für künftige Wundbehandlungen wichtig ist
Atmosphärisches Kaltplasma — im Grunde ein aufgeladenes Gas bei Raumtemperatur — wird als neue Methode untersucht, um hartnäckige Wunden zu unterstützen und Krankheitserreger zu bekämpfen. Mehrere medizinische Geräte mit dieser Technologie sind bereits auf dem Markt, unterscheiden sich jedoch stark in der Art, wie sie Plasma erzeugen und abgeben. Diese Studie stellt eine auf den ersten Blick einfache, aber weitreichende Frage: Lassen sich solche Geräte im Labor fair auf Sicherheit und Wirkung vergleichen, oder vergleichen wir unbeabsichtigt Äpfel mit Birnen?
Verschiedene Instrumente, unterschiedliche Auswirkungen auf Zellen
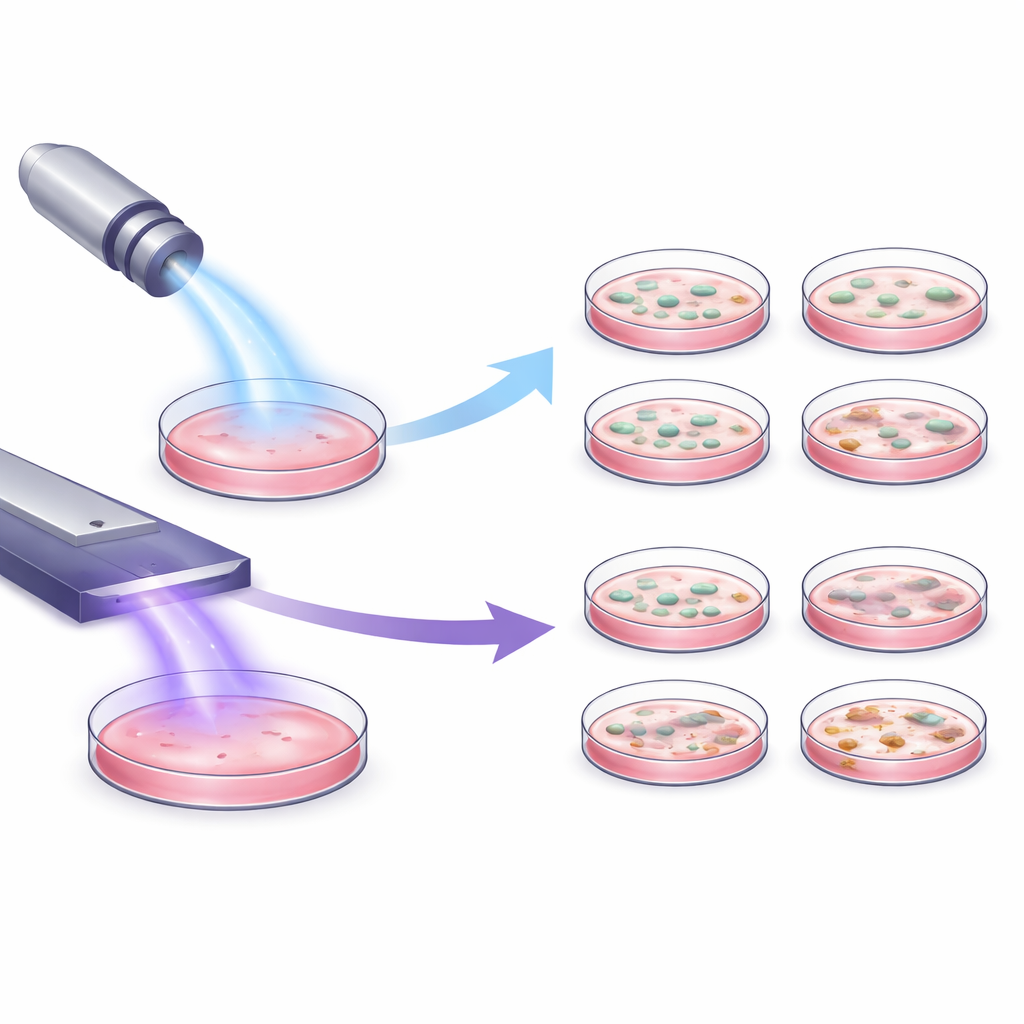
Die Forschenden untersuchten zwei medizinisch zugelassene Plasmageräte, die sehr unterschiedlich funktionieren: eine stiftartige Düse, die einen fokussierten Plasmastrom erzeugt, und ein flaches Gerät, das Plasma direkt oberhalb der behandelten Oberfläche bildet. Mit drei in Schalen kultivierten, hautbezogenen Zelltypen setzten sie die Zellen unter scheinbar identischen Laborbedingungen den jeweiligen Geräten aus. Trotz gleicher Rahmendaten reagierten die Zellen sehr unterschiedlich. Das flache Gerät verursachte kaum bis gar keinen Verlust an Zellaktivität, während das Düsengerät den Zellstoffwechsel in einer klaren, zeitabhängigen Art reduzierte — längere Exposition führte also zu stärkeren Effekten. Sogar der Fluss des inerten Trägergases aus der Düse ohne aktives Plasma beeinflusste messbar die Zellgesundheit, was zeigt, dass allein die Gasströmung Zellen belasten kann.
Wie Sie das Gerät bewegen, verändert das Ergebnis
Um zu untersuchen, wie die Behandlungsgeometrie wirkt, variierte das Team die Bewegungsführung der Plasmadüse über der Schale. Sie verglichen einen engen Kreis in der Nähe der Mitte mit einem größeren Kreis, der mehr der Schalenfläche abdeckte. Beide Bahnmuster verringerten die Zellaktivität mit der Zeit, doch der größere Kreis tat dies deutlich schneller. Anders gesagt: Die Größe des tatsächlich vom Jet überstrichenen Bereichs — ein Parameter, der oft nicht detailliert berichtet wird — veränderte die Wirkstärke dramatisch, selbst wenn Expositionszeit und Geräteeinstellungen gleich blieben. Das unterstreicht, dass einfache Laborparameter wie „Behandlungszeit“ wichtige Unterschiede in der tatsächlichen Wechselwirkung von Plasma mit Zellen verschleiern können.
Ein Versuch mit plasma-behandelter Flüssigkeit als Abkürzung
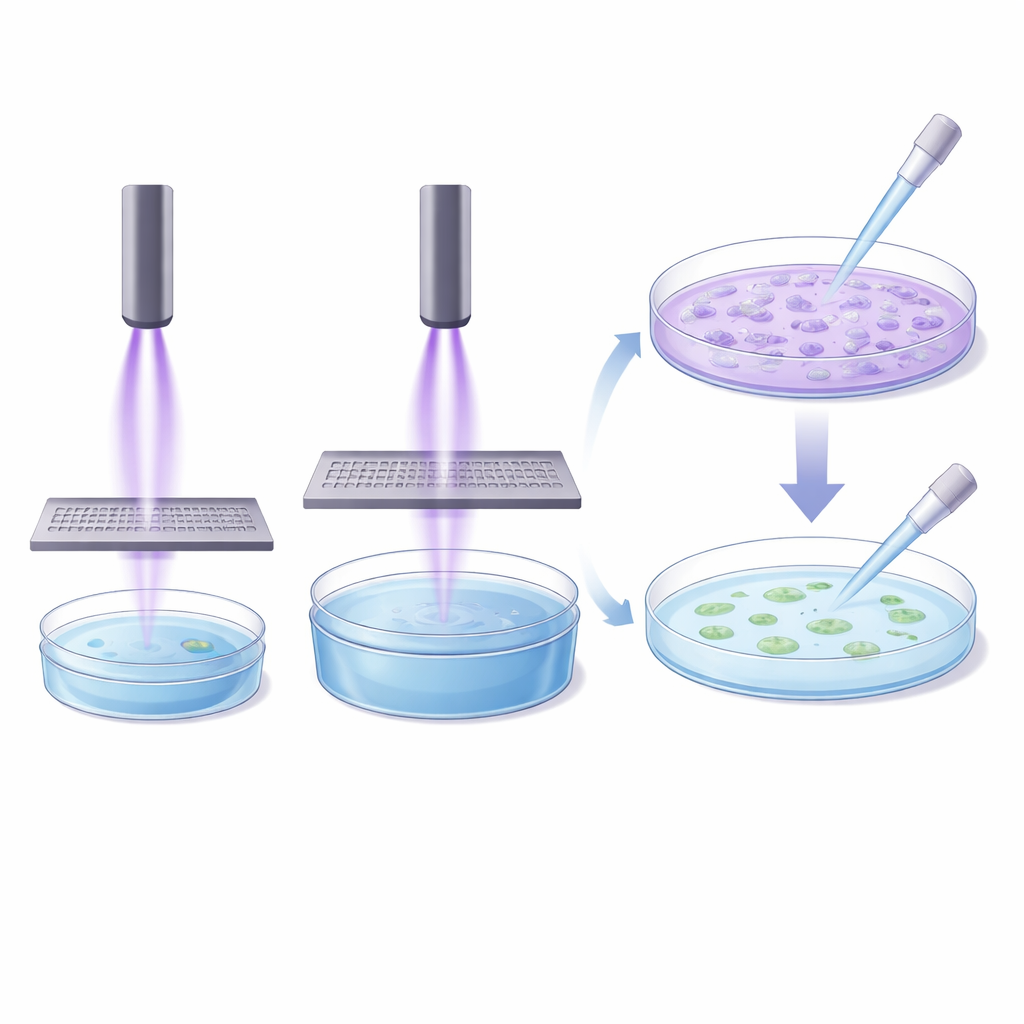
Da die direkte Exposition von Zellen gegenüber Plasmadüsen Komplikationen mit sich bringt — etwa durch von Gasströmungen verdrängte Flüssigkeit und nicht passende Größen von Gerät und Schale — testeten die Forschenden auch einen indirekten Ansatz. Sie verwendeten ein Metallgitter und eine Pufferlösung (PBS), um „plasmakonditionierte“ Flüssigkeit zu erzeugen, die anschließend auf die Zellen übertragen wurde. Auf den ersten Blick erschien das vielversprechend: Die Behandlung eines kleinen Flüssigkeitsvolumens durch das Gitter erzeugte eine Lösung, die nach dem Auftragen die Zellaktivität deutlich reduzierte. Wurde jedoch unter fast gleichen Bedingungen ein wesentlich größeres Volumen behandelt und danach nur ein kleiner Teil davon auf Zellen gegeben, verschwand der Effekt weitgehend. Das Team erweiterte diese Untersuchung, indem es Kulturgefäße unterschiedlicher Größe mit variierenden Flüssigkeitstiefen und Behandlungszeiten nutzte, und fand erneut, dass sich die Wirksamkeit nicht allein durch proportionales Hochskalieren der Behandlungszeit mit dem Volumen wiederherstellen ließ.
Warum einfaches Skalieren im Labor fehlschlägt
Die indirekten Experimente zeigten, dass die Beziehung zwischen behandelteter Flüssigkeitsmenge, Expositionsdauer und Wirkstärke auf Zellen nicht linear ist. Größere Volumina benötigten nicht nur proportional mehr Zeit, sondern oft deutlich längere Zeiten und erreichten dennoch häufig nicht die Wirkung kleinerer Volumina. Die Autorinnen und Autoren weisen außerdem darauf hin, dass indirekte Methoden kurzlebige, reaktive Komponenten des Plasmas sowie elektrische und elektromagnetische Effekte nicht erfassen, die wahrscheinlich zur biologischen Wirkung beitragen. Zusammen mit den Befunden aus den direkten Behandlungen zeigt dies, dass es kein einzelnes „universelles“ Laborprotokoll gibt, mit dem sich zuverlässig alle Plasmageräte vergleichen lassen.
Was das für Patientinnen, Patienten und Forschende bedeutet
Für diejenigen, die hoffen, dass Plasma zu einer routinemäßigen, sicheren und wirksamen Behandlung von Wunden oder Infektionen wird, ist die Botschaft vorsichtig, aber konstruktiv. Die Studie zeigt, dass kleine Unterschiede in Gerätedesign und Laborhandhabung zu großen Unterschieden in der Zellantwort führen können, wodurch direkte Kopf-an-Kopf-Vergleiche irreführend sind, wenn diese Details ignoriert werden. Anstatt alle Geräte in eine starre Prüfung zu pressen, plädieren die Autorinnen und Autoren dafür, technische und experimentelle Details bei jedem Versuch umfassend und transparent zu dokumentieren. Mit diesem reicheren Kontext können Ergebnisse aus verschiedenen Laboren und Geräten dennoch sinnvoll verglichen und zusammengeführt werden, um eine verlässlichere Evidenzbasis aufzubauen, bevor neue Plasmatechnologien in strenge klinische Studien überführt werden.
Zitation: Boeckmann, L., Ficht, PK., Bernhardt, T. et al. Challenges in the standardization of in vitro cytotoxicity assays for comparative risk assessment of cold atmospheric pressure plasma devices. Sci Rep 16, 10503 (2026). https://doi.org/10.1038/s41598-026-45037-8
Schlüsselwörter: atmosphärisches Kaltplasma, Wundheilung, Zellkulturassays, Vergleich medizinischer Geräte, Behandlungsparameter