Clear Sky Science · nl
Uitdagingen bij de standaardisatie van in vitro cytotoxiciteitsassays voor vergelijkende risicobeoordeling van koude atmosferische plasma-apparaten
Waarom dit van belang is voor toekomstige wondbehandelingen
Koude atmosferische plasma—in wezen een geactiveerd gas bij kamertemperatuur—is in onderzoek als een nieuwe manier om hardnekkige wonden te helpen genezen en ziekteverwekkers te bestrijden. Verschillende medische apparaten die deze technologie gebruiken zijn al op de markt, maar ze verschillen sterk in hoe ze plasma opwekken en toedienen. Deze studie stelt een ogenschijnlijk eenvoudige vraag met grote consequenties: kunnen laboratoriumtests eerlijk de veiligheid en effectiviteit van deze verschillende apparaten vergelijken, of vergelijken we ongemerkt appels met peren?
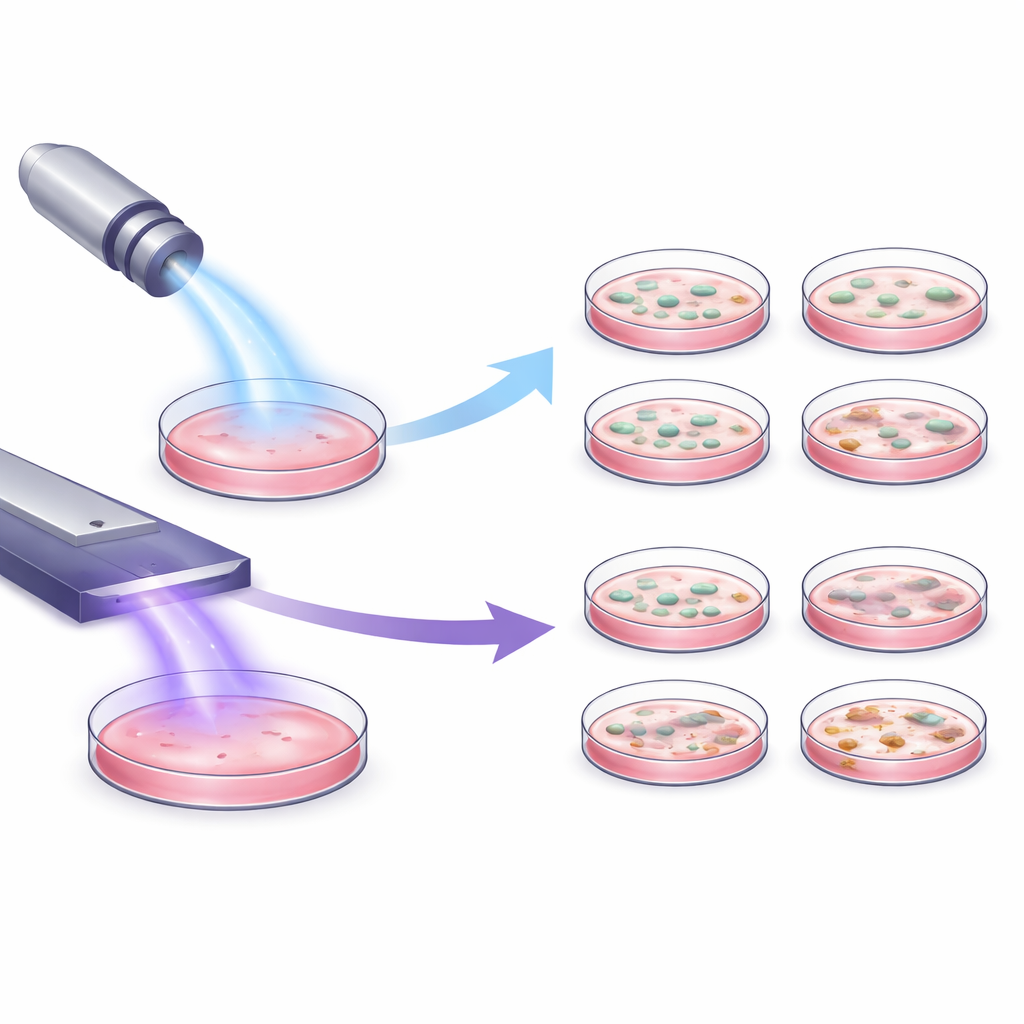
Verschillende instrumenten, verschillende effecten op cellen
De onderzoekers onderzochten twee medisch goedgekeurde plasma-apparaten die op zeer verschillende manieren werken: een penachtige jet die een gerichte stroom plasma blaast, en een vlak apparaat dat plasma direct boven het behandelde oppervlak creëert. Met drie typen huidgerelateerde cellen gekweekt in schalen, hebben ze de cellen aan elk apparaat blootgesteld onder ogenschijnlijk identieke laboratoriuminstellingen. Ondanks deze gedeelde condities reageerden de cellen heel verschillend. Het vlakke apparaat veroorzaakte weinig tot geen verlies van cellulaire activiteit, terwijl het jetapparaat het celmetabolisme duidelijk verminderde in een tijdsafhankelijke mate—duidelijker effect bij langere blootstelling. Zelfs de stroom van inert gas van de jet, zonder actief plasma, beïnvloedde merkbaar de gezondheid van cellen, wat aantoont dat alleen al gasbeweging cellen kan belasten.
Hoe je het apparaat beweegt verandert het resultaat
Om te onderzoeken hoe behandelingsgeometrie ertoe doet, varieerde het team de manier waarop de plasmajet over de schaal werd bewogen. Ze vergeleken een strakke cirkelbaan dicht bij het midden met een grotere cirkel die meer van het oppervlak besloeg. Beide patronen verlaagden de cellulaire activiteit in de tijd, maar de grotere cirkel deed dit veel sneller. Met andere woorden: de grootte van het gebied dat de jet daadwerkelijk afveegt—iets wat mogelijk niet in detail wordt gerapporteerd—wijzigte dramatisch hoe sterk de cellen werden beïnvloed, zelfs wanneer blootstellingstijd en apparaatinstellingen hetzelfde waren. Dit benadrukt dat eenvoudige laboratoriumparameters zoals “behandelingstijd” belangrijke verschillen in hoe plasma echt met cellen interageert kunnen verbergen.
Een snelkoppeling proberen met plasma-behandeld vloeistof
Aangezien directe blootstelling van cellen aan plasmajets complicaties met zich meebrengt—zoals vloeistof die door gasstroom wordt verplaatst en mismatchende apparaat- en schaalafmetingen—testten de onderzoekers ook een indirecte benadering. Ze gebruikten een metalen grid en een buffervloeistof (PBS) om “plasma-geconditioneerde” vloeistof te maken, die vervolgens op cellen werd overgebracht. Op het eerste gezicht leek dit veelbelovend: het behandelen van een kleine vloeistofhoeveelheid door het grid produceerde een oplossing die, eenmaal aangebracht, duidelijk de cellulaire activiteit verminderde. Maar toen ze een veel grotere volume onder vrijwel dezelfde condities behandelden en daarna slechts een klein deel daarvan op cellen gebruikten, verdween het effect grotendeels. Het team breidde dit idee verder uit met grotere en kleinere kweekputjes met verschillende vloeistoftijden en behandelingsdieptes, en vond opnieuw dat het simpelweg opschalen van behandeltijd met volume de gelijkwaardige kracht niet herstelde.
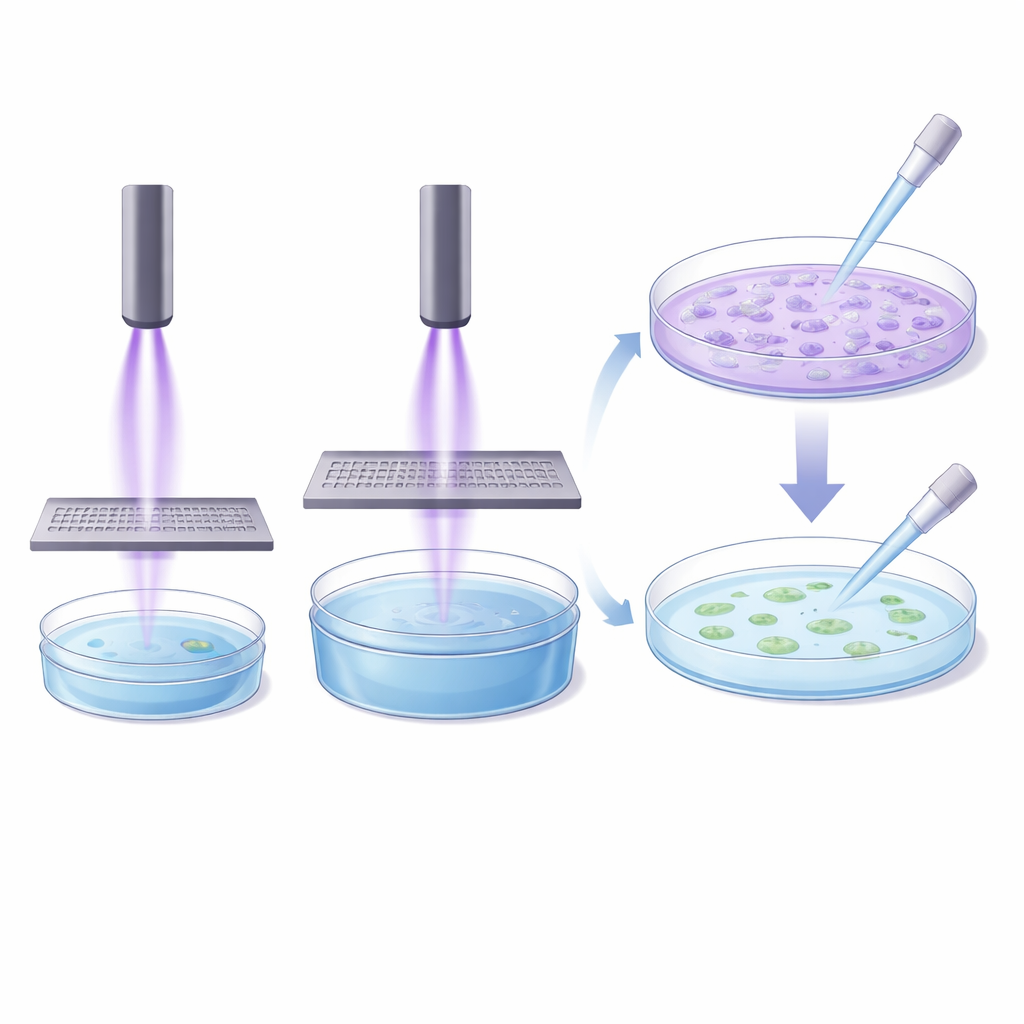
Waarom eenvoudig opschalen in het laboratorium faalt
De indirecte experimenten lieten zien dat de relatie tussen hoeveel vloeistof wordt behandeld, hoe lang die blootgesteld wordt en hoe sterk die cellen beïnvloedt, niet eenvoudig is. Grotere volumes hadden niet alleen proportioneel meer tijd nodig; ze hadden veel langer nodig, en zelfs dan slaagden ze vaak er niet in om de impact van kleinere volumes te evenaren. De auteurs wijzen erop dat indirecte methoden ook kortlevende reactieve componenten van plasma missen, evenals elektrische en elektromagnetische effecten die waarschijnlijk bijdragen aan de biologische werking. Samen met de bevindingen uit directe behandelingen toont dit aan dat er geen enkel “universeel” laboratoriumprotocol bestaat dat betrouwbaar alle plasma-apparaten kan vergelijken.
Wat dit betekent voor patiënten en onderzoekers
Voor mensen die hopen dat plasma een routinematige, veilige en effectieve behandeling voor wonden of infecties wordt, is de boodschap voorzichtig maar constructief. De studie toont aan dat kleine verschillen in apparaatontwerp en laboratoriumhandelingen kunnen leiden tot grote verschillen in hoe cellen reageren, waardoor directe steekproefsgewijze vergelijkingen misleidend kunnen zijn als die details worden genegeerd. In plaats van alle apparaten in één rigide test te dwingen, pleiten de auteurs ervoor dat onderzoekers bij elk experiment belangrijke technische en experimentele details grondig en transparant rapporteren. Met deze rijkere context kunnen resultaten van verschillende laboratoria en apparaten toch zinvol worden vergeleken en gecombineerd, en zo een betrouwbaardere bewijsbasis opbouwen voordat nieuwe plasmamiddelen in rigoureuze klinische proeven worden getest.
Bronvermelding: Boeckmann, L., Ficht, PK., Bernhardt, T. et al. Challenges in the standardization of in vitro cytotoxicity assays for comparative risk assessment of cold atmospheric pressure plasma devices. Sci Rep 16, 10503 (2026). https://doi.org/10.1038/s41598-026-45037-8
Trefwoorden: koude atmosferische plasma, wondgenezing, celkweekassays, vergelijking van medische apparaten, behandelingsparameters