Clear Sky Science · ru
Фрактально‑фракционное моделирование иммунной динамики хронического миелоидного лейкоза методом вейвлетов Лагерра
Почему это важно для рака крови и иммунной системы
Хронический миелоидный лейкоз (ХМЛ) — это рак крови, развивающийся на протяжении многих лет, в то время как иммунная система постоянно пытается его сдержать. У врачей сейчас есть мощные препараты, но предсказать, как клетки опухоли и иммунные клетки пациента будут взаимодействовать во времени, по‑прежнему сложно. В статье предлагается новый вид математической модели, который рассматривает опухоль и иммунный ответ как взаимосвязанную динамическую систему с «памятью» и сложной структурой. Цель — создать более реалистичные инструменты, которые в конечном итоге помогут проектировать более разумные терапии и долгосрочные планы лечения.
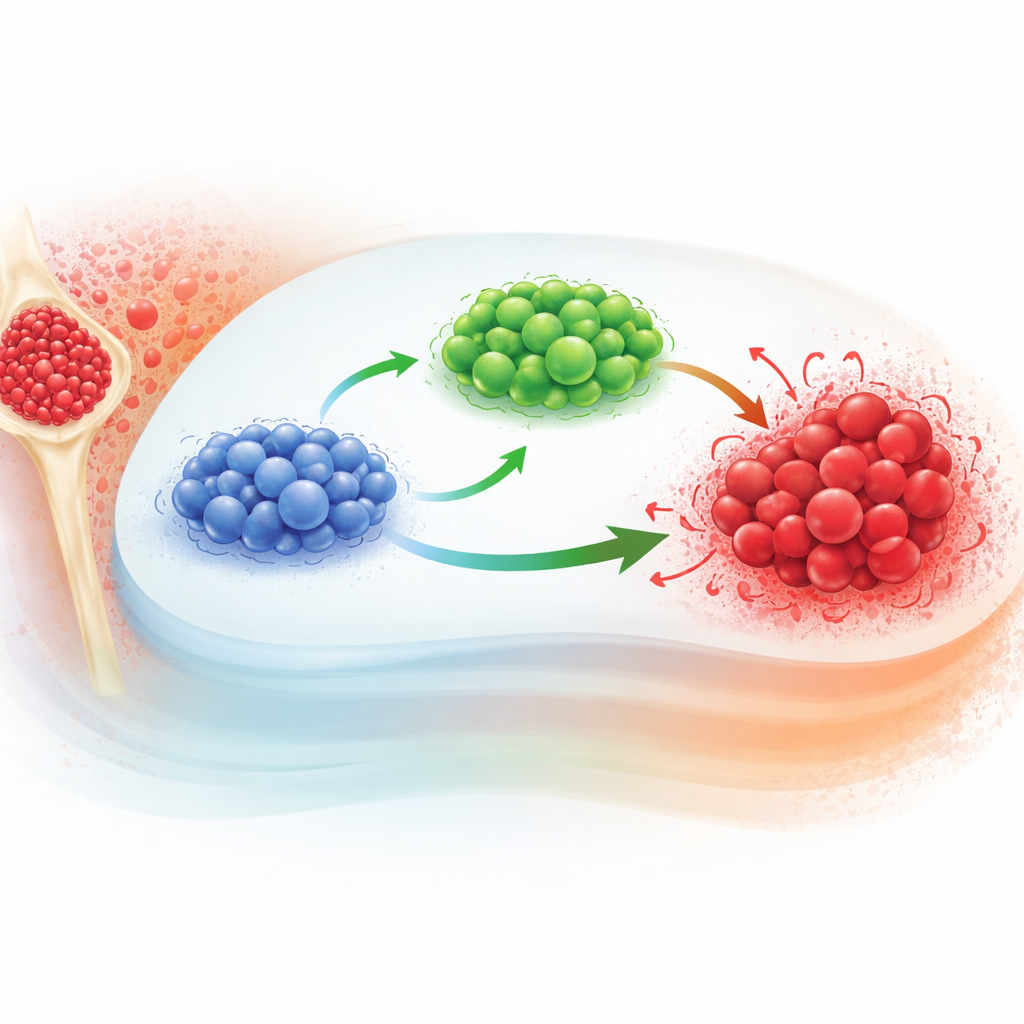
Как взаимодействуют раковые и иммунные клетки
Авторы начинают с существующей модели, отслеживающей три ключевых компонента при ХМЛ: наивные Т‑клетки, эффекторные Т‑клетки и клетки лейкоза. Наивные Т‑клетки — это неопытные новички; при контакте с сигналами от лейкоза часть из них превращается в эффекторные Т‑клетки, передовой отряд, который атакует раковые клетки. Сами раковые клетки растут по закону насыщения: при небольших размерах они быстро расширяются, затем замедляют рост по мере приближения к максимуму, определяемому окружением. Стандартные варианты такой модели используют обычные дифференциальные уравнения, которые предполагают, что дальнейшее развитие зависит только от текущего состояния, а не от предшествующей истории системы.
Добавление памяти и шероховатой структуры в модель
Реальная биология не является безпамятной или гладкой. Иммунные ответы зависят от прошлых контактов, а опухоли растут неравномерно, пятнистой структурой, а не аккуратными шарами. Чтобы учесть оба эффекта одновременно, авторы перестраивают модель ХМЛ с помощью так называемых фрактально‑фракционных операторов. Одна часть, управляемая параметром, называемым фракционным порядком, кодирует память: будущее системы зависит от взвешенной истории прошлого. Другая часть, управляемая фрактальной размерностью, отражает, насколько нерегулярно или «шероховато» устроено окружение опухоли. Когда оба параметра равны единице, модель ведёт себя как классическая; при их уменьшении возрастает влияние истории и геометрической сложности.
Обеспечение корректного поведения новых уравнений
Прежде чем доверять такой модели, нужно показать, что её решения имеют биологический смысл. Авторы доказывают, что при разумных условиях их уравнения имеют единственное решение, которое остаётся положительным и ограниченным во времени — численность клеток никогда не становится отрицательной и не уходит в бесконечность. Затем они анализируют стационарные состояния системы. В этой постановке полностью свободное от опухоли состояние математически неустойчиво: любое небольшое введение клеток лейкоза будет расти. Вместо этого система стремится к равновесию с наличием опухоли, где раковые и иммунные клетки сосуществуют. С помощью методов теории устойчивости они показывают, что это состояние сосуществования не только локально устойчиво, но и глобально притягательно: все реалистичные начальные условия эволюционируют к нему.
Быстрые численные методы для медленно протекающего заболевания
Поскольку новые уравнения включают эффекты памяти и фрактальности, их сложнее решать численно, чем стандартные. Авторы разрабатывают численный приём на основе вейвлетов Лагерра — семейства базисных функций, которые эффективно аппроксимируют поведение на длительных промежутках времени. Этот метод сводит исходную задачу к меньшей системе алгебраических уравнений, которую можно решать быстро и точно. В сравнении с более привычными пошаговыми схемами вейвлет‑метод достигает той же точности при значительно меньших вычислительных затратах, что важно при проведении многочисленных симуляций или подгонке модели под данные пациентов.
Что показывают симуляции о контроле болезни
Имея эти инструменты, авторы исследуют, как изменение параметров памяти и фрактальности влияет на исходы болезни. Понижение фракционного порядка (сильнее выраженная память) или уменьшение фрактальной размерности (более нерегулярная геометрия опухоли) оба способствуют более быстрому сокращению популяции лейкоза и установлению более низкого долгосрочного уровня. Иными словами, система, которая «помнит» своё прошлое, и опухоль, растущая в более сложном пространстве, легче поддаются контролю иммунной системы. Анализ чувствительности показывает, что двумя ключевыми биологическими величинами, определяющими конечный размер опухоли, являются собственная скорость роста рака и скорость, с которой эффекторные Т‑клетки убивают раковые клетки. Это согласуется с текущими терапевтическими стратегиями, сочетающими таргетную терапию для замедления роста опухоли и иммунотерапию для усиления иммунного уничтожения.
Что это значит для пациентов и дальнейшей работы
Проще говоря, исследование делает вывод, что ХМЛ вряд ли исчезнет само по себе; естественная динамика системы ведёт к равновесию, в котором раковые и иммунные клетки сосуществуют. Однако, включая в модель память и структурную сложность, авторы могут описать сценарии, в которых это равновесие оказывается выгодным для пациента, с меньшей долгосрочной нагрузкой опухоли. Их фрактально‑фракционная рамка в сочетании с эффективными численными методами закладывает основу для будущих «цифровых экспериментов» по временам и комбинациям лечения. При наличии клинических данных тот же подход можно персонализировать, подбирая параметры памяти и геометрии для отдельных пациентов, чтобы прогнозировать траектории болезни и оптимизировать терапию.
Цитирование: Khirsariya, S.R., Noori, N. Fractal-fractional modeling of chronic myelogenous leukemia immune dynamics using Laguerre wavelets method. Sci Rep 16, 14106 (2026). https://doi.org/10.1038/s41598-026-43767-3
Ключевые слова: хронический миелоидный лейкоз, динамика опухоль — иммунитет, фракционное исчисление, фрактальное моделирование опухоли, численные вейвлет‑методы