Clear Sky Science · he
מִדּוּל פרקטלי-שברתי של הדינמיקה החיסונית בח leukemia myelogenous כרוני באמצעות שיטת גליות לגארנר
מדוע זה חשוב לסרטן הדם ולמערכת החיסון
לוקמיה מיולוגנית כרונית (CML) היא סרטן דם שמתפתח לאורך שנים, בעוד שמערכת החיסון מנסה כל העת לשלוט בו. כיום קיימים תרופות עוצמתיות, אך עדיין קשה לחזות כיצד תתפתח האינטראקציה בין תאי הסרטן ותאי החיסון של המטופל לאורך הזמן. מאמר זה מציג סוג חדש של מודל מתמטי שטוען את הגידול והתגובה החיסונית כמערכת דינמית מקושרת עם "זיכרון" ומבנה מורכב. המטרה היא לבנות כלים מציאותיים יותר שעשויים בסופו של דבר לסייע בעיצוב טיפולים חכמים ותכניות טיפול ארוכות טווח.
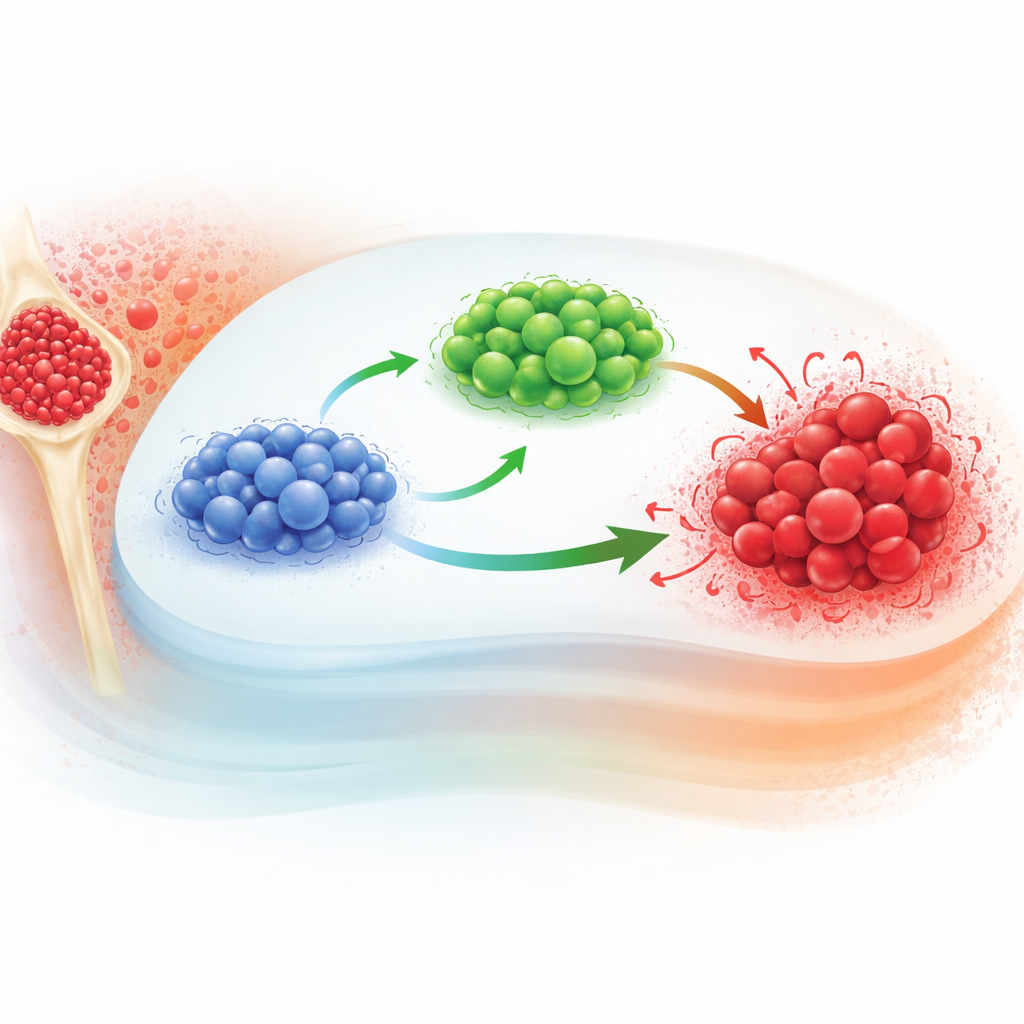
כיצד תאי הסרטן ותאי החיסון מתמקשים
המחברים מתחילים ממודל קיים שעוקב אחר שלושה שחקנים מרכזיים ב־CML: תאי T נאיביים, תאי T מבצעים (effector) ותאי לוקמיה. תאי T נאיביים הם הגיוסיות חסרות הניסיון; כאשר הם נתקלים באותות מהלוקמיה, חלקם הופכים לתאי T מבצעים, הלוחמים בחזית שמתקיפים תאי סרטן. תאי הסרטן עצמם מתרבים לפי חוק רוויה: הם מתרחבים במהירות כשהם קטנים ואז מואטים ככל שמתקרבים לגודל מקסימלי שנקבע על ידי הסביבה שלהם. גרסאות סטנדרטיות של מודל זה משתמשות במשוואות דיפרנציאליות רגילות, שמניחות שהעתיד תלוי רק במצב הנוכחי, לא באופן שבו המערכת הגיעה לשם.
הוספת זיכרון ומבנה מחוספס למודל
ביולוגיה אמיתית אינה חסרת זיכרון או חלקה. תגובות חיסוניות תלויות במפגשים עברוּת, וגידולים מתפתחים בדפוסים לא-סדירים וכתמים ולא בכדורים מסודרים. כדי ללכוד את שני ההשפעות בו־זמנית, המחברים מבססים מחדש את מודל ה־CML באמצעות מה שהם קוראים אופרטורים פרקטליים–שבריים. חלק אחד, הנשלט על ידי פרמטר שנקרא סדר שברי, מקודד זיכרון: עתיד המערכת תלוי בהיסטוריה משוקללת של העבר. החלק השני, הנשלט על ידי מימד פרקטלי, מקל על מידת ה"חספוס" או אי-הסדירות של סביבת הגידול. כאשר שני הפרמטרים מוגדרים כאחד, המודל מתנהג כמו הגרסה הקלאסית; כאשר הם מוקטנים, הזיכרון והמורכבות הגיאומטרית הופכים לחשובים יותר.
להבטיח שמשוואות חדשות יתנהגו באופן סביר
לפני שסומכים על מודל כזה, צריך להראות שהתוצאות שלו הגיוניות מבחינה ביולוגית. המחברים מוכיחים כי, בתנאים סבירים, למשוואותיהם יש פתרון יחיד שנשאר חיובי ומוגבל לאורך הזמן — מספרי התאים לעולם לא הופכים לשליליים או מתפוצצים לאינסוף. לאחר מכן הם מנתחים את מצבי השיווי המשקל של המערכת. במסגרת זו, מצב נקי לחלוטין מגידול אינו יציב מתמטית: כל הוספה קטנה של תאי לוקמיה תגדל. במקום זאת, המערכת נמשכת אל שיווי משקל של "נוכחות גידול" שבו תאי סרטן ותאי חיסון משתכנים יחד. באמצעות כלים מתורת היציבות הם מראים ששיווי משקל זה אינו יציב רק באופן מקומי אלא אטרקטיבי באופן גלובלי: כל תנאי התחלה ריאלי יתפתח לכיוונו.
שיטות נומריות מהירות לפתרון מחלה איטית
מכיוון שהמשוואות החדשות כוללות זיכרון ואפקטים פרקטליים, קשה יותר לפתור אותן במחשב מאשר משוואות סטנדרטיות. המחברים מפתחים טכניקה נומרית המבוססת על גליות לגארנר, משפחת פונקציות בניין שיכולות להתאים ביעילות התנהגות לאורך זמנים ארוכים. שיטה זו הופכת את הבעיה המקורית למערכת קטנה יותר של משוואות אלגבריות שניתן לפתור במהירות ובדיוק. בהשוואה לסכמות מוכרות המבוססות על התקדמויות בזמנים, שיטת הגליות משיגה את אותה דיוק עם הרבה פחות חישובים, מה שחשוב להרצת סימולציות רבות או להתאמת המודל לנתוני מטופל.
מה הסימולציות מגלות לגבי שליטה במחלה
עם הכלים האלה ביד, המחברים בודקים כיצד שינוי בפרמטרי הזיכרון והפרקטל משפיע על תוצאות המחלה. הקטנת סדר השברי (זיכרון חזק יותר) או הקטנת המימד הפרקטלי (גיאומטריה בלתי-סדירה יותר של הגידול) שניהם דוחפים את אוכלוסיית הלוקמיה להתכווצות מהירה יותר ולהשאר ברמה ארוכת טווח נמוכה יותר. במילים אחרות, מערכת שמ"זוכרת" את העבר שלה וגידול שמתפתח בסביבה יותר מורכבת קלים יותר להגבלה על ידי מערכת החיסון. ניתוח רגישות מראה ששני גדלים ביולוגיים שולטים על גודל הגידול הסופי: קצב הגדילה העצמי של הסרטן וקצב שבו תאי T מבצעים הורגים תאים סרטניים. זה מתאים לאסטרטגיות טיפוליות נוכחיות שמשלבות תרופות ממוקדות להאטת גדילת הסרטן עם אימונותרפיות שמגבירות את ההרג החיסוני.
מסקנות עבור מטופלים ועבודה עתידית
במונחים פשוטים, המחקר מסכם כי סביר להניח ש־CML לא תיעלם מעצמה; הנטייה הטבעית של המערכת היא להתייצב לאיזון שבו תאי סרטן ותאי חיסון מתקיימים יחד. עם זאת, על ידי בניית מודל הכולל זיכרון ומורכבות מבנית, המחברים יכולים לתאר תרחישים שבהם האיזון הזה מיטיב עם המטופל, עם עומס סרטני ארוך טווח נמוך יותר. המסגרת הפרקטלית–שברית שלהם, בשילוב עם שיטות נומריות יעילות, מניחה יסודות ל"ניסויים דיגיטליים" עתידיים על תזמון טיפולים ושילובים שלהם. עם נתונים קליניים, אותה גישה תוכל להיות מותאמת אישית, לכוון את פרמטרי הזיכרון והגיאומטריה עבור מטופלים בודדים כדי לחזות מסלולי מחלה ולמקסם את הטיפול.
ציטוט: Khirsariya, S.R., Noori, N. Fractal-fractional modeling of chronic myelogenous leukemia immune dynamics using Laguerre wavelets method. Sci Rep 16, 14106 (2026). https://doi.org/10.1038/s41598-026-43767-3
מילות מפתח: לוקמיה מיולוגנית כרונית, דינמיקת גידול וחיסון, חשבון אינטגרלי-שברי, דִגם פרקטלי של גידול, שיטות גליות נומריות