Clear Sky Science · fr
Modélisation fractale-fractionnaire des dynamiques immunitaires dans la leucémie myéloïde chronique par la méthode des ondelettes de Laguerre
Pourquoi c’est important pour le cancer du sang et le système immunitaire
La leucémie myéloïde chronique (LMC) est un cancer du sang qui évolue sur plusieurs années, tandis que le système immunitaire tente en permanence de le contrôler. Les traitements actuels sont puissants, mais il reste difficile de prédire comment les cellules cancéreuses et immunitaires d’un patient interagiront au fil du temps. Cet article propose un nouveau type de modèle mathématique qui considère la tumeur et la réponse immunitaire comme un système dynamique couplé doté de « mémoire » et d’une structure complexe. L’objectif est de construire des outils plus réalistes qui, à terme, pourront aider à concevoir des thérapies et des stratégies de traitement à long terme plus intelligentes.
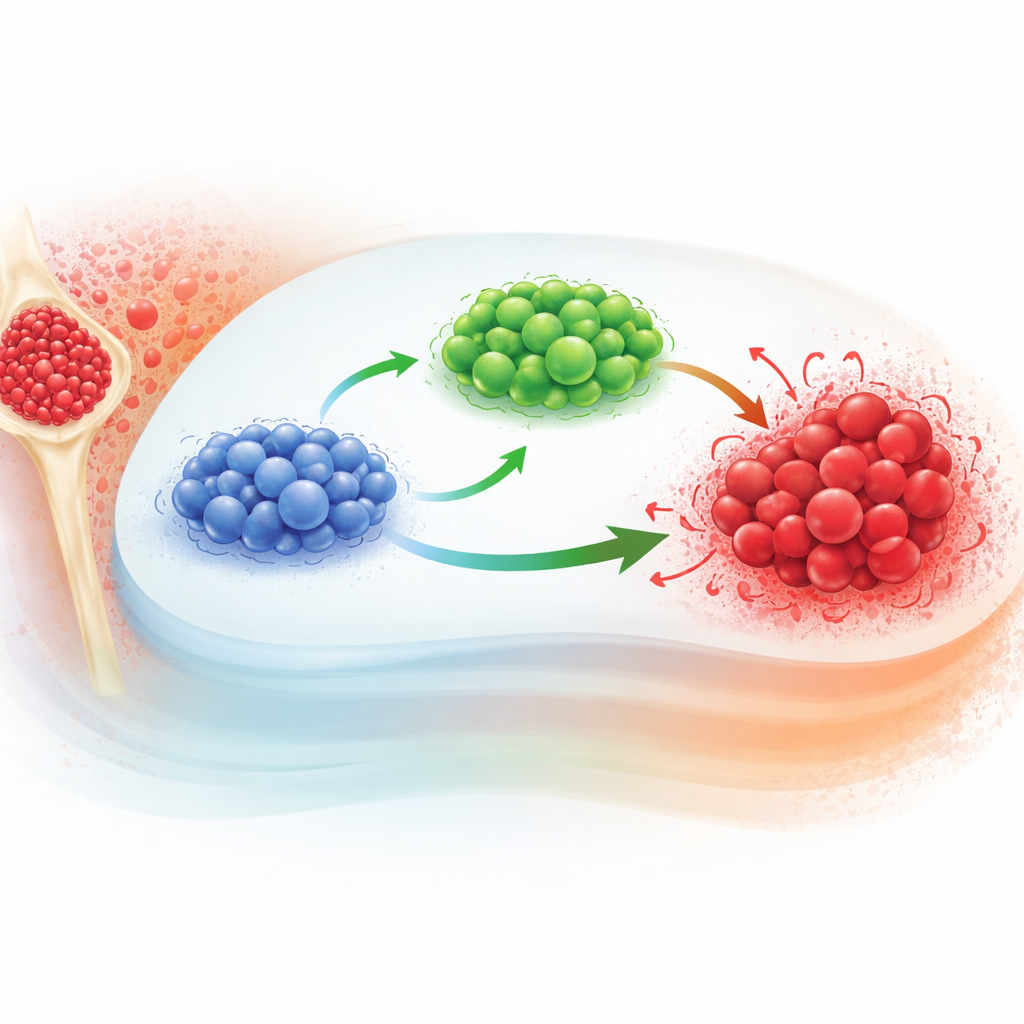
Comment les cellules cancéreuses et immunitaires interagissent
Les auteurs partent d’un modèle existant qui suit trois acteurs clés dans la LMC : les lymphocytes T naïfs, les lymphocytes T effecteurs et les cellules leucémiques. Les lymphocytes T naïfs sont les recrues inexpérimentées ; lorsqu’ils détectent des signaux leucémiques, certains se différencient en lymphocytes T effecteurs, les combattants de première ligne qui attaquent les cellules cancéreuses. Les cellules cancéreuses elles‑mêmes croissent selon une loi de saturation : elles se développent rapidement lorsqu’elles sont peu nombreuses, puis ralentissent à mesure qu’elles atteignent une taille maximale imposée par l’environnement. Les versions classiques de ce modèle utilisent des équations différentielles ordinaires, qui supposent que l’évolution future dépend uniquement de l’état actuel, et non du chemin parcouru pour y arriver.
Ajouter de la mémoire et de la rugosité au modèle
La biologie réelle n’est ni sans mémoire ni lisse. Les réponses immunitaires dépendent d’événements passés, et les tumeurs croissent de manière irrégulière, en motifs hétérogènes plutôt qu’en sphères parfaites. Pour capturer ces deux effets simultanément, les auteurs reconstruisent le modèle de la LMC en utilisant ce qu’ils appellent des opérateurs fractale–fractionnaires. Une composante, contrôlée par un paramètre appelé ordre fractionnaire, encode la mémoire : l’avenir du système dépend d’un historique pondéré de son passé. L’autre composante, contrôlée par une dimension fractale, traduit le caractère irrégulier ou « rugueux » de l’environnement tumoral. Lorsque ces deux paramètres valent un, le modèle se comporte comme la version classique ; lorsqu’ils diminuent, l’histoire et la complexité géométrique deviennent plus prépondérantes.
Garantir un comportement cohérent des nouvelles équations
Avant d’accorder sa confiance à un tel modèle, il faut montrer que ses solutions ont un sens biologique. Les auteurs démontrent que, sous des conditions raisonnables, leurs équations admettent une unique solution qui reste positive et bornée dans le temps — les effectifs cellulaires ne deviennent jamais négatifs ni infinis. Ils analysent ensuite les états d’équilibre du système. Dans ce cadre, un état complètement exempt de tumeur est mathématiquement instable : toute petite introduction de cellules leucémiques tend à croître. Le système est plutôt attiré vers un équilibre « présence de tumeur » où cancer et cellules immunitaires coexistent. À l’aide d’outils de théorie de la stabilité, ils montrent que cet état de coexistence n’est pas seulement localement stable mais globalement attractif : toutes les conditions initiales réalistes évoluent vers lui.
Méthodes numériques rapides pour une maladie lente
Parce que les nouvelles équations intègrent des effets de mémoire et fractals, elles sont plus difficiles à résoudre numériquement que les équations classiques. Les auteurs développent une technique numérique fondée sur les ondelettes de Laguerre, une famille de fonctions de base qui permet d’approximer efficacement le comportement sur de longues périodes. Cette méthode transforme le problème initial en un système réduit d’équations algébriques qui se résout rapidement et avec précision. Comparée aux schémas de pas de temps classiques, la méthode par ondelettes atteint la même précision avec beaucoup moins de calculs, ce qui est important pour exécuter de nombreuses simulations ou ajuster le modèle sur des données de patients.
Ce que révèlent les simulations sur le contrôle de la maladie
Avec ces outils, les auteurs étudient comment la variation des paramètres de mémoire et fractale influence l’évolution de la maladie. Abaisser l’ordre fractionnaire (mémoire plus forte) ou réduire la dimension fractale (géométrie tumorale plus irrégulière) favorise tous deux une décroissance plus rapide de la population leucémique et un niveau d’équilibre à long terme plus faible. Autrement dit, un système qui « se souvient » et une tumeur qui croît dans un environnement plus complexe sont plus faciles à contenir par le système immunitaire. Une analyse de sensibilité montre que deux quantités biologiques dominent la taille tumorale finale : le taux de croissance propre de la tumeur et le taux auquel les lymphocytes T effecteurs tuent les cellules cancéreuses. Cela correspond aux stratégies thérapeutiques actuelles qui combinent des médicaments ciblés pour ralentir la croissance tumorale et des immunothérapies pour renforcer la cytotoxicité immunitaire.
Ce que cela signifie pour les patients et les travaux futurs
En termes simples, l’étude conclut que la LMC a peu de chances de disparaître spontanément ; la tendance naturelle du système est de s’établir dans un équilibre où cancer et cellules immunitaires coexistent. Cependant, en construisant un modèle qui inclut mémoire et complexité structurelle, les auteurs décrivent des scénarios où cet équilibre est plus favorable au patient, avec une charge tumorale à long terme plus faible. Leur cadre fractale–fractionnaire, associé à des méthodes numériques efficaces, prépare le terrain pour de futurs « expériences numériques » sur le timing et les combinaisons de traitements. Avec des données cliniques, la même approche pourrait être personnalisée en ajustant les paramètres de mémoire et de géométrie pour chaque patient afin de prévoir les trajectoires de la maladie et optimiser la thérapie.
Citation: Khirsariya, S.R., Noori, N. Fractal-fractional modeling of chronic myelogenous leukemia immune dynamics using Laguerre wavelets method. Sci Rep 16, 14106 (2026). https://doi.org/10.1038/s41598-026-43767-3
Mots-clés: leucémie myéloïde chronique, dynamiques tumeur‑immunité, calcul fractionnaire, modélisation fractale des tumeurs, méthodes numériques par ondelettes