Clear Sky Science · nl
Fractal-fractiesmodelering van immuundynamiek bij chronische myeloïde leukemie met de Laguerre-golfletmethode
Waarom dit van belang is voor bloedkanker en het immuunsysteem
Chronische myeloïde leukemie (CML) is een bloedkanker die zich over jaren ontvouwt, terwijl het immuunsysteem voortdurend probeert deze onder controle te houden. Artsen beschikken tegenwoordig over krachtige geneesmiddelen, maar voorspellen hoe de kanker en immuuncellen van een patiënt in de loop van de tijd op elkaar reageren blijft lastig. Dit artikel introduceert een nieuw wiskundig model dat tumor- en immuunrespons als een gekoppeld dynamisch systeem met "geheugen" en complexe structuur beschouwt. Het doel is om realistischer hulpmiddelen te bouwen die uiteindelijk kunnen helpen bij het ontwerpen van betere therapieën en langetermijnbehandelplannen.
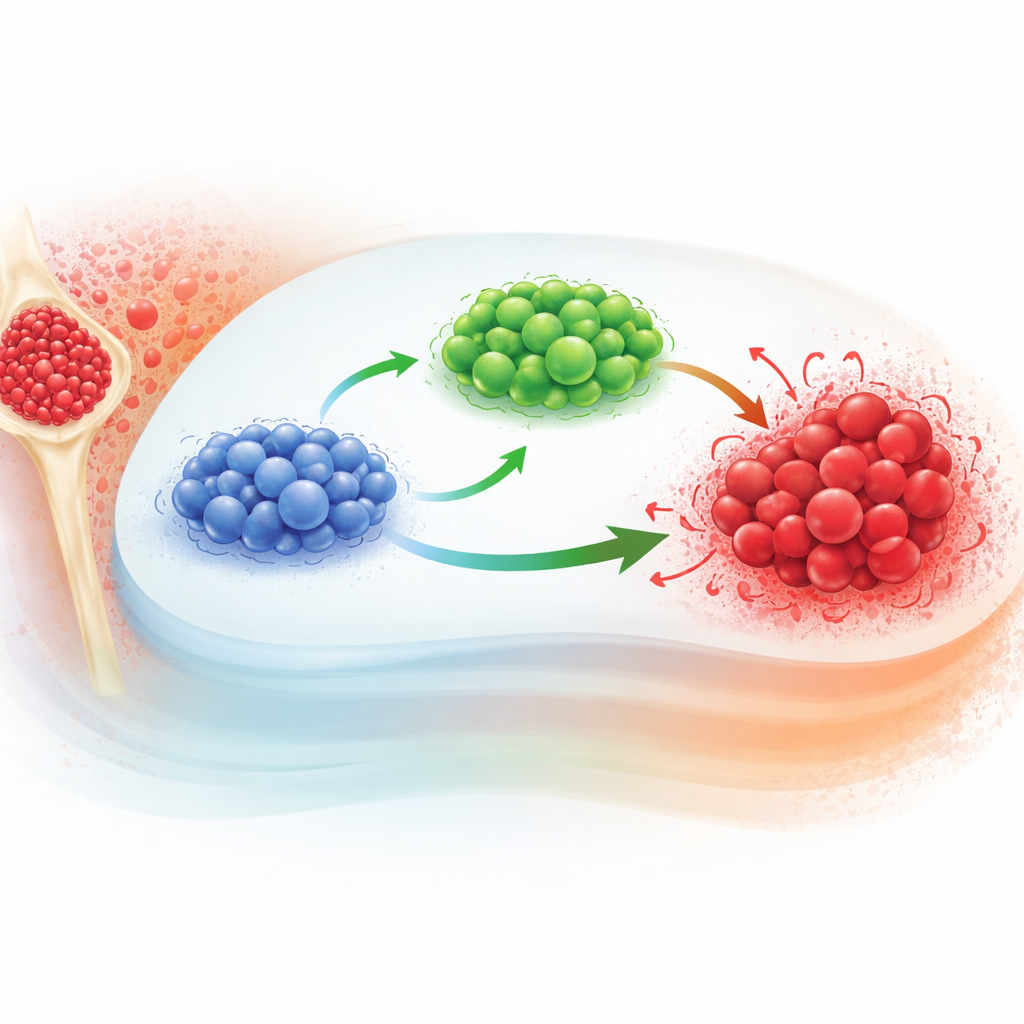
Hoe de kankercellen en immuuncellen met elkaar omgaan
De auteurs vertrekken van een bestaand model dat drie hoofdrolspelers in CML volgt: naïeve T-cellen, effector-T-cellen en leukemiecellen. Naïeve T-cellen zijn de onervaren rekruten; wanneer ze leukemiesignalen tegenkomen, veranderen sommige in effector-T-cellen, de frontlinie die kankercellen aanvalt. De kankercellen zelf groeien volgens een verzadigingswet: ze breiden zich snel uit wanneer ze klein zijn en vertragen naarmate ze een maximale grootte benaderen die door de omgeving wordt bepaald. Standaardversies van dit model gebruiken gewone differentiaalvergelijkingen, die veronderstellen dat wat er vervolgens gebeurt alleen afhangt van de huidige toestand, niet van hoe het systeem daar is gekomen.
Geheugen en ruwe structuur toevoegen aan het model
Werkelijke biologie is niet geheugenloos of glad. Immuunresponsen hangen af van eerdere ontmoetingen, en tumoren groeien in onregelmatige, vlekkerige patronen in plaats van nette bollen. Om beide effecten tegelijk vast te leggen bouwen de auteurs het CML-model opnieuw op met zogenaamde fractaal–fractionele operatoren. Eén onderdeel, geregeld door een parameter die de fractionele orde heet, codeert geheugen: de toekomst van het systeem hangt af van een gewogen geschiedenis van het verleden. Het andere onderdeel, geregeld door een fractale dimensie, vangt hoe onregelmatig of "ruw" de tumoromgeving is. Wanneer beide parameters op één worden gezet, gedraagt het model zich als de klassieke versie; wanneer ze worden verlaagd, worden geschiedenis en geometrische complexiteit belangrijker.
Zorgen dat de nieuwe vergelijkingen zich verstandig gedragen
Voordat men een dergelijk model kan vertrouwen, moet worden aangetoond dat de oplossingen biologisch zinvol zijn. De auteurs bewijzen dat, onder redelijke voorwaarden, hun vergelijkingen een unieke oplossing hebben die positief en begrensd blijft in de tijd — celgetallen worden nooit negatief of schieten naar oneindig. Vervolgens analyseren ze de evenwichtsstanden van het systeem. In dit kader is een volledig tumorvrije toestand wiskundig onstabiel: elke kleine introductie van leukemiecellen zal groeien. In plaats daarvan wordt het systeem aangetrokken naar een "tumor-aanwezige" evenwichtstoestand waarin kankercellen en immuuncellen naast elkaar bestaan. Met instrumenten uit de stabiliteitstheorie laten ze zien dat deze coexistente toestand niet alleen lokaal stabiel is maar globaal aantrekkend: alle realistische begincondities evolueren ernaartoe.
Snelle numerieke methoden om een trage ziekte op te lossen
Omdat de nieuwe vergelijkingen geheugen- en fractaaleffecten bevatten, zijn ze op een computer lastiger op te lossen dan standaardvergelijkingen. De auteurs ontwikkelen een numerieke techniek gebaseerd op Laguerre-golflets, een familie bouwsteenfuncties die efficiënt gedrag over lange tijden kunnen benaderen. Deze methode zet het originele probleem om in een kleiner stelsel algebraïsche vergelijkingen dat snel en nauwkeurig kan worden opgelost. In vergelijking met meer gebruikelijke tijdstapmethoden bereikt de golfletmethode dezelfde nauwkeurigheid met veel minder berekeningen, wat belangrijk is voor het uitvoeren van vele simulaties of het fitten van het model aan patiëntgegevens.
Wat de simulaties onthullen over ziektecontrole
Met deze hulpmiddelen onderzoeken de auteurs hoe het veranderen van geheugen- en fractaalparameters de ziekte-uitkomsten beïnvloedt. Het verlagen van de fractionele orde (sterker geheugen) of het verlagen van de fractale dimensie (meer onregelmatige tumorgeometrie) doet beide de leukemiep opulatie sneller afnemen en zich op een lager langdurig niveau vestigen. Met andere woorden: een systeem dat zich zijn verleden "herinnert" en een tumor die in een meer ingewikkelde omgeving groeit, zijn gemakkelijker te onderdrukken door het immuunsysteem. Een gevoeligheidsanalyse toont aan dat twee biologische grootheden het uiteindelijke tumorniveau domineren: de eigen groeisnelheid van de kanker en de snelheid waarmee effector-T-cellen kankercellen doden. Dit sluit aan bij huidige therapiestrategieën die gerichte middelen gebruiken om kankergroei te vertragen in combinatie met immunotherapieën die immuun doding versterken.
Wat dit betekent voor patiënten en toekomstig werk
Simpel gezegd concluderen de onderzoekers dat CML onwaarschijnlijk vanzelf zal verdwijnen; de natuurlijke neiging van het systeem is zich te vestigen in een evenwicht waarbij kankercellen en immuuncellen naast elkaar bestaan. Door echter een model te bouwen dat geheugen en structurele complexiteit omvat, kunnen de auteurs scenario’s beschrijven waarin dat evenwicht in het voordeel van de patiënt uitvalt, met een lagere langdurige kankerlading. Hun fractaal–fractionele raamwerk, gekoppeld aan efficiënte numerieke methoden, legt de basis voor toekomstige "digitale experimenten" over timing en combinaties van behandelingen. Met klinische gegevens zou dezelfde benadering gepersonaliseerd kunnen worden, door de geheugen- en geometrieparameters af te stemmen op individuele patiënten om ziekteverlopen te voorspellen en therapie te optimaliseren.
Bronvermelding: Khirsariya, S.R., Noori, N. Fractal-fractional modeling of chronic myelogenous leukemia immune dynamics using Laguerre wavelets method. Sci Rep 16, 14106 (2026). https://doi.org/10.1038/s41598-026-43767-3
Trefwoorden: chronische myeloïde leukemie, tumor-immuundynamica, fractionele calculus, fractaal tumormodelleren, numerieke golfletmethoden