Clear Sky Science · ru
Инновационные модели слияния: повышение точности предоперационного прогнозирования грубого экстращитовидного распространения у пациентов с раком щитовидной железы
Почему это исследование важно для пациентов
Для многих людей с раком щитовидной железы ключевой вопрос перед операцией — насколько далеко опухоль распространилась за пределы самой железы. Это распространение, называемое грубым экстращитовидным распространением, часто определяет, нужна ли пациенту небольшая целенаправленная операция или более обширное вмешательство, которое может повлиять на голос, глотание и качество жизни в долгосрочной перспективе. Исследование, описанное в этой статье, изучает, может ли продвинутый компьютерный анализ рутинных ультразвуковых сканов точнее предсказывать такое распространение, помогая хирургам более точно подбирать лечение и снижать как риски, так и ненужные операции.
Смотреть дальше, чем видит глаз
Традиционно радиологи на УЗИ оценивают распространение опухоли, визуально определяя, насколько узел сдавливает или деформирует окружающие ткани. Такой подход субъективен и пропускает многие агрессивные опухоли. Авторы предлагают использовать вычислительные методы для измерения тонких закономерностей в и вокруг опухоли, которые человеческий глаз не может надежно заметить. Они сосредоточились как на самой опухоли, так и на узкой окружной полосе ткани, полагая, что эта «пограничная зона» содержит ранние признаки того, проникают ли раковые клетки через капсулу щитовидной железы и инфильтрируют соседние мышцы или органы.
Преобразование УЗ-изображений в измеряемые данные
Команда собрала ультразвуковые снимки и клиническую информацию у 4 542 пациентов с папиллярным раком щитовидной железы, лечившихся в нескольких больницах в течение пяти лет. После тщательной разметки опухолей они использовали программное обеспечение для создания тонких концентрических колец ткани вокруг каждого узла, имитируя расстояния от края опухоли. Из этих областей извлекли сотни числовых характеристик изображения, описывающих размер, яркость и текстуру. Параллельно применяли глубокое обучение — нейронные сети, первоначально обученные на естественных изображениях — чтобы автоматически обнаруживать сложные паттерны, связанные с поведением опухоли. Систематически варьируя, насколько далеко простирались эти перифокальные кольца, исследователи могли проверить, сколько информации действительно добавляет окружающая ткань.
Слияние человеко‑разработанных признаков и глубокого обучения
Вместо опоры на один метод исследователи создали «модель слияния», которая комбинировала два типа информации: ручные радиомические признаки и признаки глубокого обучения. Они обнаружили, что включение умеренной полосы ткани вокруг опухоли — примерно соответствующей расширению на 15 пикселей на УЗ-изображении — последовательно улучшало способность отличать опухоли, прорвавшие капсулу щитовидной железы. Лучшая модель глубокого обучения сама по себе показала хорошие результаты, но при объединении ее признаков с радиомикой из опухоли и ближайшего окружения, а затем с ключевыми клиническими факторами, такими как размер опухоли и характер краев, точность прогноза ещё возрастала. Эта интегрированная модель достигла высокой точности и сильной способности правильно исключать случаи без опасного распространения, что важно для предотвращения чрезмерно агрессивных операций.
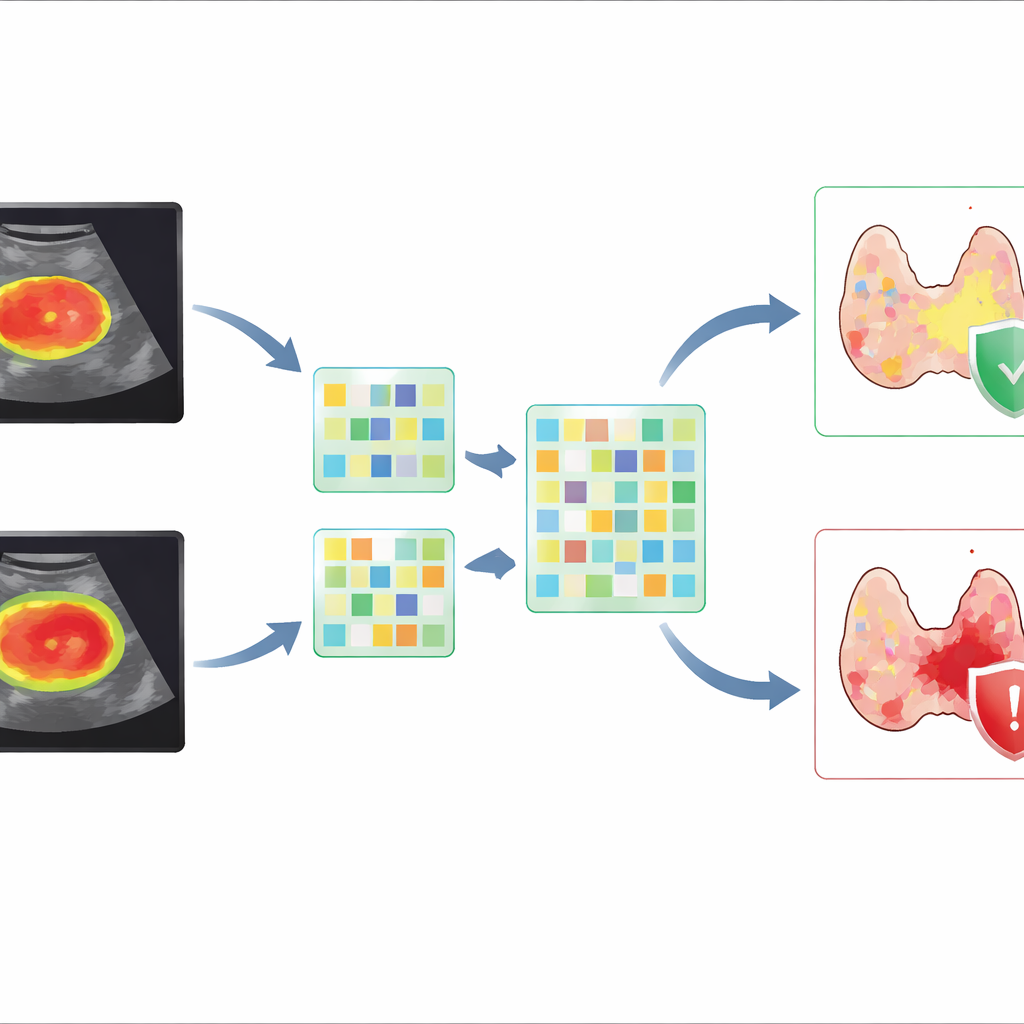
Объединение продвинутых моделей в один простой инструмент
Чтобы сделать эти сложные модели применимыми на практике, авторы создали визуальную шкалу оценки, известную как номограмма. Клиники могут использовать эту шкалу, находя на ней размер опухоли, характеристики краев и балл, полученный моделью по изображению, а затем суммируя очки для оценки вероятности грубого экстращитовидного распространения. Команда верифицировала этот инструмент на независимой группе пациентов из других центров и с других ультразвуковых аппаратов, показав, что его эффективность сохраняется в различных реальных условиях. Также применяли методы визуализации, чтобы выделить области изображения и признаки, которые влияли на предсказания модели, помогая врачам увидеть, что компьютер фокусируется на клинически значимых деталях по краю опухоли.
Что это может означать для будущих операций на щитовидной железе
Проще говоря, это исследование показывает, что тщательный анализ как самой опухоли, так и её ближайшего окружения на стандартных УЗ-изображениях может помочь предсказать, какие опухоли щитовидной железы, вероятно, вышли за пределы железы. Сочетая традиционные измерения изображения, мощное глубокое обучение и базовую клиническую информацию в одной простой в использовании шкале, авторы предлагают неинвазивный способ лучше планировать операции и стратифицировать риски. Хотя метод всё ещё пропускает некоторые глубоко инвазивные опухоли и требует дальнейшей проспективной проверки, он указывает на будущее, в котором рутинные сканы будут сочетаться с интеллектуальным программным обеспечением для более точной и индивидуализированной помощи пациентам с раком щитовидной железы.
Цитирование: Pan, T., Wu, F., Cai, J. et al. Innovative fusion models: elevating preoperative gross ETE prediction in thyroid cancer patients. Sci Rep 16, 13070 (2026). https://doi.org/10.1038/s41598-026-43230-3
Ключевые слова: рак щитовидной железы, ультразвуковая визуализация, глубокое обучение, радиомика, планирование хирургии