Clear Sky Science · fr
Modèles de fusion innovants : améliorer la prédiction préopératoire de l’ETE macroscopique chez les patients atteints de cancer de la thyroïde
Pourquoi cette recherche compte pour les patients
Pour de nombreuses personnes atteintes d’un cancer de la thyroïde, une question cruciale avant l’intervention est de savoir à quel point la tumeur s’est étendue au‑delà de la glande thyroïde. Cette extension, appelée extension extrathyroïdienne macroscopique, détermine souvent si la personne a besoin d’une intervention ciblée limitée ou d’une procédure plus étendue pouvant affecter la voix, la déglutition et la qualité de vie à long terme. L’étude présentée ici examine si des analyses informatiques avancées d’échographies de routine peuvent prédire avec plus de précision ce type d’extension, aidant les chirurgiens à adapter le traitement tout en réduisant les risques et les interventions inutiles.
Voir au‑delà de ce que l’œil perçoit
Traditionnellement, les radiologues estiment l’extension tumorale sur échographie en jugeant visuellement dans quelle mesure un nodule thyroïdien appuie sur ou déforme les tissus environnants. Cette approche est subjective et passe à côté de nombreuses tumeurs agressives. Les auteurs proposent d’utiliser l’informatique pour mesurer des motifs subtils dans et autour de la tumeur que l’œil humain ne détecte pas de façon fiable. Ils se concentrent à la fois sur la tumeur et sur la mince marge de tissu qui l’entoure, en raisonnant que cette « zone frontalière » porte des indices précoces quant à la capacité des cellules cancéreuses à franchir la capsule thyroïdienne et à infiltrer les muscles ou organes voisins.
Transformer les images échographiques en données mesurables
L’équipe a rassemblé des échographies et des données cliniques provenant de 4 542 patients atteints de carcinome papillaire de la thyroïde traités dans plusieurs hôpitaux sur cinq ans. Après avoir délimité avec soin les tumeurs, ils ont utilisé un logiciel pour créer de fines anneaux concentriques de tissu autour de chaque nodule, simulant différentes distances par rapport au bord tumoral. À partir de ces régions, ils ont extrait des centaines de caractéristiques numériques d’image décrivant la taille, la luminosité et la texture. En parallèle, ils ont utilisé l’apprentissage profond — des réseaux neuronaux initialement entraînés sur des images naturelles — pour découvrir automatiquement des motifs d’image complexes liés au comportement tumoral. En faisant varier systématiquement l’étendue de ces anneaux péritumoraux, ils ont pu tester combien d’informations le tissu environnant apportait réellement.
Fusionner caractéristiques humaines et apprentissage profond
Plutôt que de s’appuyer sur une seule méthode, les chercheurs ont créé des modèles de « fusion » combinant deux types d’informations : des caractéristiques radiomiques conçues par l’homme et des caractéristiques issues de l’apprentissage profond. Ils ont constaté qu’inclure une bande modeste de tissu autour de la tumeur — correspondant approximativement à une expansion de 15 pixels sur l’image échographique — améliorait systématiquement la capacité à distinguer les tumeurs ayant franchi la thyroïde. Le meilleur modèle d’apprentissage profond seul donnait déjà de bonnes performances, mais lorsque ses caractéristiques étaient fusionnées avec les radiomiques de la tumeur et de son environnement immédiat, puis complétées par des facteurs cliniques clés tels que la taille de la tumeur et l’aspect des bords, la prédiction s’améliorait encore. Ce modèle intégré a atteint une précision élevée et une forte capacité à exclure correctement les cas sans extension dangereuse, ce qui est crucial pour éviter des chirurgies excessivement agressives.
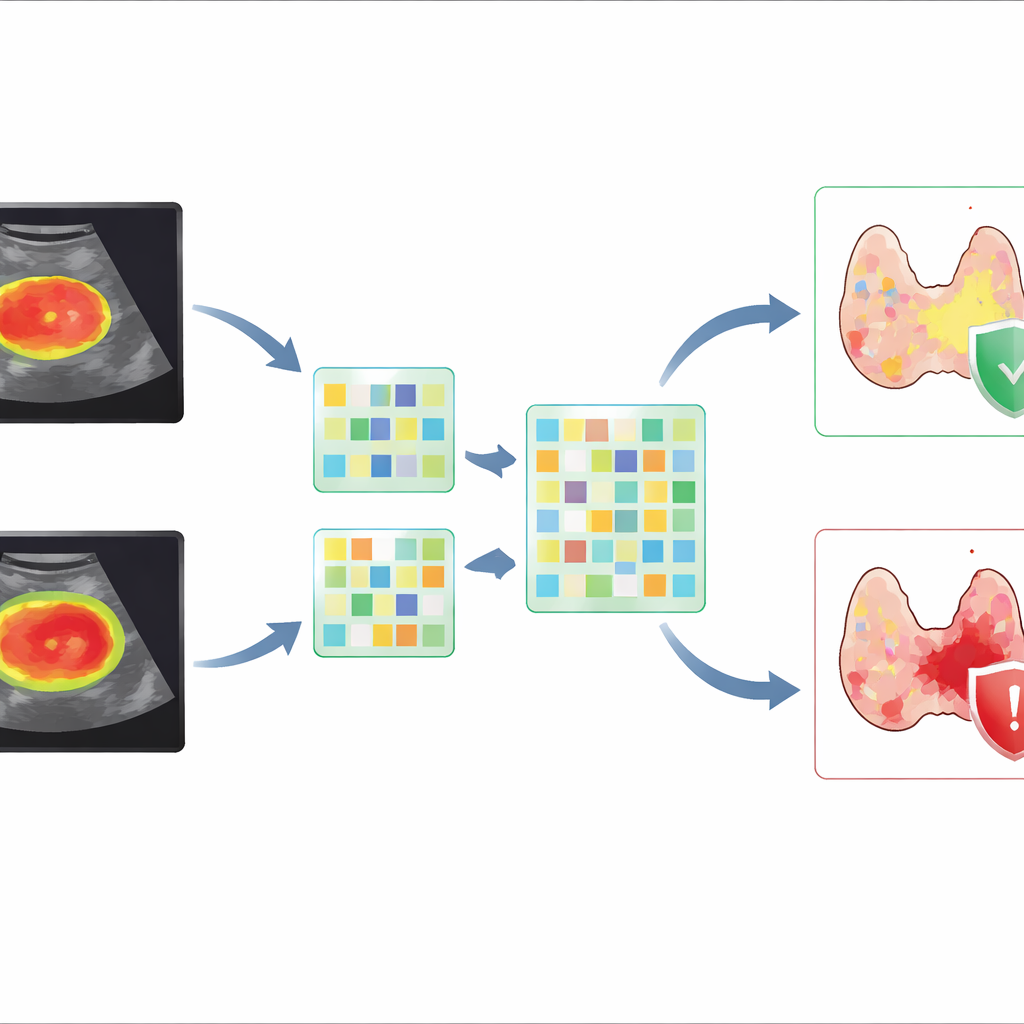
Rassembler des modèles avancés dans un outil simple
Pour rendre ces modèles complexes utilisables en pratique, les auteurs ont construit un tableau de score visuel connu sous le nom de nomogramme. Les cliniciens peuvent lire ce tableau en repérant la taille de la tumeur du patient, les caractéristiques des marges et le score d’image dérivé du modèle, puis en additionnant les points pour estimer la probabilité d’extension extrathyroïdienne macroscopique. L’équipe a validé cet outil sur un groupe indépendant de patients provenant de centres et d’appareils échographiques différents, montrant que ses performances tenaient dans des conditions réelles variées. Ils ont également utilisé des méthodes de visualisation pour mettre en évidence les régions d’image et les caractéristiques qui guidaient les prédictions du modèle, aidant les médecins à voir que l’algorithme se concentrait sur des détails cliniquement significatifs au niveau du bord tumoral.
Ce que cela pourrait signifier pour la chirurgie thyroïdienne à venir
En termes clairs, cette étude montre qu’une analyse soignée de la tumeur et de son environnement immédiat sur des images échographiques standard peut aider à prédire quelles tumeurs thyroïdiennes ont probablement dépassé la glande. En combinant mesures d’image traditionnelles, apprentissage profond performant et informations cliniques de base dans un seul tableau facile à utiliser, les auteurs proposent une méthode non invasive pour mieux planifier la chirurgie et stratifier les risques. Bien que la méthode manque encore certaines tumeurs très envahissantes et nécessite des tests prospectifs complémentaires, elle ouvre la voie à un avenir où les examens de routine seraient couplés à des logiciels intelligents pour orienter des soins thyroïdiens plus précis et individualisés.
Citation: Pan, T., Wu, F., Cai, J. et al. Innovative fusion models: elevating preoperative gross ETE prediction in thyroid cancer patients. Sci Rep 16, 13070 (2026). https://doi.org/10.1038/s41598-026-43230-3
Mots-clés: cancer de la thyroïde, imagerie échographique, apprentissage profond, radiomique, planification chirurgicale