Clear Sky Science · de
Innovative Fusionsmodelle: Verbesserung der präoperativen Vorhersage von makroskopischer ETE bei Schilddrüsenkrebspatienten
Warum diese Forschung für Patientinnen und Patienten wichtig ist
Für viele Menschen mit Schilddrüsenkrebs ist vor der Operation eine zentrale Frage, wie weit der Tumor über die Schilddrüse hinausgewachsen ist. Diese Ausbreitung, als makroskopische extrathyreoidale Extension bezeichnet, entscheidet häufig darüber, ob eine kleine, gezielte Operation ausreicht oder ein umfangreicherer Eingriff nötig ist, der Stimme, Schlucken und die langfristige Lebensqualität beeinträchtigen kann. Die vorliegende Studie untersucht, ob fortgeschrittene Computeranalysen routinemäßiger Ultraschalluntersuchungen diese Form der Ausbreitung genauer vorhersagen können, sodass Chirurgen die Behandlung besser anpassen und gleichzeitig Risiken sowie unnötige Operationen reduzieren können.
Über das hinausblicken, was das Auge erkennt
Traditionell schätzen Radiologinnen und Radiologen die Tumorausbreitung im Ultraschall visuell ein, indem sie beurteilen, wie sehr ein Schilddrüsenknoten an benachbartem Gewebe anliegt oder dieses verdrängt. Dieser Ansatz ist subjektiv und übersieht viele aggressive Tumoren. Die Autoren schlagen vor, Computer zu nutzen, um subtile Muster im und um den Tumor zu quantifizieren, die das menschliche Auge nicht zuverlässig erkennt. Sie konzentrieren sich sowohl auf den Tumor selbst als auch auf den schmalen Geweberand darum, mit der Überlegung, dass diese "Grenzzone" frühe Hinweise darauf enthält, ob Krebszellen die Schilddrüsenkapsel durchbrechen und in nahegelegene Muskeln oder Organe eindringen.
Ultraschallbilder in messbare Daten verwandeln
Das Team sammelte Ultraschalluntersuchungen und klinische Daten von 4.542 Patientinnen und Patienten mit papillärem Schilddrüsenkarzinom, die über fünf Jahre an mehreren Krankenhäusern behandelt wurden. Nach sorgfältiger Abgrenzung der Tumoren erzeugten sie mit Software dünne, konzentrische Ringe aus Gewebe um jeden Knoten, die Abstände vom Tumorrand nachahmen. Aus diesen Regionen extrahierten sie Hunderte numerischer Bildmerkmale, die Größe, Helligkeit und Textur beschreiben. Parallel dazu setzten sie Deep Learning ein — neuronale Netze, die ursprünglich an natürlichen Bildern trainiert wurden — um automatisch komplexe Bildmuster zu entdecken, die mit dem Tumorverhalten zusammenhängen. Durch systematisches Variieren der Ausdehnung dieser peritumoralen Ringe konnten sie testen, wie viel zusätzliche Information das umliegende Gewebe tatsächlich liefert.
Verschmelzung menschlich entworfener Merkmale mit Deep Learning
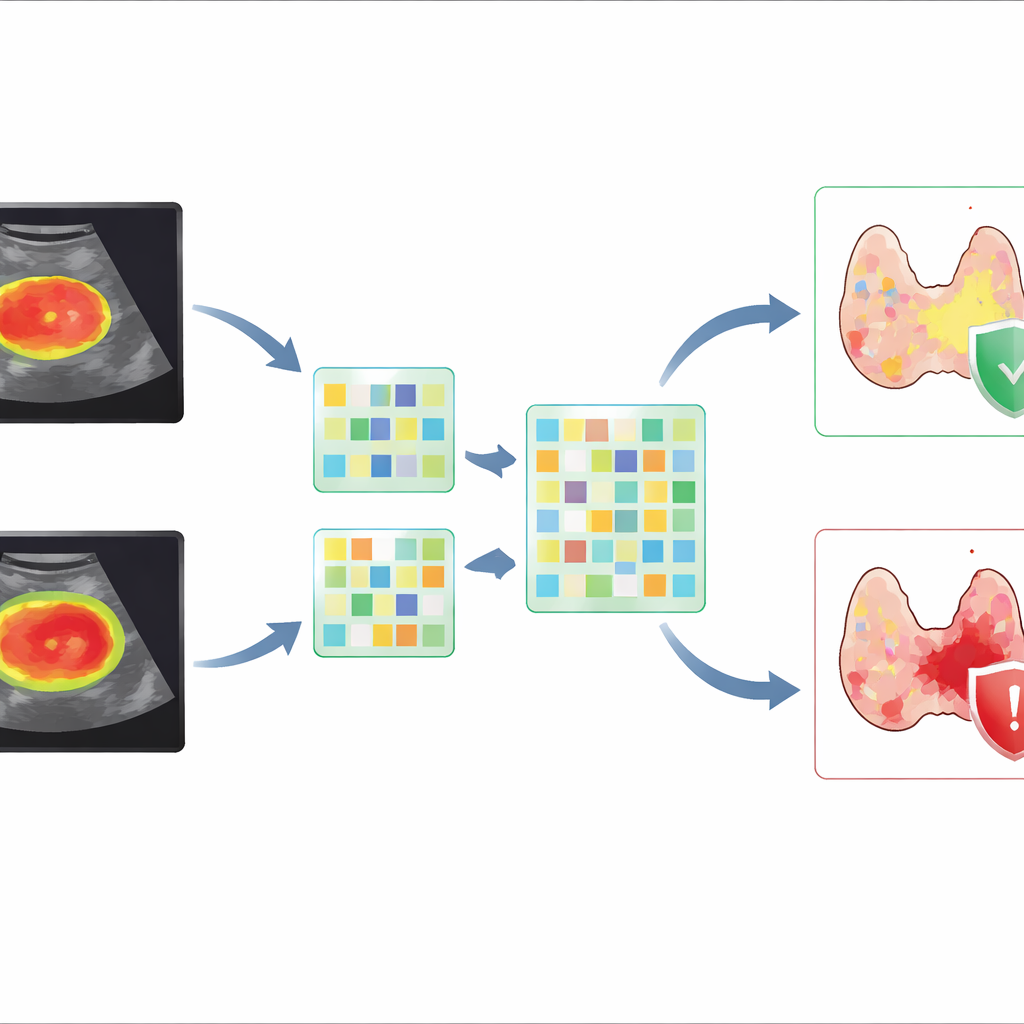
Statt sich auf eine einzige Methode zu verlassen, entwickelten die Forschenden "Fusions"-Modelle, die zwei Informationsarten kombinierten: manuell entwickelte Radiomics-Merkmale und Deep-Learning-Features. Sie stellten fest, dass die Einbeziehung eines moderaten Gewebebandes um den Tumor — ungefähr entsprechend einer Erweiterung um 15 Pixel im Ultraschallbild — beständig die Fähigkeit verbesserte, Tumoren zu unterscheiden, die aus der Schilddrüse herausgebrochen waren. Das beste Deep-Learning-Modell allein erzielte gute Ergebnisse, doch als seine Merkmale mit Radiomics aus dem Tumor und dessen unmittelbarer Umgebung verschmolzen und zusätzlich mit wichtigen klinischen Faktoren wie Tumorgröße und Randcharakteristik kombiniert wurden, verbesserte sich die Vorhersage weiter. Dieses integrierte Modell erreichte eine hohe Genauigkeit und eine starke Fähigkeit, Fälle ohne gefährliche Ausbreitung korrekt auszuschließen, was entscheidend ist, um übermäßig aggressive Operationen zu vermeiden.
Fortgeschrittene Modelle in einem einfachen Werkzeug bündeln
Um diese komplexen Modelle in der Praxis nutzbar zu machen, erstellten die Autoren ein visuelles Bewertungsschema in Form eines Nomogramms. Klinikerinnen und Kliniker können dieses Schema nutzen, indem sie die Tumorgröße, Randmerkmale und den modellbasierten Bildscore eines Patienten ablesen und die Punkte summieren, um die Wahrscheinlichkeit einer makroskopischen extrathyreoidalen Extension abzuschätzen. Das Team validierte dieses Werkzeug an einer unabhängigen Patientengruppe aus anderen Zentren und mit unterschiedlichen Ultraschallgeräten und zeigte, dass die Leistungsfähigkeit unter realen, heterogenen Bedingungen erhalten blieb. Außerdem nutzten sie Visualisierungsmethoden, um hervorzuheben, welche Bildregionen und Merkmale die Vorhersagen des Modells beeinflussten, sodass Ärztinnen und Ärzte sehen können, dass der Computer sich auf klinisch relevante Details am Tumorrand konzentriert.
Was das für die Zukunft der Schilddrüsenchirurgie bedeuten könnte
Kurz gesagt zeigt diese Studie, dass die sorgfältige Analyse sowohl des Tumors als auch seines unmittelbaren Umfelds auf standardmäßigen Ultraschallbildern helfen kann vorherzusagen, welche Schilddrüsentumoren wahrscheinlich über die Drüse hinausgewachsen sind. Durch die Verbindung traditioneller Bildmessungen, leistungsfähigem Deep Learning und grundlegenden klinischen Informationen in einem einfachen, leicht anwendbaren Schema bieten die Autoren einen nichtinvasiven Weg, um Operationen besser zu planen und Risiken zu stratifizieren. Zwar werden noch einige tief eindringende Tumoren übersehen und es bedarf weiterer prospektiver Prüfungen, doch die Arbeit weist in eine Zukunft, in der Routine-Scans mit intelligenter Software gekoppelt werden, um eine präzisere, individualisierte Versorgung von Patientinnen und Patienten mit Schilddrüsenkrebs zu ermöglichen.
Zitation: Pan, T., Wu, F., Cai, J. et al. Innovative fusion models: elevating preoperative gross ETE prediction in thyroid cancer patients. Sci Rep 16, 13070 (2026). https://doi.org/10.1038/s41598-026-43230-3
Schlüsselwörter: Schilddrüsenkrebs, Ultraschallbildgebung, Tiefes Lernen, Radiomics, chirurgische Planung