Clear Sky Science · nl
Innovatieve fusie‑modellen: betere voorspelling van preoperatieve grootschalige ETE bij schildklierkankerpatiënten
Waarom dit onderzoek belangrijk is voor patiënten
Voor veel mensen met schildklierkanker is een centrale vraag vóór de operatie hoe ver de tumor zich buiten de schildklier heeft verspreid. Deze verspreiding, aangeduid als grootschalige extrathyroïdale uitbreiding (ETE), bepaalt vaak of iemand een kleine, gerichte ingreep nodig heeft of een meer ingrijpende procedure die invloed kan hebben op stem, slikken en de levenslange kwaliteit van leven. De studie in dit artikel onderzoekt of geavanceerde computeranalyse van routinematige echoscans deze vorm van uitbreiding nauwkeuriger kan voorspellen, zodat chirurgen de behandeling kunnen afstemmen en zowel risico als onnodige operaties kunnen verminderen.
Kijken voorbij wat het oog kan zien
Traditioneel schatten radiologen tumoruitbreiding op echo visueel door te beoordelen hoe sterk een schildklierknobbel omliggend weefsel indrukt of vervormt. Deze aanpak is subjectief en mist veel agressieve tumoren. De auteurs stellen voor computers te gebruiken om subtiele patronen in en rond de tumor te meten die het menselijk oog niet betrouwbaar kan waarnemen. Ze concentreren zich zowel op de tumor zelf als op de smalle rand van weefsel daaromheen, met de redenering dat deze “grenszone” vroege aanwijzingen bevat of kankercellen door de schildklierkapsel breken en naburige spieren of organen binnendringen.
Echobeelden omzetten in meetbare data
Het team verzamelde echoscans en klinische gegevens van 4.542 patiënten met papillaire schildkliercarcinoom die over vijf jaar in meerdere ziekenhuizen werden behandeld. Nadat de tumoren zorgvuldig waren afgebakend, gebruikten ze software om dunne, concentrische ringen van weefsel rond elke knobbel te creëren, die afstanden vanaf de tumorrand nabootsen. Uit deze regio’s haalden ze honderden numerieke beeldkenmerken die grootte, helderheid en textuur beschrijven. Parallel daaraan gebruikten ze deep learning—neurale netwerken oorspronkelijk getraind op natuurlijke afbeeldingen—om automatisch complexe beeldpatronen te ontdekken die gerelateerd zijn aan tumorgedrag. Door systematisch te variëren hoe ver deze peritumorale ringen zich uitstrekten, konden ze testen hoeveel informatie het omliggende weefsel werkelijk toevoegde.
Het samenbrengen van door mensen ontworpen kenmerken met deep learning
In plaats van te vertrouwen op één methode ontwikkelden de onderzoekers “fusie”-modellen die twee soorten informatie combineerden: door mensen gemaakte radiomics‑kenmerken en deep learning‑kenmerken. Ze ontdekten dat het opnemen van een bescheiden band weefsel rond de tumor—ongeveer overeenkomend met een uitbreiding van 15 pixels in de echobeelden—consistente verbetering gaf in het onderscheidingsvermogen tussen tumoren die uit de schildklier waren doorgebroken. Het beste deep learning‑model op zichzelf presteerde goed, maar wanneer zijn kenmerken werden gefuseerd met radiomics van de tumor plus diens onmiddellijke omgeving en vervolgens gecombineerd met belangrijke klinische factoren zoals tumorgrootte en randkenmerken, verbeterde de voorspelling nog verder. Dit geïntegreerde model behaalde een hoge nauwkeurigheid en een sterke capaciteit om gevallen zonder gevaarlijke uitbreiding correct uit te sluiten, wat cruciaal is om te voorkomen dat er te agressief wordt geopereerd.
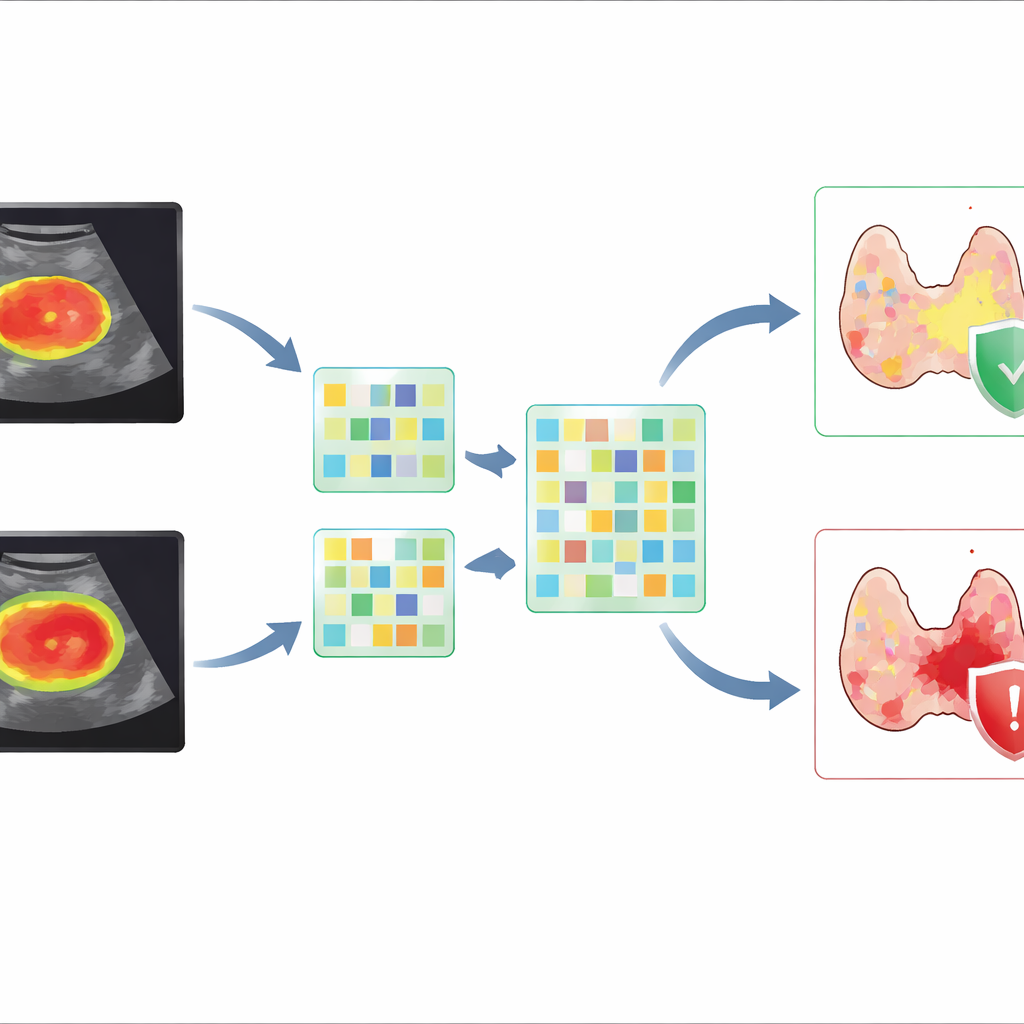
Geavanceerde modellen samenbrengen in één eenvoudig hulpmiddel
Om deze complexe modellen bruikbaar te maken in de praktijk, bouwden de auteurs een visuele scorekaart die bekendstaat als een nomogram. Klinici kunnen deze kaart gebruiken door de tumorgrootte van een patiënt, randkenmerken en de door het model afgeleide beeldscore op te zoeken en vervolgens de punten op te tellen om de kans op grootschalige extrathyroïdale uitbreiding te schatten. Het team valideerde dit hulpmiddel op een onafhankelijke groep patiënten uit andere centra en met andere echoapparatuur, en toonde aan dat de prestaties behouden bleven onder uiteenlopende real‑world omstandigheden. Ze gebruikten ook visualisatiemethoden om te benadrukken welke beeldregio’s en kenmerken de voorspellingen van het model aandreven, zodat artsen konden zien dat de computer zich concentreerde op klinisch betekenisvolle details aan de rand van de tumor.
Wat dit kan betekenen voor toekomstige schildklierchirurgie
Simpel gezegd toont deze studie aan dat het zorgvuldig analyseren van zowel de tumor als diens onmiddellijke omgeving op standaard echobeelden kan helpen voorspellen welke schildkliertumoren waarschijnlijk buiten de klier zijn gedrongen. Door traditionele beeldmetingen, krachtige deep learning en basis klinische informatie te combineren in één gemakkelijk te gebruiken kaart, bieden de auteurs een niet‑invasieve manier om operaties beter te plannen en risico’s te stratificeren. Hoewel de methode nog steeds sommige diep indringende tumoren mist en verdere prospectieve testen nodig heeft, wijst het op een toekomst waarin routinematige scans worden gekoppeld aan intelligente software om preciezere, geïndividualiseerde zorg voor patiënten met schildklierkanker te sturen.
Bronvermelding: Pan, T., Wu, F., Cai, J. et al. Innovative fusion models: elevating preoperative gross ETE prediction in thyroid cancer patients. Sci Rep 16, 13070 (2026). https://doi.org/10.1038/s41598-026-43230-3
Trefwoorden: schildklierkanker, echografische beeldvorming, deep learning, radiomics, chirurgische planning