Clear Sky Science · pl
Innowacyjne modele fuzji: podnoszenie dokładności przedoperacyjnego przewidywania widocznego ETE u pacjentów z rakiem tarczycy
Dlaczego te badania mają znaczenie dla pacjentów
Dla wielu osób z rakiem tarczycy kluczowym pytaniem przed operacją jest, jak daleko guz rozprzestrzenił się poza gruczoł tarczycy. To rozprzestrzenienie, zwane widocznym naciekaniem pozatarczycowym (gross extrathyroidal extension), często decyduje o tym, czy konieczny jest niewielki, celowany zabieg, czy też bardziej rozległa operacja, która może wpłynąć na głos, połykanie i długoterminową jakość życia. Badanie opisane w tym artykule analizuje, czy zaawansowana analiza komputerowa rutynowych badań ultrasonograficznych może dokładniej przewidywać tego rodzaju naciekanie, pomagając chirurgom dostosować leczenie przy jednoczesnym zmniejszeniu ryzyka i uniknięciu niepotrzebnych zabiegów.
Patrząc poza to, co widoczne gołym okiem
Tradycyjnie radiolodzy oceniają rozprzestrzenianie się guza w ultrasonografii, wizualnie oceniając, jak mocno węzeł tarczycowy uciska lub deformuje otaczające tkanki. To podejście jest subiektywne i pomija wiele agresywnych zmian. Autorzy proponują wykorzystanie komputerów do pomiaru subtelnych wzorców w obrębie guza i wokół niego, których oko ludzkie nie wykrywa niezawodnie. Skupiają się zarówno na samym guzie, jak i na wąskim pasie tkanki wokół niego, zakładając, że ta „strefa brzeżna” niesie wczesne wskazówki, czy komórki nowotworowe przenikają przez torebkę tarczycy i infiltrują pobliskie mięśnie lub narządy.
Przekształcanie obrazów ultrasonograficznych w dane mierzalne
Zespół zgromadził obrazy ultrasonograficzne i dane kliniczne od 4 542 pacjentów z rakiem pęcherzykowym tarczycy (papillary thyroid carcinoma) leczonych w wielu szpitalach w ciągu pięciu lat. Po dokładnym obrysowaniu guzów użyli oprogramowania do stworzenia cienkich, koncentrycznych pierścieni tkanki wokół każdego węzła, odwzorowując odległości od krawędzi guza. Z tych obszarów wydobyli setki numerycznych cech obrazowych opisujących rozmiar, jasność i teksturę. Równolegle zastosowali uczenie głębokie — sieci neuronowe pierwotnie trenowane na obrazach naturalnych — aby automatycznie odkrywać złożone wzorce obrazowe związane z zachowaniem guza. Systematycznie zmieniając, jak daleko rozciągały się pierścienie okołoguzowe, mogli sprawdzić, ile informacji dostarcza tkanka otaczająca guz.
Łączenie cech projektowanych przez człowieka z uczeniem głębokim
Zamiast polegać na jednej metodzie, badacze stworzyli modele „fuzji”, łączące dwa rodzaje informacji: ręcznie opracowane cechy radiomiki i cechy z uczenia głębokiego. Stwierdzili, że uwzględnienie umiarkowanego pasa tkanki wokół guza — odpowiadającego w przybliżeniu rozszerzeniu o 15 pikseli na obrazie ultrasonograficznym — konsekwentnie poprawiało zdolność rozróżniania guzów, które przebiły torebkę tarczycy. Najlepszy samodzielny model uczenia głębokiego działał dobrze, ale gdy jego cechy połączono z radiomiką guza i jego bezpośredniego otoczenia, a następnie zestawiono z kluczowymi czynnikami klinicznymi, takimi jak rozmiar guza i wygląd marginesu, przewidywanie uległo dalszej poprawie. Ten zintegrowany model osiągnął wysoką dokładność i dużą zdolność do prawidłowego wykluczania przypadków bez niebezpiecznego naciekania, co jest kluczowe dla unikania nadmiernie agresywnej chirurgii.
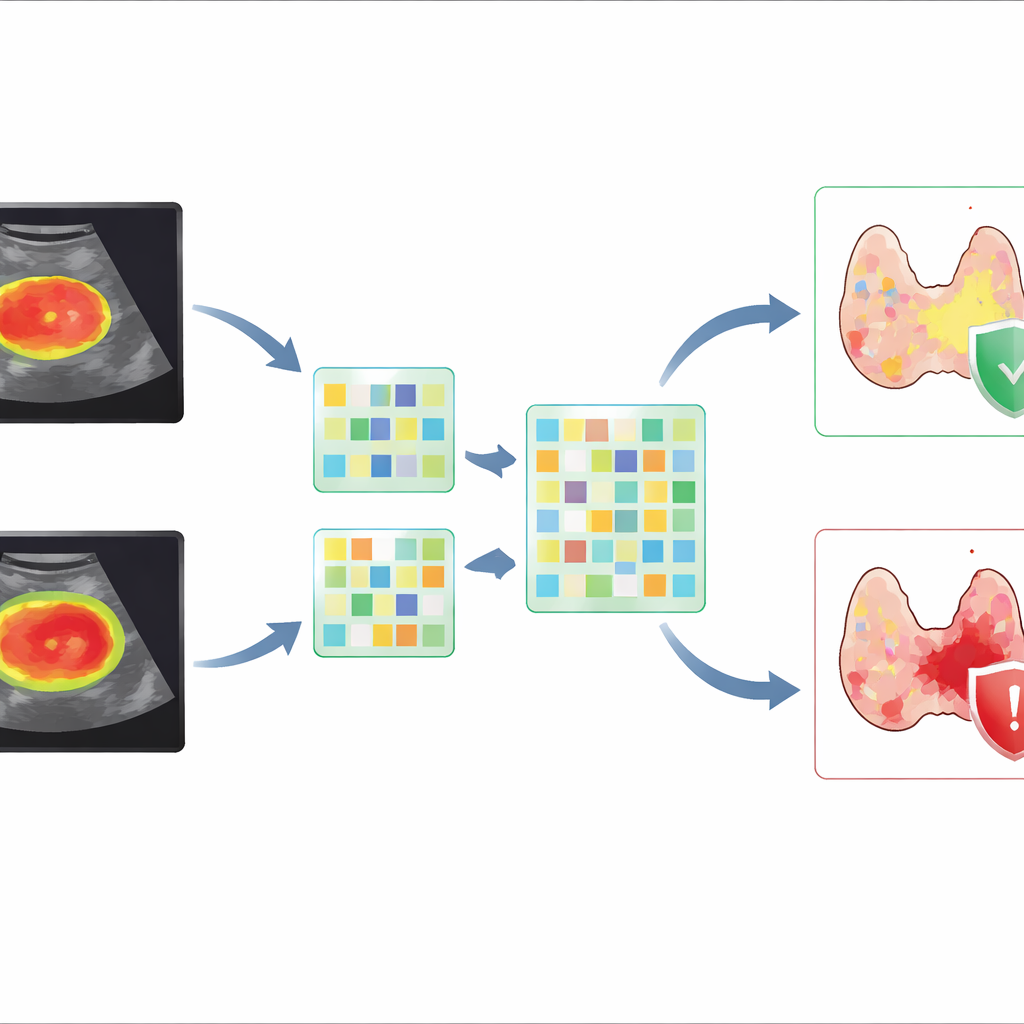
Zamknięcie zaawansowanych modeli w jednym prostym narzędziu
Aby uczynić te złożone modele użytecznymi w praktyce, autorzy opracowali wizualny wykres punktowy znany jako nomogram. Klinicyści mogą odczytać ten wykres, lokalizując rozmiar guza u pacjenta, cechy marginesu i wynik obrazowy wygenerowany przez model, a następnie zsumować punkty, aby oszacować prawdopodobieństwo widocznego naciekania pozatarczycowego. Zespół zwalidował to narzędzie na niezależnej grupie pacjentów z różnych ośrodków i przy użyciu różnych aparatów ultrasonograficznych, wykazując, że jego wydajność utrzymuje się w zróżnicowanych warunkach rzeczywistych. Użyli także metod wizualizacji, by podkreślić, które regiony obrazu i cechy wpływały na przewidywania modelu, pomagając lekarzom zobaczyć, że komputer skupia się na klinicznie istotnych detalach na krawędzi guza.
Co to może oznaczać dla przyszłej chirurgii tarczycy
Mówiąc prosto, badanie pokazuje, że staranna analiza zarówno nowotworu, jak i jego bezpośredniego otoczenia na standardowych obrazach ultrasonograficznych może pomóc przewidzieć, które guzy tarczycy prawdopodobnie wydostały się poza gruczoł. Poprzez połączenie tradycyjnych pomiarów obrazowych, potężnego uczenia głębokiego i podstawowych informacji klinicznych w jeden, łatwy w użyciu wykres, autorzy oferują nieinwazyjny sposób lepszego planowania operacji i stratyfikacji ryzyka. Choć metoda nadal nie wykrywa wszystkich głęboko naciekających guzów i wymaga dalszych badań prospektywnych, wskazuje na przyszłość, w której rutynowe badania będą łączone z inteligentnym oprogramowaniem, by prowadzić bardziej precyzyjną, spersonalizowaną opiekę dla pacjentów z rakiem tarczycy.
Cytowanie: Pan, T., Wu, F., Cai, J. et al. Innovative fusion models: elevating preoperative gross ETE prediction in thyroid cancer patients. Sci Rep 16, 13070 (2026). https://doi.org/10.1038/s41598-026-43230-3
Słowa kluczowe: rak tarczycy, obrazowanie ultrasonograficzne, uczenie głębokie, radiomika, planowanie chirurgiczne