Clear Sky Science · ru
Масс-спектрометрическое изображение MALDI-TOF экспрессии сульфатидных липидов в ЦНС мышей с экспериментальным аутоиммунным энцефаломиелитом
Почему это важно для здоровья мозга
Рассеянный склероз (РС) — заболевание, при котором собственная иммунная система организма атакует изоляцию вокруг нервных волокон в мозге и спинном мозге. Эта изоляция, называемая миелином, необычно богата жирами, известными как липиды. В этом исследовании задают на первый взгляд простой, но значимый вопрос: выявляются ли тонкие изменения в этих миелиновых липидах раньше, чем появляются явные симптомы и видимые повреждения? С помощью специализированной версии масс-спектрометрии для «картирования» липидов непосредственно в тканях мозга мышей исследователи показывают, что конкретные миелиновые жиры меняются рано и широко при экспериментальном РС, что указывает на новые пути для обнаружения и, возможно, лечения болезни.
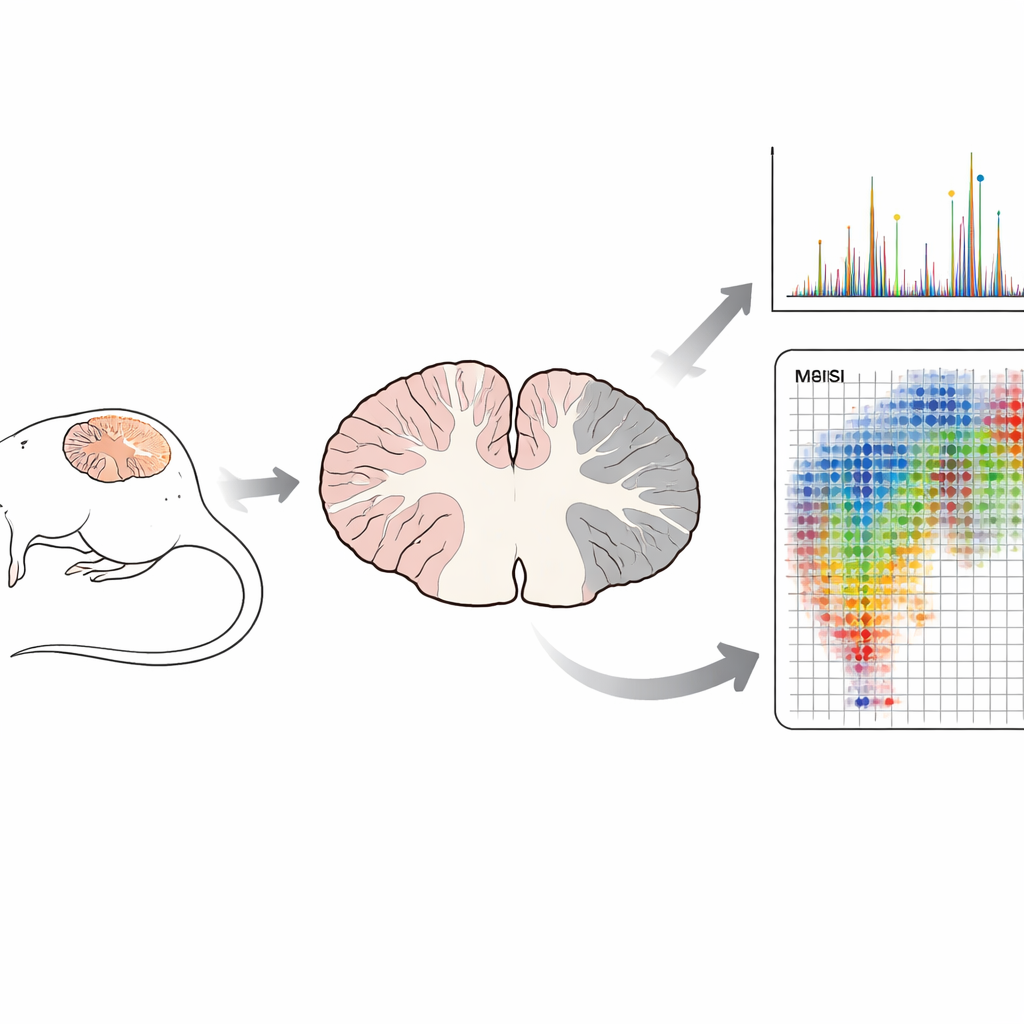
Ближе к жировой броне миелина
Миелин — это многослойная оболочка, окружающая многие нервные волокна, необходимая для быстрой электрической проводимости и долгосрочного здоровья нервов. В отличие от большинства тканей, миелин доминируется липидами, а не белками. Среди его наиболее характерных компонентов — сульфатиды, семейство специализированных жиров, которые встречаются в миелине в особенно высоких концентрациях по сравнению с другими частями организма. Эти молекулы помогают организовать слои миелина, поддерживают клетки, синтезирующие миелин, и участвуют во взаимодействии между нервными волокнами и их глиальными клетками. Нарушения в синтезе или распаде сульфатидов связывают с несколькими расстройствами мозга, включая болезнь Альцгеймера и редкие наследственные миелиновые болезни, что делает их основным подозреваемым и при РС.
Наблюдение молекул на месте, а не в пробирке
Традиционные биохимические методы часто измельчают ткань до однородной смеси перед измерением её содержимого. Такой подход может показать, что присутствует, но уничтожает пространственный контекст расположения каждой молекулы. В этом исследовании команда использовала матрично-ассистированную лазерную десорбцию/ионизацию с временем пролёта масс (MALDI-TOF MSI) — технику, которая сканирует тонкие срезы мозга точка за точкой. В каждой точке лазер высвобождает молекулы, и прибор регистрирует их массы, создавая «молекулярные карты» сотен соединений одновременно. Важно, что это делается без меток или красителей и сохраняет тонкую структуру ткани, которую затем можно напрямую сопоставить со стандартными микроскопическими окрасками.
Как липиды миелина меняются при экспериментальном РС
Исследователи использовали хорошо зарекомендовавшую себя модель РС у мышей — экспериментальный аутоиммунный энцефаломиелит (EAE), которая воспроизводит воспаление, потерю миелина и повреждение нервов, сходные с наблюдаемыми у пациентов. Они изучали мозжечок, область мозга, где повреждения при EAE часто проявляются, на четырёх стадиях: здоровая, ранняя «предкурсорная» фаза без явных симптомов, начало болезни и пик паралича. Сфокусировавшись на наборе известных миелиновых сульфатидов, они сначала подтвердили, что у здоровых мышей эти липиды концентрируются в белом веществе — миелин-зависимых «магистралях» нервных волокон. С помощью фрагментационных схем масс-спектрометрии они отделили сульфатиды от других липидов с почти идентичными массами и подтвердили тождественность девяти из десяти целевых молекул.
Ранние и широко распространённые изменения до появления симптомов
Сравнение липидных карт на разных стадиях болезни выявило чёткую закономерность. Несколько видов сульфатидов увеличивали свою концентрацию в белом веществе до появления каких-либо внешних признаков EAE, в то время как по крайней мере один важный сульфатид уменьшался. Анализ главных компонент — метод суммирования сложных данных в несколько ключевых паттернов — показал, что общий профиль сульфатидов существенно смещался, особенно вокруг начала болезни, а затем частично возвращался к прежнему образцу на пике болезни. Важно, что эти изменения не ограничивались локальными очагами воспаления, традиционно выделяемыми в патологии РС; напротив, они простирались по более широкой области белого вещества. Кроме того, нетаргетированный характер MSI выявил десятки других липидов в белом и сером веществе, распределение которых менялось с прогрессией болезни, что указывает на вовлечённость широкой сети липидного метаболизма.
Что это может означать для диагностики и лечения
Показав, что миелиновые сульфатиды и другие липиды меняют уровни и местоположение рано и широко в ходе экспериментального РС, эта работа выделяет липидные профили как потенциальную раннюю систему предупреждения о повреждении нервной изоляции. Возможность визуализировать эти молекулы на месте, а не после гомогенизации ткани, даёт более точное представление о том, как развивается нейровоспаление. В будущем такие молекулярные паттерны могут направлять разработку контрастных средств для клинической МРТ или указывать на новые лекарственные мишени, направленные на стабилизацию миелиновых липидов. Хотя требуется дальнейшая работа для переноса этих результатов от мышей к людям, исследование демонстрирует, что масс-спектрометрическое изображение может фиксировать «молекулярную снимку» поражённого мозга, которая может помочь прогнозировать, отслеживать и в конечном итоге изменять ход РС.
Цитирование: Berlin, K.A., Huizar, C.C., Garza, C. et al. MALDI-TOF mass spectrometry imaging of sulfatide lipid expression in the CNS of mice with experimental autoimmune encephalomyelitis. Sci Rep 16, 11462 (2026). https://doi.org/10.1038/s41598-026-41147-5
Ключевые слова: рассеянный склероз, миелиновые липиды, масс-спектрометрическое изображение, нейровоспаление, сульфатиды