Clear Sky Science · pl
Obrazowanie spektrometrii mas MALDI-TOF ekspresji lipidów sulfatydowych w OUN myszy z eksperymentalnym autoimmunologicznym zapaleniem mózgu
Dlaczego ma to znaczenie dla zdrowia mózgu
Stwardnienie rozsiane (SR) to choroba, w której własny układ odpornościowy organizmu atakuje izolację włókien nerwowych w mózgu i rdzeniu kręgowym. Ta izolacja, zwana mieliną, jest wyjątkowo bogata w tłuszcze określane jako lipidy. Badanie stawia pozornie proste pytanie o dużych implikacjach: czy subtelne zmiany w tych lipidach mielinowych pojawiają się zanim wystąpią oczywiste objawy i widoczne uszkodzenia? Dzięki zastosowaniu specjalistycznej formy spektrometrii mas do „mapowania” lipidów bezpośrednio w tkance mózgowej myszy, badacze pokazują, że konkretne tłuszcze mielinowe zmieniają się wcześnie i szeroko w przebiegu doświadczalnego SR, co sugeruje nowe możliwości wykrywania, a może i leczenia choroby.
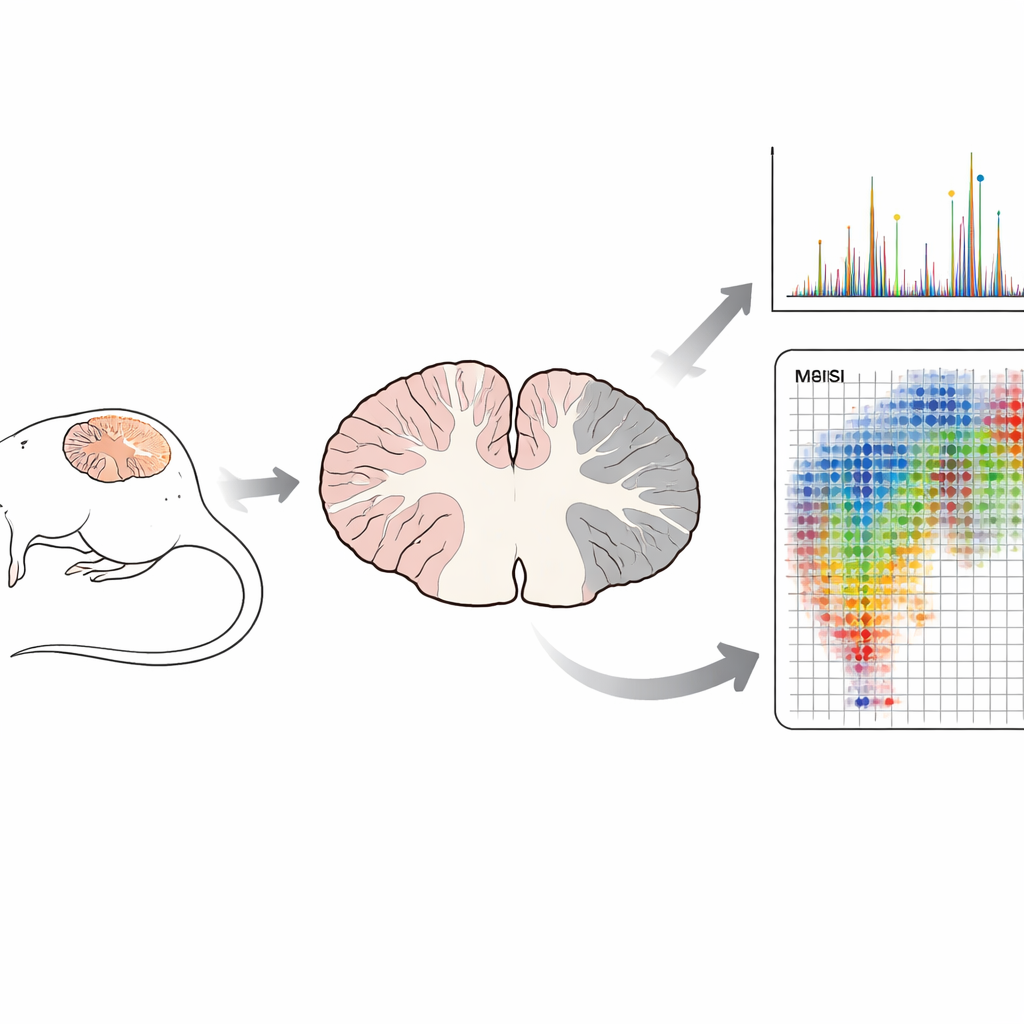
Bliższe spojrzenie na tłustą zbroję mieliny
Mielina to wielowarstwowe otoczenie otaczające wiele włókien nerwowych, niezbędne do szybkiego przewodzenia impulsów elektrycznych i długoterminowego zdrowia neuronów. W przeciwieństwie do większości tkanek, mielina jest zdominowana przez lipidy, a nie białka. Do jej najbardziej charakterystycznych składników należą sulfatydy — rodzina wyspecjalizowanych tłuszczów występujących w mielinie w znacznie wyższych stężeniach niż w innych częściach ciała. Molekuły te pomagają organizować warstwy mieliny, wspierać komórki wytwarzające mielinę oraz uczestniczyć w komunikacji między włóknami nerwowymi a komórkami glejowymi. Zaburzenia w wytwarzaniu lub rozkładzie sulfatydów powiązano z kilkoma chorobami mózgu, w tym z chorobą Alzheimera oraz rzadkimi dziedzicznymi chorobami mieliny, co czyni je głównym podejrzanym także w SR.
Widzieć cząsteczki na miejscu, a nie w probówce
Tradycyjne metody biochemiczne często rozdrabniają tkankę do jednorodnej mieszaniny przed zmierzeniem jej składu. Takie podejście może ujawnić, co jest obecne, ale niszczy kontekst przestrzenny — gdzie każda cząsteczka występuje. W tym badaniu zespół zastosował obrazowanie spektrometrii mas z użyciem matrycy i laserowej desorpcji/jonizacji w czasie przelotu (MALDI-TOF MSI), technikę skanującą cienkie plastry mózgu punkt po punkcie. W każdym punkcie laser uwalnia molekuły, a instrument rejestruje ich masy, tworząc „mapy molekularne” setek związków jednocześnie. Co istotne, odbywa się to bez znaczników czy barwników i zachowuje drobną strukturę tkanki, którą później można bezpośrednio porównać z klasycznymi barwieniami mikroskopowymi.
Jak lipidy mielinowe zmieniają się podczas doświadczalnego SR
Badacze odwołali się do dobrze opisanych modeli mysich SR, nazywanych eksperymentalnym autoimmunologicznym zapaleniem mózgu (EAE), które odzwierciedla zapalenie, utratę mieliny i uszkodzenie nerwów podobne do obserwowanego u pacjentów. Zbadali móżdżek, obszar mózgu, w którym uszkodzenia EAE często się pojawiają, na czterech etapach: zdrowie, wczesna faza „przed wystąpieniem” bez widocznych objawów, początek choroby oraz szczytowy poziom paraliżu. Skupiając się na zestawie znanych sulfatydów mielinowych, najpierw potwierdzili, że u zdrowych myszy lipidy te koncentrują się w szlakach istoty białej — mielinowych autostradach włókien nerwowych. Wykorzystując wzorce fragmentacji w spektrometrii mas, rozróżnili sulfatydy od innych lipidów o niemal identycznych masach i potwierdzili tożsamość dziewięciu z dziesięciu docelowych molekuł.
Wczesne i rozległe zmiany przed objawami
Porównanie map lipidowych między etapami choroby ujawniło wyraźny wzorzec. Kilka gatunków sulfatydów zwiększyło obfitość w istocie białej zanim pojawiły się jakiekolwiek zewnętrzne oznaki EAE, podczas gdy przynajmniej jeden istotny sulfatyd zmniejszył się. Analiza składowych głównych — sposób podsumowania złożonych danych w kilka kluczowych wzorców — pokazała, że ogólny profil sulfatydowy przesunął się wyraźnie, szczególnie w okolicach początku choroby, a następnie częściowo powrócił w kierunku wzorca wcześniejszego w szczytowej fazie choroby. Co istotne, zmiany te nie ograniczały się do ogniskowych miejsc zapalnych typowo podkreślanych w patologii SR; zamiast tego rozciągały się na szersze obszary istoty białej. Ponadto, bezzałożeniowy charakter MSI ujawnił dziesiątki innych lipidów zarówno w istocie białej, jak i szarej, których rozmieszczenie zmieniało się wraz z etapem choroby, sugerując zaangażowanie szerszej sieci metabolizmu lipidów.
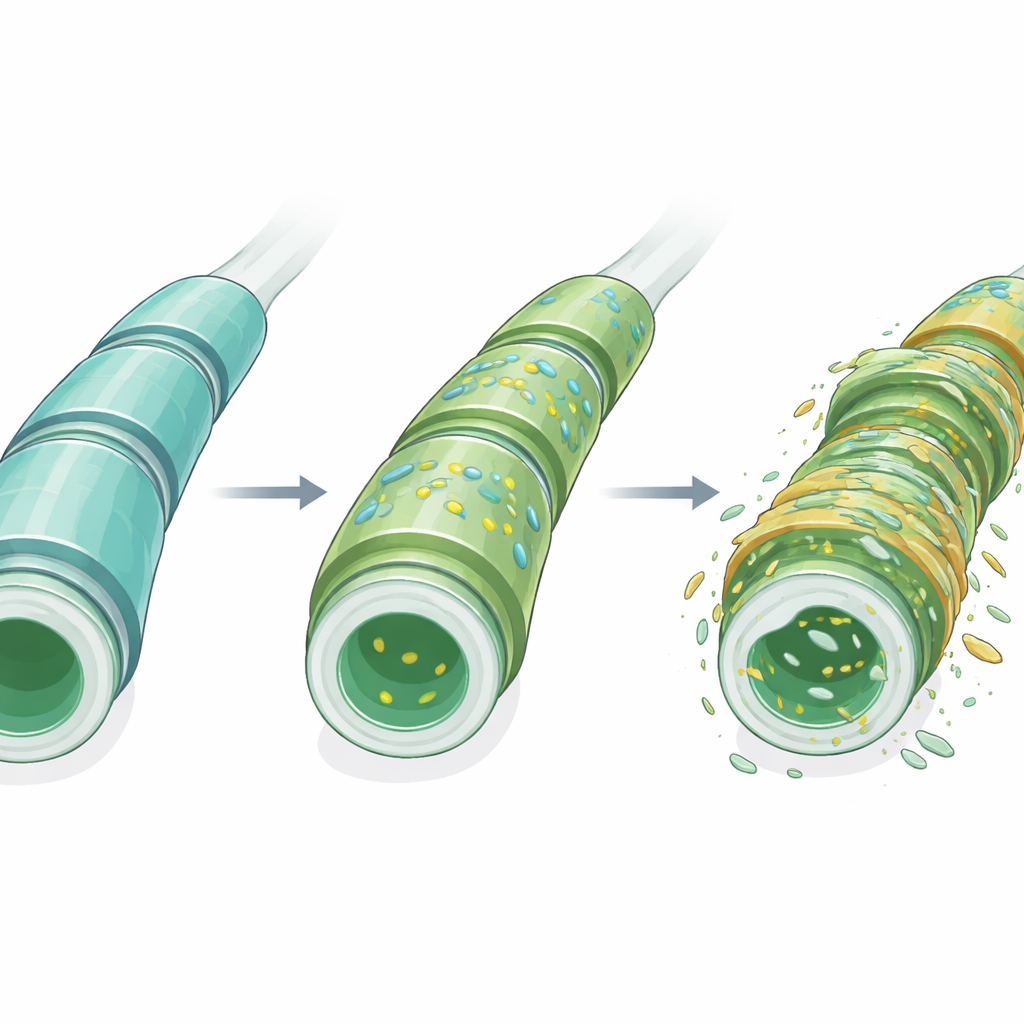
Co to może znaczyć dla diagnozy i leczenia
Pokazując, że sulfatydy mielinowe i inne lipidy zmieniają swoje poziomy i lokalizacje wcześnie i szeroko w przebiegu doświadczalnego SR, praca ta podkreśla profile lipidowe jako potencjalny wczesny system ostrzegawczy przed uszkodzeniem izolacji nerwowej. Możliwość wizualizacji tych molekuł na miejscu, zamiast po homogenizacji tkanki, oferuje precyzyjniejszy obraz przebiegu neurozapalnego. W przyszłości takie wzorce molekularne mogą naprowadzić rozwój czynników kontrastowych do klinicznego MRI lub wskazać nowe cele terapeutyczne ukierunkowane na stabilizację lipidów mielinowych. Choć konieczne są dalsze badania, by przenieść te odkrycia z myszy na ludzi, badanie pokazuje, że obrazowanie spektrometrii mas może uchwycić „molekularne ujęcie” chorego mózgu, które może pomóc przewidywać, monitorować i ostatecznie modyfikować przebieg SR.
Cytowanie: Berlin, K.A., Huizar, C.C., Garza, C. et al. MALDI-TOF mass spectrometry imaging of sulfatide lipid expression in the CNS of mice with experimental autoimmune encephalomyelitis. Sci Rep 16, 11462 (2026). https://doi.org/10.1038/s41598-026-41147-5
Słowa kluczowe: stwardnienie rozsiane, lipidy osłonki mielinowej, obrazowanie spektrometrii mas, nezapalenie nerwowe, sulfatydy