Clear Sky Science · de
MALDI-TOF-Massenspektrometrie-Bildgebung der Sulfatid-Lipid-Expression im ZNS von Mäusen mit experimenteller autoimmuner Enzephalomyelitis
Warum das für die Gehirngesundheit wichtig ist
Multiple Sklerose (MS) ist eine Erkrankung, bei der das körpereigene Immunsystem die Isolierung um Nervenfasern im Gehirn und Rückenmark angreift. Diese Isolierung, Myelin genannt, ist ungewöhnlich reich an Fetten, sogenannten Lipiden. Die Studie stellt eine auf den ersten Blick einfache, aber weitreichende Frage: Zeigen sich subtile Veränderungen dieser Myelinlipide, bevor offensichtliche Symptome und sichtbare Schäden auftreten? Mithilfe einer spezialisierten Form der Massenspektrometrie, mit der Lipide direkt in Mausgewebe „kartiert“ werden, zeigen die Forschenden, dass sich bestimmte myeline Fette früh und breit während experimenteller MS verändern — ein Hinweis auf neue Wege zur Erkennung und möglicherweise Behandlung der Erkrankung.
Ein genauerer Blick auf Myelins fettige Schutzschicht
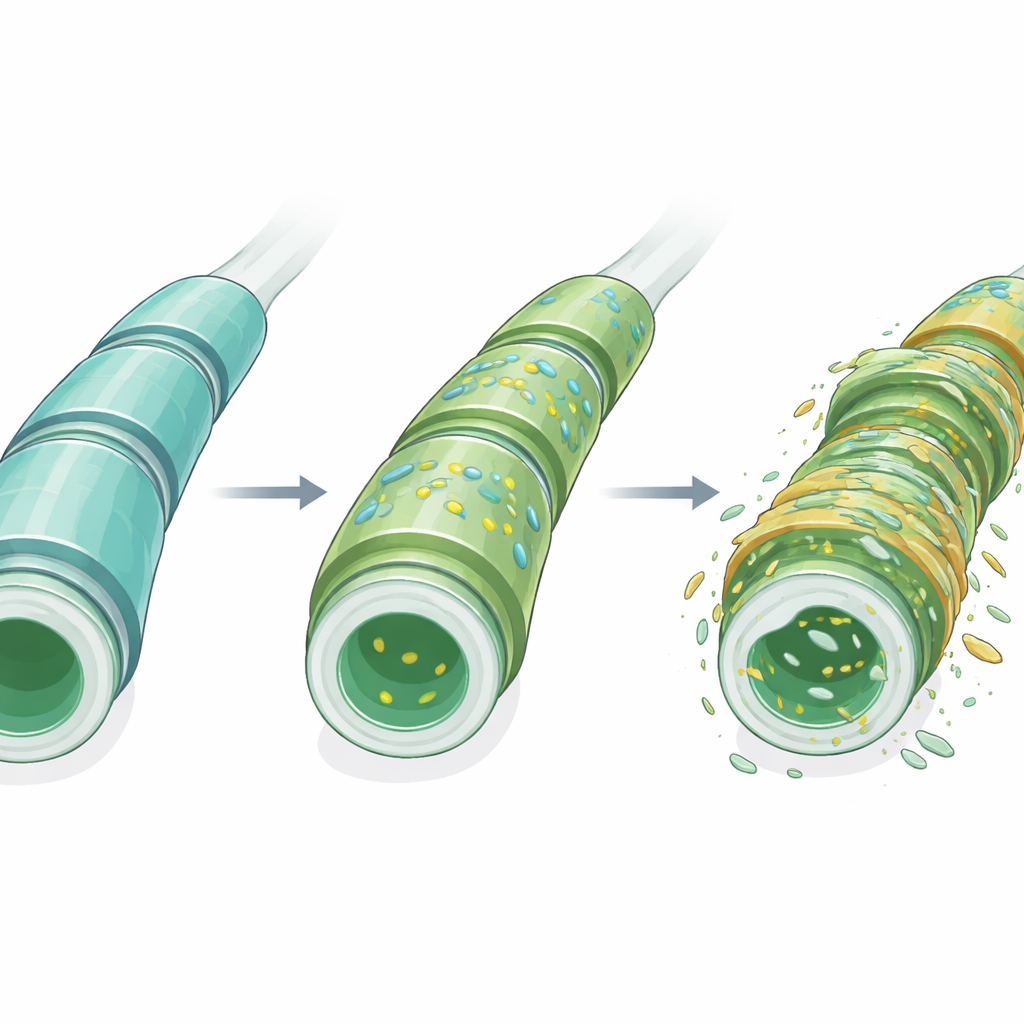
Myelin ist eine mehrschichtige Hülle, die viele Nervenfasern umgibt und für schnelle elektrische Signale sowie die langfristige Gesundheit der Nerven essenziell ist. Anders als in den meisten Geweben dominieren im Myelin Lipide statt Proteine. Zu seinen markantesten Bestandteilen zählen Sulfatide, eine Familie spezialisierter Fette, die in Myelin deutlich höhere Konzentrationen erreichen als in anderen Körperbereichen. Diese Moleküle helfen, die Myelinschichten zu organisieren, unterstützen die Zellen, die Myelin herstellen, und sind an der Kommunikation zwischen Nervenfasern und ihren glialen Stützzellen beteiligt. Störungen in der Produktion oder dem Abbau von Sulfatiden wurden mit mehreren Hirnerkrankungen in Verbindung gebracht, darunter Alzheimer und seltene erbliche Myelinerkrankungen, was sie auch bei MS zu Verdächtigen macht.
Moleküle am Ort sehen, nicht im Reagenzglas
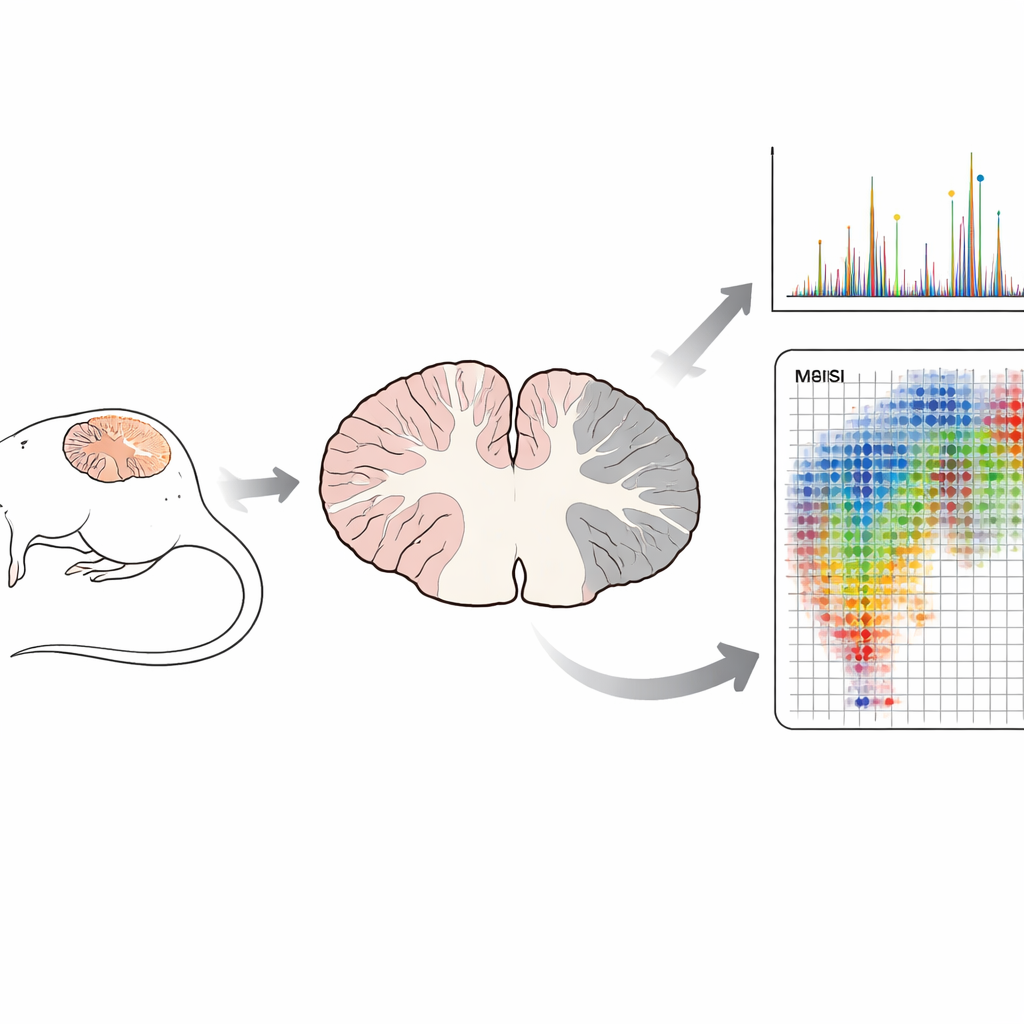
Traditionelle biochemische Methoden zerkleinern Gewebe oft zu einer einheitlichen Mischung, bevor deren Inhaltsstoffe gemessen werden. Dieser Ansatz kann zeigen, was vorhanden ist, zerstört aber den räumlichen Kontext, wo jedes Molekül lokalisiert ist. In dieser Studie nutzte das Team die Matrix-unterstützte Laser-Desorption/Ionisation Time-of-Flight-Massenspektrometrie-Bildgebung (MALDI-TOF MSI), eine Technik, die dünne Gehirnschnitte Punkt für Punkt abtastet. An jedem Punkt setzt ein Laser Moleküle frei, und das Gerät zeichnet ihre Massen auf, wodurch „molekulare Karten“ von hunderten Verbindungen gleichzeitig entstehen. Entscheidend ist, dass dies ohne Marker oder Farbstoffe geschieht und die feine Struktur des Gewebes erhält, die später direkt mit Standardmikroskopfärbungen verglichen werden kann.
Wie sich Myelinlipide während experimenteller MS verändern
Die Forschenden verwendeten ein etabliertes Mausmodell der MS, die experimentelle autoimmune Enzephalomyelitis (EAE), das Entzündungen, Myelinverlust und Nervenschäden nachbildet, wie sie bei Patienten vorkommen. Sie untersuchten das Kleinhirn, eine Hirnregion, in der EAE-Schäden häufig auftreten, in vier Stadien: gesund, eine frühe „Prä-Onset“-Phase ohne offensichtliche Symptome, Krankheitsbeginn und Höhepunkt der Lähmung. Mit Fokus auf eine Reihe bekannter myeliner Sulfatide bestätigten sie zunächst, dass diese Lipide bei gesunden Mäusen in den weißen Substanzbahnen konzentriert sind — den myelinreichen Verkehrsadern der Nervenfasern. Mithilfe von Massenspektrometrie-Fragmentierungsmustern unterschieden sie Sulfatide von anderen Lipiden mit nahezu identischen Massen und bestätigten die Identität von neun von zehn Zielmolekülen.
Frühe und weitreichende Veränderungen vor Symptombeginn
Beim Vergleich der Lipidkarten über die Krankheitsstadien zeichnete sich ein klares Muster ab. Mehrere Sulfatidarten nahmen in der weißen Substanz bereits zu, bevor äußere Anzeichen von EAE sichtbar wurden, während mindestens ein wichtiges Sulfatid abnahm. Die Hauptkomponentenanalyse — ein Verfahren, komplexe Daten in wenige Schlüsselmuster zu verdichten — zeigte, dass sich das gesamte Sulfatidprofil deutlich verschob, besonders um den Krankheitsbeginn, und sich dann zum Höhepunkt der Erkrankung teilweise wieder in Richtung des früheren Musters zurückbewegte. Wichtig ist, dass diese Veränderungen nicht auf die typischen fokalen Entzündungsherde beschränkt waren, die in der MS-Pathologie oft betont werden; stattdessen erstreckten sie sich über die breitere weiße Substanz. Darüber hinaus offenbarte die ungerichtete Natur der MSI Dutzende weiterer Lipide in Weiß- und Grauer Substanz, deren Verteilungen sich mit dem Krankheitsstadium veränderten, was darauf hinweist, dass ein größeres Netzwerk des Lipidstoffwechsels beteiligt ist.
Was das für Diagnose und Behandlung bedeuten könnte
Indem die Studie zeigt, dass myeline Sulfatide und andere Lipide ihre Mengen und Lokalisationen früh und breit während der experimentellen MS verändern, hebt sie Lipidprofile als potenzielles Frühwarnsystem für Schäden an der Nervenisolierung hervor. Die Möglichkeit, diese Moleküle am Ort sichtbar zu machen, statt nachdem das Gewebe homogenisiert wurde, liefert ein präziseres Bild davon, wie sich Neuroinflammation entfaltet. Künftig könnten solche molekularen Muster die Entwicklung von Bildgebungsagentien für klinische MRT-Verfahren lenken oder neue pharmakologische Ziele aufzeigen, die darauf abzielen, Myelinlipide zu stabilisieren. Zwar sind weitere Arbeiten nötig, um diese Befunde von Mäusen auf Menschen zu übertragen, doch die Studie demonstriert, dass die Massenspektrometrie-Bildgebung einen „molekularen Schnappschuss“ des erkrankten Gehirns erfassen kann, der helfen könnte, MS vorherzusagen, zu überwachen und letztlich den Verlauf zu verändern.
Zitation: Berlin, K.A., Huizar, C.C., Garza, C. et al. MALDI-TOF mass spectrometry imaging of sulfatide lipid expression in the CNS of mice with experimental autoimmune encephalomyelitis. Sci Rep 16, 11462 (2026). https://doi.org/10.1038/s41598-026-41147-5
Schlüsselwörter: multiple Sklerose, Myelinlipide, Massenspektrometrie-Bildgebung, Neuroinflammation, Sulfatide