Clear Sky Science · nl
MALDI-TOF massaspectrometrie‑beeldvorming van sulfatide-lipideexpressie in het CZS van muizen met experimentele auto-immuun encefalomyelitis
Waarom dit ertoe doet voor hersengezondheid
Multiple sclerose (MS) is een ziekte waarbij het eigen immuunsysteem van het lichaam de isolatie rond zenuwvezels in de hersenen en het ruggenmerg aanvalt. Die isolatie, myeline genoemd, bevat uitzonderlijk veel vetten die bekendstaan als lipiden. Deze studie stelt een ogenschijnlijk eenvoudige vraag met grote implicaties: laten subtiele veranderingen in deze myelinelipiden zich zien voordat duidelijke symptomen en zichtbare schade optreden? Door een gespecialiseerde vorm van massaspectrometrie te gebruiken om lipiden direct in muizenhersenweefsel te "kaarten", tonen de onderzoekers aan dat specifieke myelinevetten vroeg en wijdverspreid verschuiven tijdens experimentele MS, wat wijst op nieuwe manieren om de ziekte te detecteren en mogelijk te behandelen.
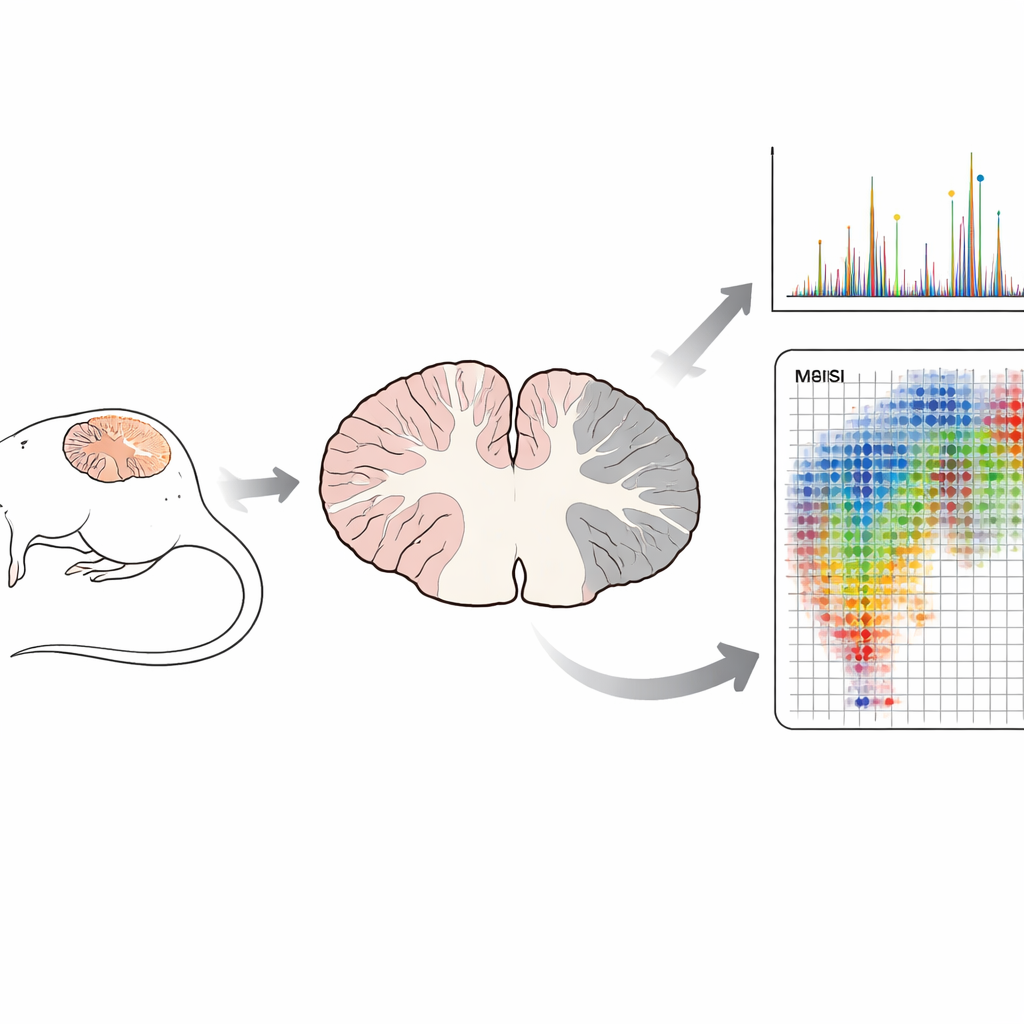
Een nadere blik op myelines vetharnas
Myeline is een gelaagde wikkeling die veel zenuwvezels omgeeft en essentieel is voor snelle elektrische signalering en de langdurige gezondheid van zenuwen. In tegenstelling tot de meeste weefsels wordt myeline gedomineerd door lipiden in plaats van eiwitten. Tot de meest kenmerkende componenten behoren sulfatiden, een familie gespecialiseerde vetten die in myeline bijzonder hoog geconcentreerd zijn vergeleken met andere delen van het lichaam. Deze moleculen helpen de myelinelagen te organiseren, ondersteunen de cellen die myeline maken en nemen deel aan de communicatie tussen zenuwvezels en hun gliale ondersteuningscellen. Verstoring van sulfatidesynthese of -afbraak is in verband gebracht met verschillende hersenaandoeningen, waaronder de ziekte van Alzheimer en zeldzame erfelijke myelineziekten, waardoor ze ook bij MS een belangrijke verdachte zijn.
Moleculen op hun plek zien, niet in een reageerbuis
Traditionele biochemische methoden malen weefsel vaak tot een uniforme mengeling voordat de samenstelling wordt gemeten. Die aanpak kan onthullen wat aanwezig is, maar vernietigt de ruimtelijke context van waar elk molecuul zich bevindt. In deze studie gebruikte het team matrix-assisted laser desorption/ionization time-of-flight massaspectrometriebeeldvorming (MALDI-TOF MSI), een techniek die dunne hersenplakjes punt voor punt scant. Op elk punt maakt een laser moleculen los en registreert het instrument hun massa’s, waarmee "moleculaire kaarten" van honderden verbindingen tegelijk worden opgebouwd. Cruciaal is dat dit gebeurt zonder labels of kleurstoffen en dat de fijne structuur van het weefsel behouden blijft, die later rechtstreeks kan worden vergeleken met standaard microscopische kleuringen.
Hoe myelinelipiden verschuiven tijdens experimentele MS
De onderzoekers gebruikten een goed ingeburgerd muismodel van MS, experimentele auto-immuun encefalomyelitis (EAE), dat ontsteking, myelineverlies en zenuwschade nabootst zoals bij patiënten. Ze bestudeerden het cerebellum, een hersengebied waar EAE-schade vaak optreedt, in vier stadia: gezond, een vroeg "pre-onset" stadium zonder duidelijke symptomen, ziektebegin en piekparalyse. Gericht op een reeks bekende myeline-sulfatiden bevestigden ze eerst dat deze lipiden bij gezonde muizen geconcentreerd zijn in de witte stofbanen, de myline-rijke snelwegen van zenuwvezels. Met behulp van massaspectrometrie-fragmentatiepatronen onderscheidden ze sulfatiden van andere lipiden met nagenoeg identieke massa’s en bevestigden de identiteit van negen van de tien doelmoleculen.
Vroege en wijdverspreide veranderingen vóór symptomen
Bij vergelijking van lipidenkaarten over de ziektefasen trad een duidelijk patroon naar voren. Verschillende sulfatide-soorten namen in hoeveelheid toe in de witte stof vóórdat er zichtbare tekenen van EAE verschenen, terwijl ten minste één belangrijke sulfatide afnam. Principal component analysis—een manier om complexe data samen te vatten in enkele kernpatronen—toonde dat het algehele sulfatideprofiel sterk verschuifde, vooral rond het ziektebegin, en vervolgens gedeeltelijk terugkeerde naar het eerdere patroon bij piekziekte. Belangrijk is dat deze veranderingen zich niet beperkten tot de focale ontstekingsplekken die typisch in MS-pathologie worden benadrukt; in plaats daarvan strekten ze zich uit over de bredere witte stof. Daarnaast onthulde de niet‑gerichte aard van MSI tientallen andere lipiden in zowel witte als grijze stof waarvan de verdeling met het ziekteverloop veranderde, wat suggereert dat een breder netwerk van lipidenmetabolisme betrokken is.
Wat dit kan betekenen voor diagnose en behandeling
Door aan te tonen dat myeline-sulfatiden en andere lipiden hun niveaus en locaties vroeg en breed veranderen tijdens experimentele MS, benadrukt dit werk lipidenprofielen als een mogelijk vroeg waarschuwingssysteem voor beschadiging van zenuwisolatie. Het vermogen om deze moleculen op hun plek te visualiseren, in plaats van nadat weefsel is gehomogeniseerd, biedt een preciezer beeld van hoe neuro-inflammatie zich ontwikkelt. In de toekomst zouden dergelijke moleculaire patronen de ontwikkeling van beeldvormingsmiddelen voor klinische MRI kunnen aansturen of kunnen wijzen op nieuwe medicijndoelen gericht op het stabiliseren van myinelipiden. Hoewel meer onderzoek nodig is om deze bevindingen van muizen naar mensen te vertalen, toont de studie aan dat massaspectrometriebeeldvorming een "moleculair momentopname" van de zieke hersenen kan vastleggen die kan helpen bij het voorspellen, monitoren en uiteindelijk beïnvloeden van het beloop van MS.
Bronvermelding: Berlin, K.A., Huizar, C.C., Garza, C. et al. MALDI-TOF mass spectrometry imaging of sulfatide lipid expression in the CNS of mice with experimental autoimmune encephalomyelitis. Sci Rep 16, 11462 (2026). https://doi.org/10.1038/s41598-026-41147-5
Trefwoorden: multiple sclerose, myeline-lipiden, massaspectrometriebeeldvorming, neuro-inflammatie, sulfatiden