Clear Sky Science · fr
Imagerie par spectrométrie de masse MALDI-TOF de l’expression des lipides sulfatides dans le SNC de souris atteintes d’encéphalomyélite auto-immune expérimentale
Pourquoi cela compte pour la santé cérébrale
La sclérose en plaques (SEP) est une maladie dans laquelle le système immunitaire attaque l’isolant entourant les fibres nerveuses du cerveau et de la moelle épinière. Cet isolant, appelé myéline, est exceptionnellement riche en graisses appelées lipides. Cette étude pose une question apparemment simple mais aux grandes implications : des changements subtils dans ces lipides de la myéline apparaissent-ils avant l’apparition de symptômes évidents et de lésions visibles ? En utilisant une forme spécialisée de spectrométrie de masse pour « cartographier » les lipides directement dans le tissu cérébral de souris, les chercheurs montrent que des lipides myéliniques spécifiques se modifient tôt et de manière étendue pendant une SEP expérimentale, suggérant de nouvelles voies pour détecter et peut‑être traiter la maladie.
Un regard approfondi sur l’armure lipidique de la myéline
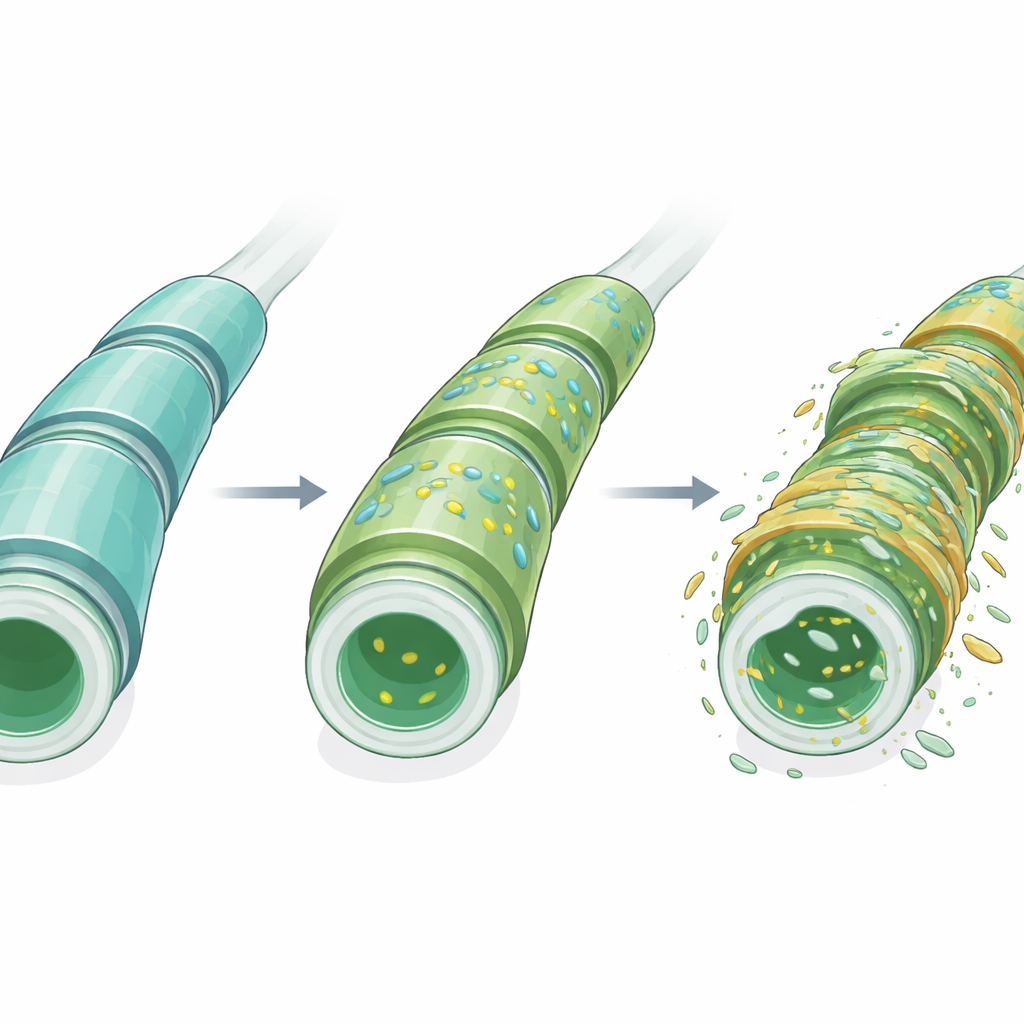
La myéline est un enroulement multicouche qui entoure de nombreuses fibres nerveuses et est essentiel pour la conduction électrique rapide et la santé nerveuse à long terme. Contrairement à la plupart des tissus, la myéline est dominée par les lipides plutôt que par les protéines. Parmi ses composants les plus distinctifs figurent les sulfatides, une famille de lipides spécialisés présents à des niveaux particulièrement élevés dans la myéline par rapport à d’autres régions du corps. Ces molécules contribuent à organiser les couches de myéline, soutiennent les cellules qui la produisent et participent à la communication entre les fibres nerveuses et leurs cellules gliales de soutien. Des perturbations de la production ou de la dégradation des sulfatides ont été liées à plusieurs maladies cérébrales, notamment la maladie d’Alzheimer et des affections myéliniques héréditaires rares, ce qui en fait également un suspect de choix dans la SEP.
Voir les molécules in situ, pas dans un tube à essai
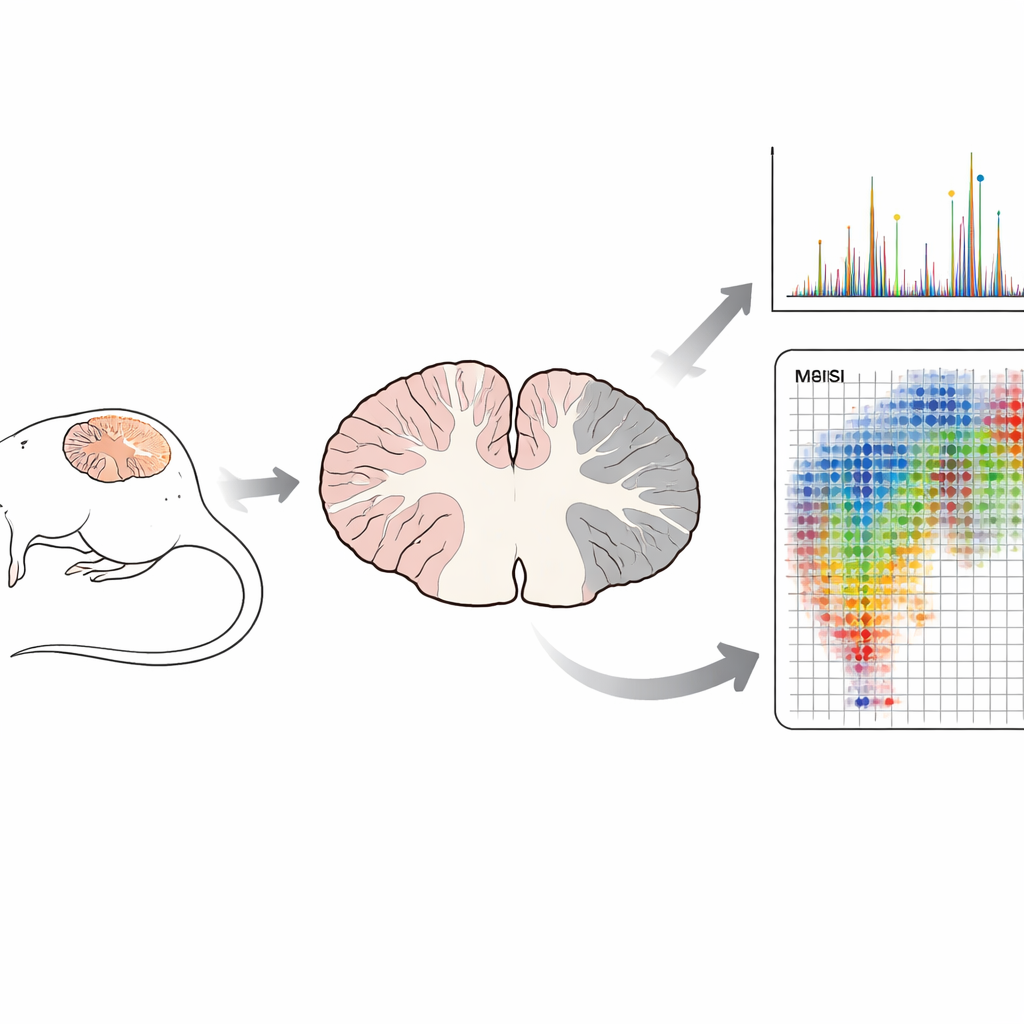
Les méthodes biochimiques traditionnelles broient souvent le tissu en un mélange homogène avant d’en mesurer le contenu. Cette approche peut révéler ce qui est présent, mais elle détruit le contexte spatial où chaque molécule se trouve. Dans cette étude, l’équipe a utilisé l’imagerie par spectrométrie de masse par désorption/ionisation laser assistée par matrice temps de vol (MALDI-TOF MSI), une technique qui balaie des coupes cérébrales fines point par point. À chaque point, un laser libère les molécules et l’instrument enregistre leurs masses, construisant des « cartes moléculaires » de centaines de composés en une seule fois. Fait crucial, cela se fait sans marqueurs ni colorants et préserve la structure fine du tissu, qui peut ensuite être comparée directement aux colorations microscopiques classiques.
Comment les lipides de la myéline évoluent pendant la SEP expérimentale
Les chercheurs ont utilisé un modèle murin bien établi de la SEP appelé encéphalomyélite auto-immune expérimentale (EAE), qui reproduit l’inflammation, la perte de myéline et les lésions nerveuses semblables à celles observées chez les patients. Ils ont examiné le cervelet, une région cérébrale où les lésions d’EAE apparaissent souvent, à quatre stades : sain, une phase précoce « pré-émission » sans symptômes évidents, le début de la maladie et le pic de paralysie. En se concentrant sur un ensemble de sulfatides myéliniques connus, ils ont d’abord confirmé que, chez les souris saines, ces lipides sont concentrés dans les faisceaux de substance blanche, les autoroutes riches en myéline des fibres nerveuses. En utilisant les schémas de fragmentation en spectrométrie de masse, ils ont distingué les sulfatides d’autres lipides de masses presque identiques et confirmé l’identité de neuf des dix molécules ciblées.
Des changements précoces et étendus avant les symptômes
Lorsque les cartes lipidiques ont été comparées entre les stades de la maladie, un schéma clair est apparu. Plusieurs espèces de sulfatides ont augmenté en abondance dans la substance blanche avant l’apparition de signes extérieurs d’EAE, tandis qu’au moins une sulfatide importante a diminué. L’analyse en composantes principales — une méthode pour résumer des données complexes en quelques motifs clés — a montré que le profil global des sulfatides a fortement évolué, en particulier autour du début de la maladie, puis est revenu partiellement vers le profil antérieur au pic de la maladie. Fait important, ces changements n’étaient pas confinés aux foyers inflammatoires typiquement mis en avant dans la pathologie de la SEP ; au contraire, ils s’étendaient à une plus large portion de la substance blanche. De plus, le caractère non ciblé de l’imagerie MSI a révélé des dizaines d’autres lipides dans la substance blanche et grise dont la distribution variait selon le stade de la maladie, suggérant qu’un réseau plus vaste du métabolisme lipidique est impliqué.
Ce que cela pourrait signifier pour le diagnostic et le traitement
En montrant que les sulfatides myéliniques et d’autres lipides modifient leurs niveaux et leurs localisations tôt et de manière étendue pendant la SEP expérimentale, ce travail met en lumière les profils lipidiques comme un système d’alerte précoce potentiel pour les atteintes de l’isolant nerveux. La capacité à visualiser ces molécules in situ, plutôt qu’après homogénéisation du tissu, offre une image plus précise du déroulement de la neuroinflammation. À l’avenir, de tels motifs moléculaires pourraient orienter le développement d’agents d’imagerie utilisables avec l’IRM clinique ou indiquer de nouvelles cibles médicamenteuses visant à stabiliser les lipides de la myéline. Bien que des travaux supplémentaires soient nécessaires pour traduire ces résultats des souris aux humains, l’étude démontre que l’imagerie par spectrométrie de masse peut capturer un « instantané moléculaire » du cerveau malade susceptible d’aider à prédire, surveiller et, en fin de compte, modifier l’évolution de la SEP.
Citation: Berlin, K.A., Huizar, C.C., Garza, C. et al. MALDI-TOF mass spectrometry imaging of sulfatide lipid expression in the CNS of mice with experimental autoimmune encephalomyelitis. Sci Rep 16, 11462 (2026). https://doi.org/10.1038/s41598-026-41147-5
Mots-clés: sclérose en plaques, lipides de la myéline, imagerie par spectrométrie de masse, neuroinflammation, sulfatides