Clear Sky Science · ru
In silico проектирование мультиэпитопной вакцины против антибиотикорезистентного Acinetobacter baumannii
Почему это важно для повседневного здоровья
Больницы должны нас исцелять, но некоторые из самых опасных инфекций возникают именно в них. Один из виновников — выносливая бактерия Acinetobacter baumannii — выработала устойчивость ко многим из наших сильнейших антибиотиков, превращая рутинный уход в риск для жизни у уязвимых пациентов. В этом исследовании рассматривается новый способ опережать такие супермоши: использование вычислительных методов для проектирования вакцины следующего поколения, составленной из тщательно отобранных коротких фрагментов белков, с целью предотвращения инфекций прежде, чем они начнутся.
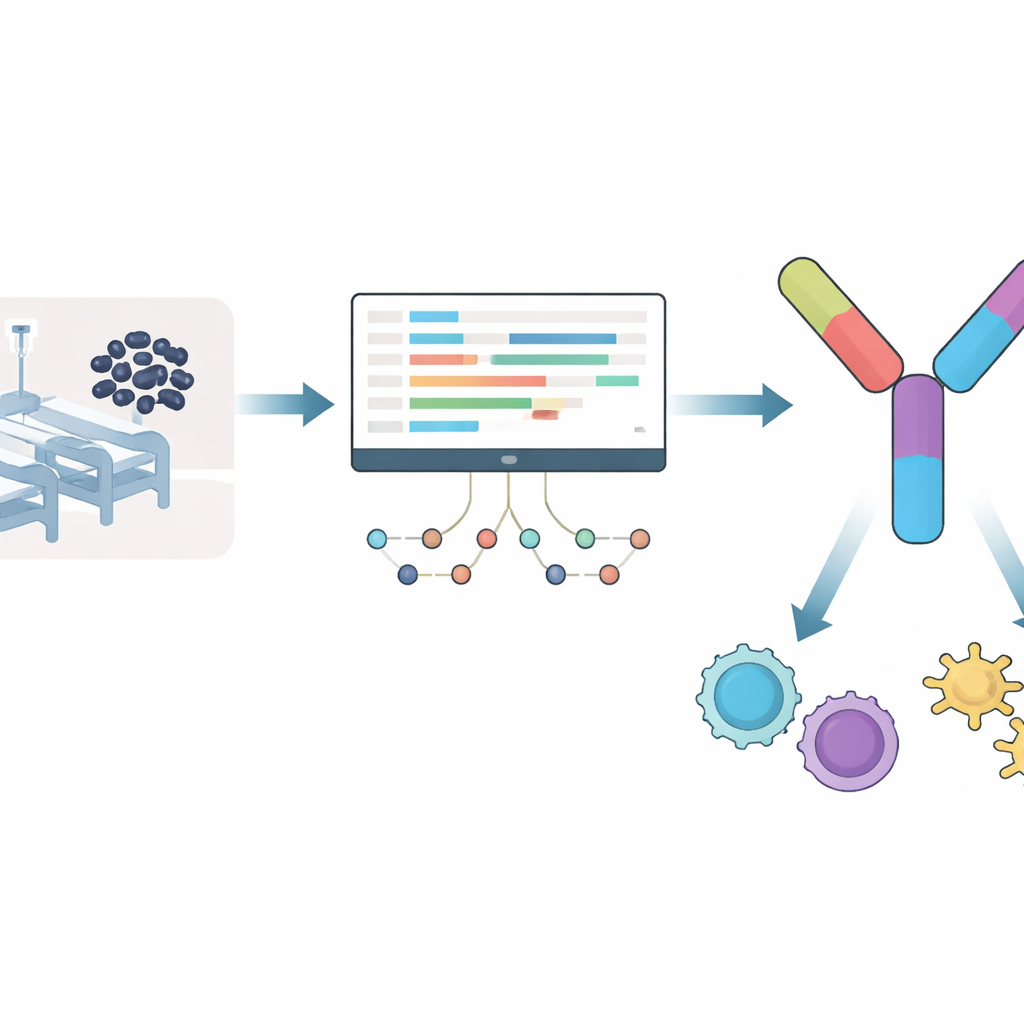
Больничный микроб, который не уходит
Acinetobacter baumannii процветает на поверхностях и оборудовании в больницах, где может заражать людей с ослабленным иммунитетом, хроническими заболеваниями легких или длительным пребыванием в отделении интенсивной терапии. Он принадлежит к печально известной группе госпитальных микробов, известных множественной лекарственной устойчивостью. Как только этот микроб становится резистентным к карбапенемам — классу антибиотиков последней инстанции — у врачей остается мало безопасных вариантов. Поскольку одобренной вакцины нет, Всемирная организация здравоохранения отнесла эту бактерию к приоритетным целям для разработки вакцин, что побудило исследователей искать более умные способы борьбы с ней.
Даем бактерии показать свои слабые места
Вместо того чтобы полагаться на догадки о том, какие части бактерии могут быть хорошими мишенями для вакцины, команда наблюдала, как Acinetobacter baumannii реагирует на воздействие ключевого антибиотика — меропенема. Они проанализировали данные РНК‑секвенирования, которые показывают, какие гены включаются или выключаются, после девяти часов воздействия препарата. Более тысячи генов были повышены и примерно такое же количество — понижено, особенно в путях, связанных с метаболизмом, системами секреции и механизмами выкачивания препаратов, которые бактерия может использовать, чтобы уклониться от лечения. Из белков, кодируемых этими активированными генами, исследователи исключили те, что похожи на белки человека или обычных кишечных бактерий, чтобы снизить риск побочных эффектов. После этой фильтрации остался сокращенный список бактериальных белков, которые важны при воздействии антибиотика и вряд ли запутают иммунную систему.
Создание многокомпонентной вакцины из крошечных фрагментов
Из этой уточненной подборки ученые искали короткие участки белков, называемые эпитопами, которые особенно хорошо распознаются иммунными клетками человека. Они сосредоточились на двух типах: фрагментах, стимулирующих «убийственные» T‑клетки, которые уничтожают инфицированные клетки, и тех, что активируют «хелперные» T‑клетки, координирующие более широкую иммунную защиту. С помощью проверенных предиктивных инструментов они отобрали 12 эпитопов для убийственных клеток и 7 эпитопов для хелперных клеток, которые были нетоксичны, вряд ли вызывали аллергию и с высокой вероятностью связывались с распространенными маркерами иммунной системы человека. Критически важно, что эти эпитопы происходили из белков, полностью консервативных в нескольких высоковирулентных штаммах Acinetobacter, что повышает шансы, что одна вакцина сможет защитить от многих вариантов микроба.
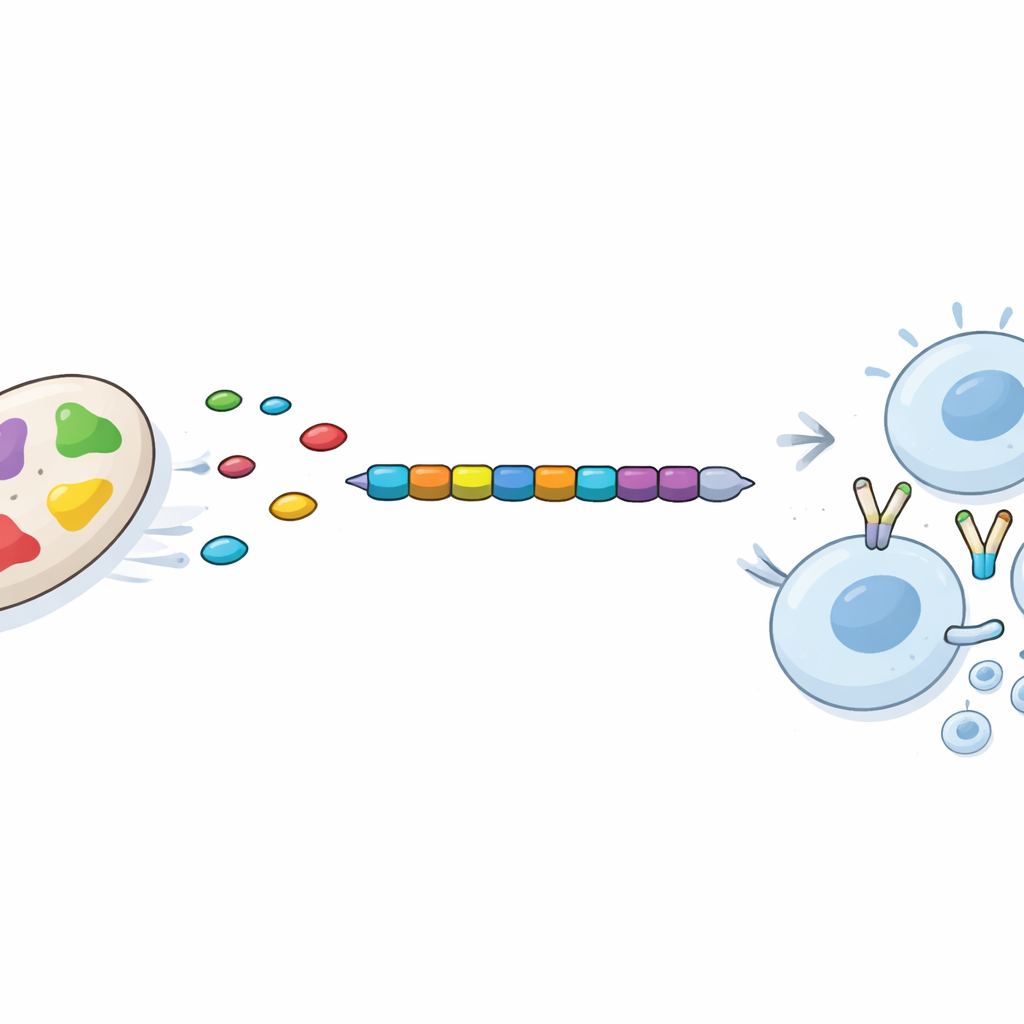
Проверка виртуальной вакцины на стабильность и ответ
Выбранные эпитопы были соединены в заданном порядке, чтобы создать единый вакцинный белок длиной 335 аминокислот, с иммунно‑стимулирующим компонентом, заимствованным у человека, добавленным на один конец. Команда затем использовала современные компьютерные модели, чтобы предсказать, как этот многокомпонентный белок свернется в трехмерной структуре и насколько он будет стабилен в водной среде, подобной организму. Детализированные симуляции показали, что структура быстро принимает компактную стабильную форму и сохраняет ее со временем. Отдельные докинговые исследования указали, что каждый эпитоп может плотно вписаться в рецепторы иммунной системы человека. Наконец, имитация работы иммунной системы in silico предсказала, что доза этой вакцины быстро устранит введенный антиген, вызовет раннее образование антител, сильно активирует убийственные и хелперные T‑клетки и сформирует долгую иммунную память, не обнаружив признаков чрезмерной или несбалансированной реакции.
Что это означает и что дальше
Эта работа пока не приводит к готовой для инъекции вакцине, но она демонстрирует, насколько мощными могут быть вычислительные методы для проектирования вакцин, нацеленных на те свойства, которые делают госпитального микроба лекарственно‑устойчивым. Сосредоточившись на компонентах бактерии, которые включаются при антибиотическом стрессe и присутствуют во многих опасных штаммах, и собрав несколько таких фрагментов в единый конструкт, исследование представляет многообещающий план широкозонной вакцины против Acinetobacter baumannii. Следующие ключевые шаги — лабораторные и животные исследования, чтобы подтвердить, что эта виртуальная вакцина безопасна, стабильна и защищает в реальных условиях — необходимый мост от умного дизайна на экране до спасительной защиты у постели больного.
Цитирование: Khadka, S., Khan, M.A., Iqbal, S. et al. In silico design of a multiepitope vaccine against antibiotic drug-resistant Acinetobacter baumannii. Sci Rep 16, 14151 (2026). https://doi.org/10.1038/s41598-025-30795-8
Ключевые слова: антибиотикорезистость, госпитальные инфекции, Acinetobacter baumannii, разработка вакцин, вычислительная иммунология