Clear Sky Science · ru
Удаление HDAC3 в миелоидных клетках защищает от травмы зрительного нерва
Защита зрения после травм головы и глаз
Удары по голове или лицу могут оставить не только синяк — они могут незаметно повредить зрительный нерв, который передаёт зрительную информацию от глаза к мозгу. Это состояние, называемое травматической оптической нейропатией, часто приводит к необратимой потере зрения и в настоящее время не имеет надёжного лечения. В представленном исследовании рассматривается новая стратегия: перепрограммировать определённые иммунные клетки, чтобы они эффективнее удаляли повреждённые элементы и помогали восстановлению зрительного нерва, потенциально сохраняя зрение после травмы.
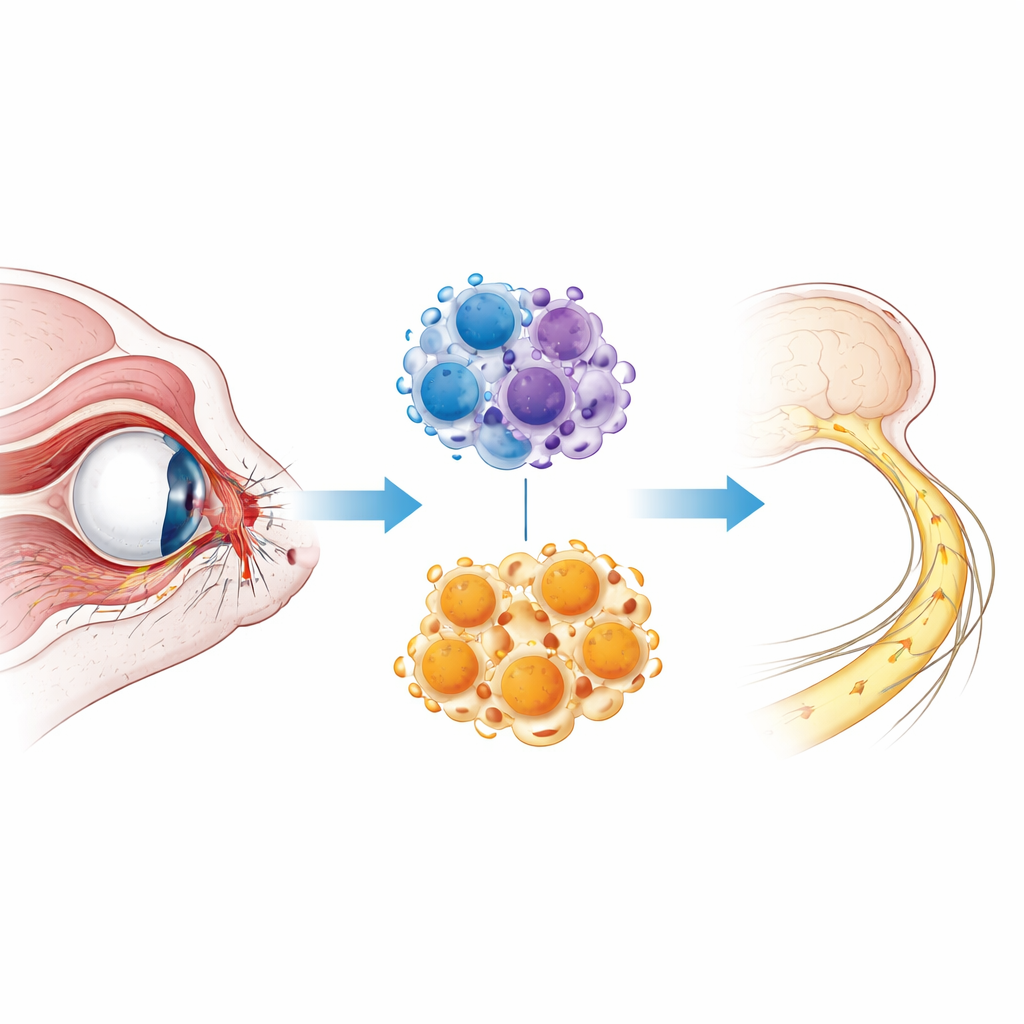
Когда повреждена проводящая система глаза
Зрительный нерв — это плотный пучок волокон от ганглиозных клеток сетчатки, выходных нейронов глаза. При сжатии или растяжении этого пучка во время травмы многие волокна погибают мгновенно, тогда как другие дегенерируют постепенно в течение дней или недель. Отёк, воспаление и скопление клеточного и миелинового мусора усугубляют повреждение и затрудняют отрастание выживших волокон. Существующая помощь в основном направлена на стабилизацию пациента, поскольку у нас по-прежнему нет способов остановить эту волну дегенерации. Чтобы подробно изучать эти процессы, учёные часто используют модель на мышах, в которой зрительный нерв кратковременно защемляют, имитируя ключевые черты травматической оптической нейропатии.
Неожиданная сила «уборочных» клеток
После травмы специализированные иммунные клетки — микроглия и макрофаги — устремляются к повреждённому нерву и сетчатке. Эти «бригады уборки», объединённые термином миелоидные клетки, имеют двойную природу: они могут подпитывать воспаление, но также способны к эфероцитозу — поглощать и переваривать мёртвые клетки и обломки, что способствует заживлению тканей. Исследователи сосредоточились на молекулярном переключателе внутри этих клеток — ферменте HDAC3, который контролирует, какие гены включаются или выключаются. Предыдущие работы показали, что блокирование HDAC3 непосредственно в нервных клетках может снижать их гибель. В этом исследовании команда поставила другой вопрос: что произойдёт, если убрать HDAC3 специально из миелоидных клеток?
Перевод миелоидных клеток в режим восстановления
Используя генетически модифицированных мышей, учёные удалили HDAC3 только в миелоидных клетках, оставив его в других тканях. После защемления зрительного нерва у этих мышей сохранялось больше ганглиозных клеток сетчатки и регистрировались более сильные электрические сигналы от сетчатки по сравнению с контрольными животными, что указывает на лучшую функцию зрения. У них также было больше восстанавливающихся волокон, растущих за участком повреждения. Микроскопия показала, что миелоидные клетки без HDAC3 активнее поглощали умирающие клетки в сетчатке и удаляли миелиновые обломки из зрительного нерва. Когда миелиновые фрагменты предлагались макрофагам в культуре, клетки без HDAC3 гораздо сильнее поглощали этот материал, подтверждая, что фермент обычно сдерживает их уборочную активность.
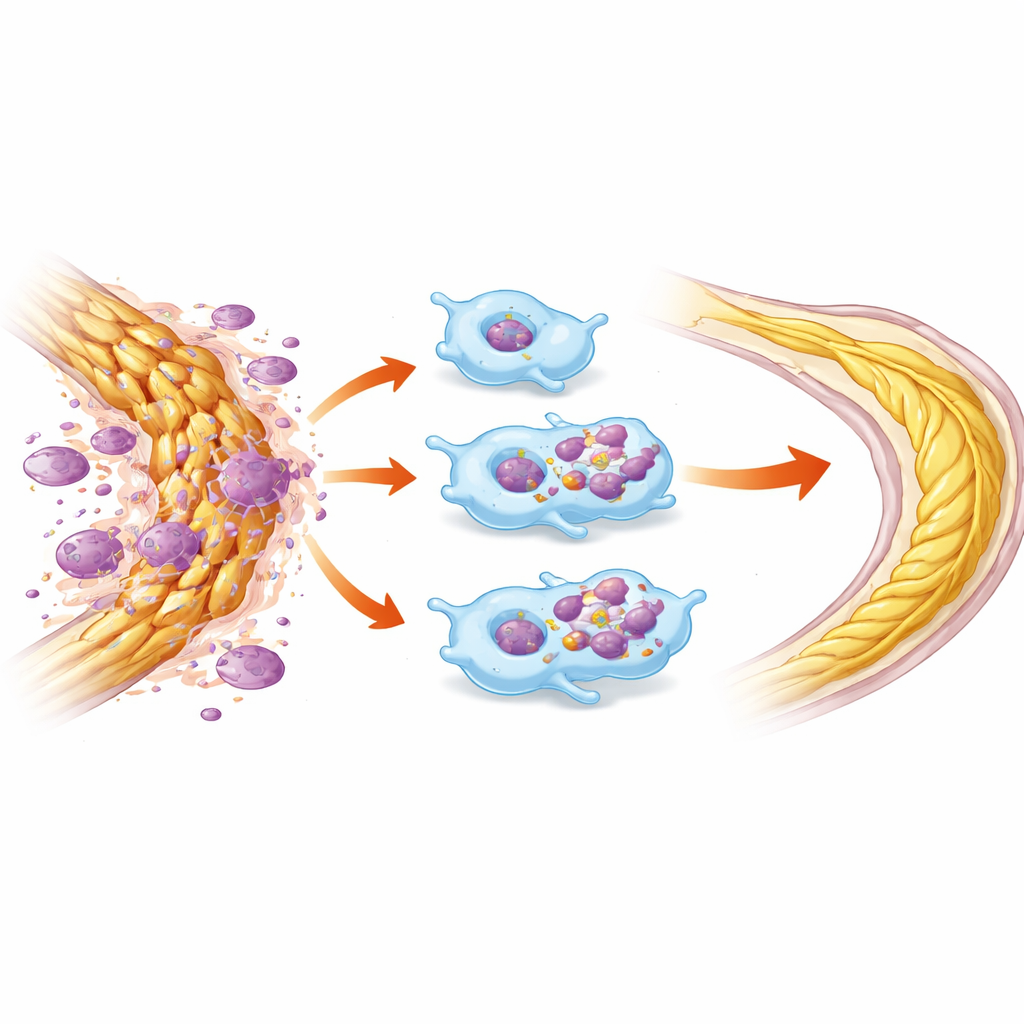
Ключевой рецептор помогает ускорить очистку от мусора
Чтобы понять, как HDAC3 контролирует такое поведение, исследователи изучали молекулы, участвующие в эфероцитозе. Они обнаружили, что макрофаги, лишённые HDAC3, увеличивали продукцию MerTK — клеточного рецептора, известного распознаванием и поглощением мёртвых клеток и миелина — вместе с сопутствующими факторами, способствующими разрешению воспаления. Блокирование MerTK небольшим молекулярным ингибитором в значительной мере устраняло преимущество в поглощении миелина, что указывает на то, что удаление HDAC3 помогает, освобождая MerTK и его партнёров для более активной работы. Любопытно, что при удалении HDAC3 только из долговечных микроглиальных клеток, но не из инфильтрирующих макрофагов, защитный эффект для клеток сетчатки и функции зрения исчезал, указывая на макрофаги как на главных исполнителей этой восстановительной программы в данной модели травмы.
Что это может значить для будущих методов лечения
Проще говоря, работа показывает: ослабление HDAC3 в определённых иммунных клетках превращает их в более эффективных уборщиков — они быстрее удаляют мёртвые клетки и миелиновую оболочку, успокаивают воспаление и создают более благоприятную среду для отрастания повреждённых волокон зрительного нерва. Хотя требуется больше исследований, чтобы точно выяснить, как HDAC3 регулирует MerTK, и разработать безопасные препараты, избирательно действующие на миелоидные клетки, сама концепция ясна. Научив собственные «бригады уборки» организма работать лучше, мы однажды сможем сохранить зрение и стимулировать восстановление нервов после тяжёлых травм глаза и головы.
Цитирование: Shahror, R.A., Morris, C.A., Cunningham, A. et al. Myeloid HDAC3 deletion protects against traumatic optic injury. Cell Death Discov. 12, 163 (2026). https://doi.org/10.1038/s41420-026-03030-0
Ключевые слова: травматическая оптическая нейропатия, повреждение зрительного нерва, макрофаги, HDAC3, эфероцитоз