Clear Sky Science · es
La eliminación de HDAC3 en mieloides protege contra la lesión óptica traumática
Proteger la visión tras traumatismos craneales y oculares
Los golpes contundentes en la cabeza o la cara pueden hacer más que dejar un hematoma: silenciosamente pueden dañar el nervio óptico que transporta la información visual desde el ojo hasta el cerebro. Esta condición, llamada neuropatía óptica traumática, a menudo conduce a pérdida visual permanente y actualmente no tiene un tratamiento fiable. El estudio resumido aquí explora una nueva estrategia: reprogramar ciertos tipos de células inmunitarias para que eliminen los daños con mayor eficiencia y ayuden al nervio óptico a repararse, con lo que potencialmente se preservaría la vista tras la lesión.
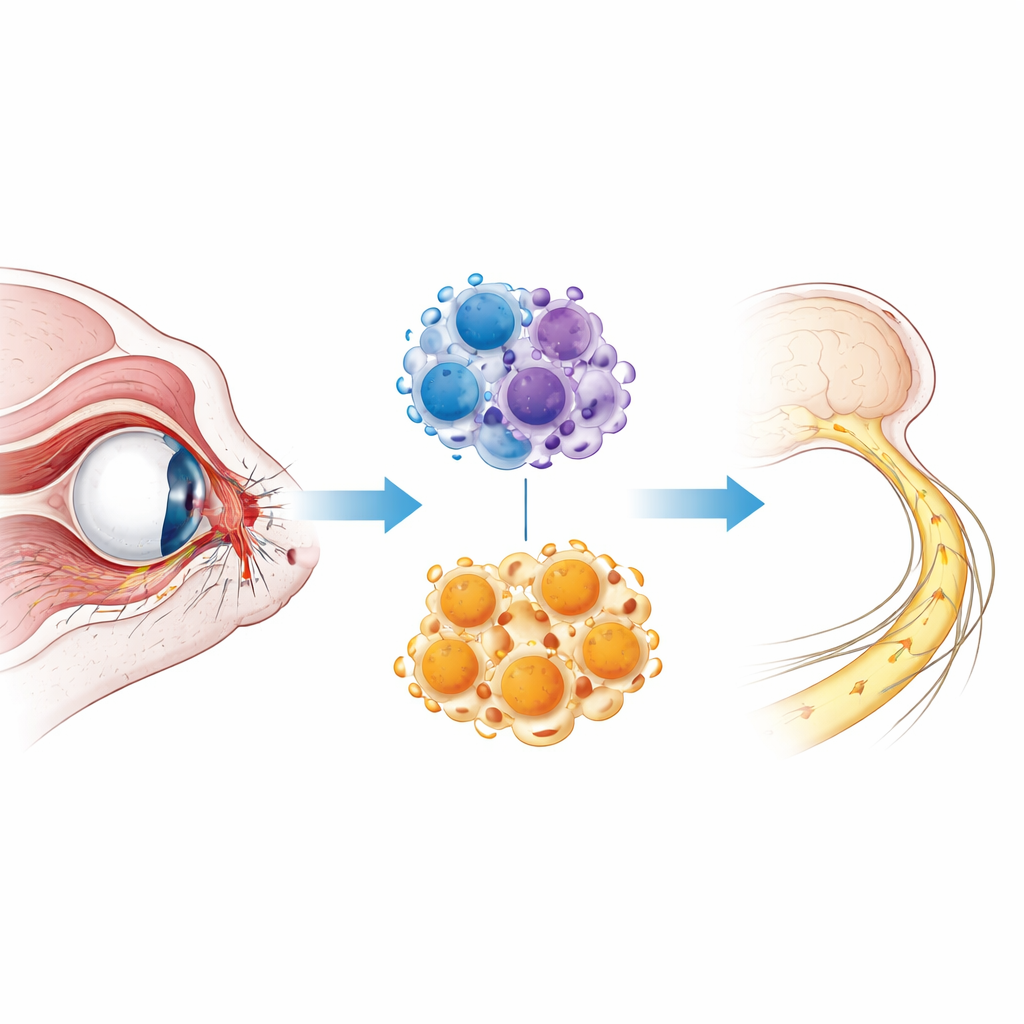
Cuando se deteriora el cableado ocular
El nervio óptico es un haz compacto de fibras procedentes de las células ganglionares de la retina, las neuronas de salida del ojo. Cuando este haz se aplasta o estira durante un traumatismo, muchas de esas fibras nerviosas mueren de inmediato, mientras que otras degeneran lentamente durante días o semanas. La hinchazón, la inflamación y la acumulación de restos celulares y de mielina empeoran la lesión y dificultan que las fibras nerviosas supervivientes vuelvan a crecer. Los cuidados actuales se centran en estabilizar al paciente, porque aún nos faltan formas de detener esta onda de degeneración. Para estudiar estos procesos en detalle, los científicos usan a menudo un modelo en ratón en el que se pellizca brevemente el nervio óptico, imitando las características principales de la neuropatía óptica traumática.
El poder inesperado de las células limpiadoras
Tras la lesión, células inmunitarias especializadas llamadas microglía y macrófagos acuden al nervio y a la retina dañados. Estas «brigadas de limpieza», conocidas colectivamente como células mieloides, pueden ser de doble filo: pueden alimentar la inflamación, pero también realizar eferocitosis—engullir y digerir células muertas y restos para que el tejido pueda sanar. Los investigadores se centraron en un interruptor molecular dentro de estas células, una enzima llamada HDAC3 que ayuda a controlar qué genes se activan o se silencian. Trabajos previos mostraron que bloquear HDAC3 directamente en las neuronas podía reducir la muerte celular. Aquí, el equipo planteó una pregunta distinta: ¿qué ocurre si HDAC3 se elimina específicamente de las células mieloides?
Convertir las células mieloides en modo reparación
Usando ratones genéticamente modificados, los científicos eliminaron HDAC3 solo en las células mieloides dejando la enzima intacta en el resto del organismo. Tras el aplastamiento del nervio óptico, estos ratones conservaron más neuronas retinianas y mostraron señales eléctricas más intensas desde la retina en comparación con ratones normales, lo que indica una mejor función visual. También presentaron más fibras nerviosas en regeneración que crecieron más allá del sitio de la lesión. La microscopia reveló que las células mieloides sin HDAC3 estaban más activas al engullir células moribundas en la retina y al retirar los restos de mielina del nervio óptico. Cuando se ofrecieron fragmentos de mielina a macrófagos en cultivo, las células sin HDAC3 ingirieron mucha más de esta materia, confirmando que la enzima restringe habitualmente su capacidad de limpieza.
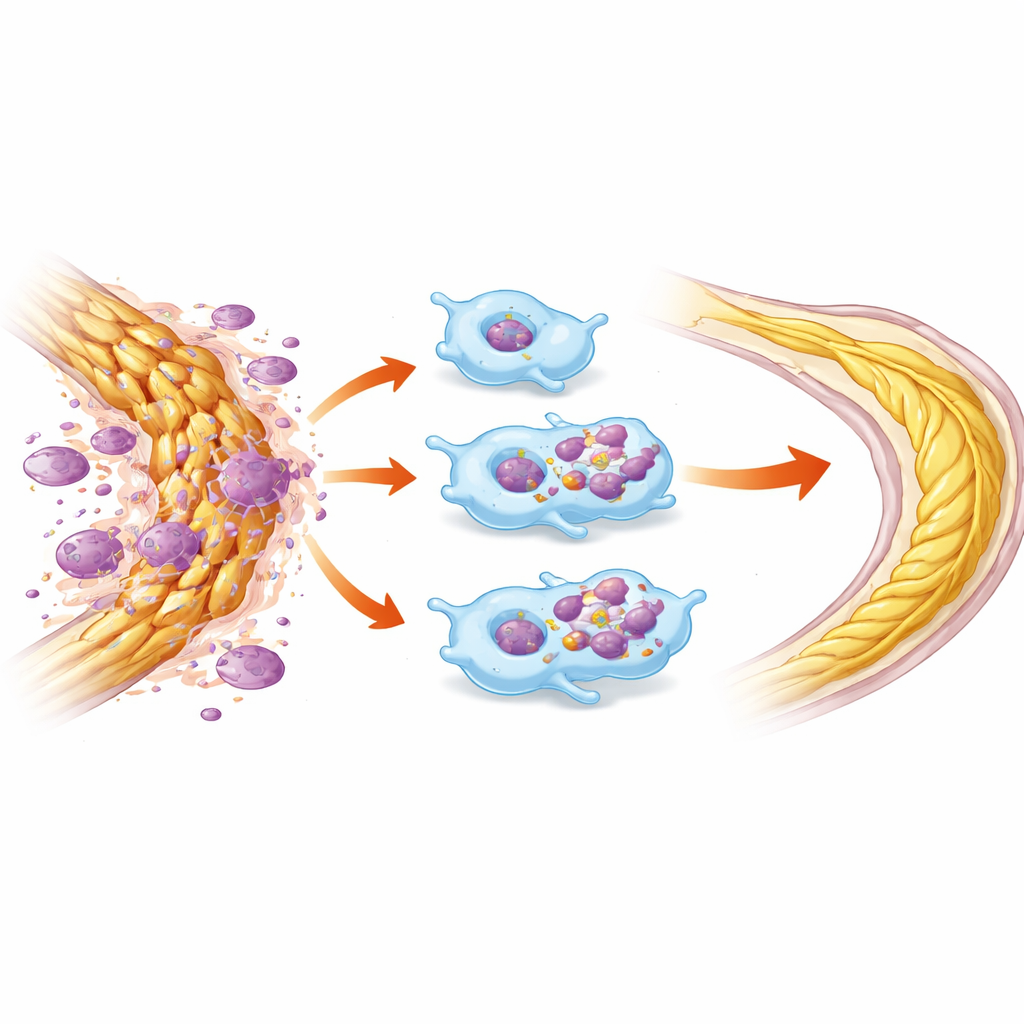
Un receptor clave impulsa la eliminación de residuos
Para entender cómo HDAC3 controla este comportamiento, los investigadores examinaron moléculas implicadas en la eferocitosis. Hallaron que los macrófagos deficientes en HDAC3 aumentaban la producción de MerTK, un receptor de superficie conocido por reconocer e ingerir células muertas y mielina, junto con factores relacionados que promueven la resolución de la inflamación. Bloquear MerTK con un inhibidor de pequeña molécula borró en gran medida la ventaja en la captación de mielina, lo que sugiere que la eliminación de HDAC3 ayuda al permitir que MerTK y sus colaboradores actúen con mayor fuerza. Curiosamente, cuando HDAC3 se eliminó solo de las microglías de larga vida pero no de los macrófagos infiltrantes, el efecto protector sobre las células retinianas y la función desapareció, apuntando a los macrófagos como los principales impulsores de este programa de reparación en este modelo de lesión.
Qué podría significar esto para tratamientos futuros
En términos simples, este trabajo muestra que reducir HDAC3 en ciertas células inmunitarias las convierte en conserjes más eficientes: eliminan las células muertas y el aislamiento de las fibras nerviosas con mayor rapidez, calman la inflamación y crean un entorno más favorable para que las fibras dañadas del nervio óptico vuelvan a crecer. Aunque se necesita más investigación para entender exactamente cómo HDAC3 regula MerTK y para diseñar fármacos seguros que actúen de forma selectiva sobre las células mieloides, el concepto es claro. Al enseñar a las brigadas de limpieza del propio organismo a hacer mejor su trabajo, algún día podríamos proteger la visión y promover la reparación nerviosa tras lesiones oculares y craneales devastadoras.
Cita: Shahror, R.A., Morris, C.A., Cunningham, A. et al. Myeloid HDAC3 deletion protects against traumatic optic injury. Cell Death Discov. 12, 163 (2026). https://doi.org/10.1038/s41420-026-03030-0
Palabras clave: neuropatía óptica traumática, lesión del nervio óptico, macrófagos, HDAC3, eferocitosis