Clear Sky Science · fr
La suppression de HDAC3 dans les myéloïdes protège contre les lésions optiques traumatiques
Protéger la vision après des blessures à la tête et aux yeux
Des coups contondants à la tête ou au visage peuvent faire plus que provoquer un bleu : ils peuvent discrètement endommager le nerf optique qui transporte l’information visuelle de l’œil vers le cerveau. Cette affection, appelée neuropathie optique traumatique, conduit souvent à une perte permanente de la vision et ne bénéficie aujourd’hui d’aucun traitement fiable. L’étude résumée ici explore une nouvelle stratégie : reprogrammer certains globules blancs pour qu’ils éliminent les dégâts plus efficacement et favorisent la réparation du nerf optique, ce qui pourrait préserver la vision après une blessure.
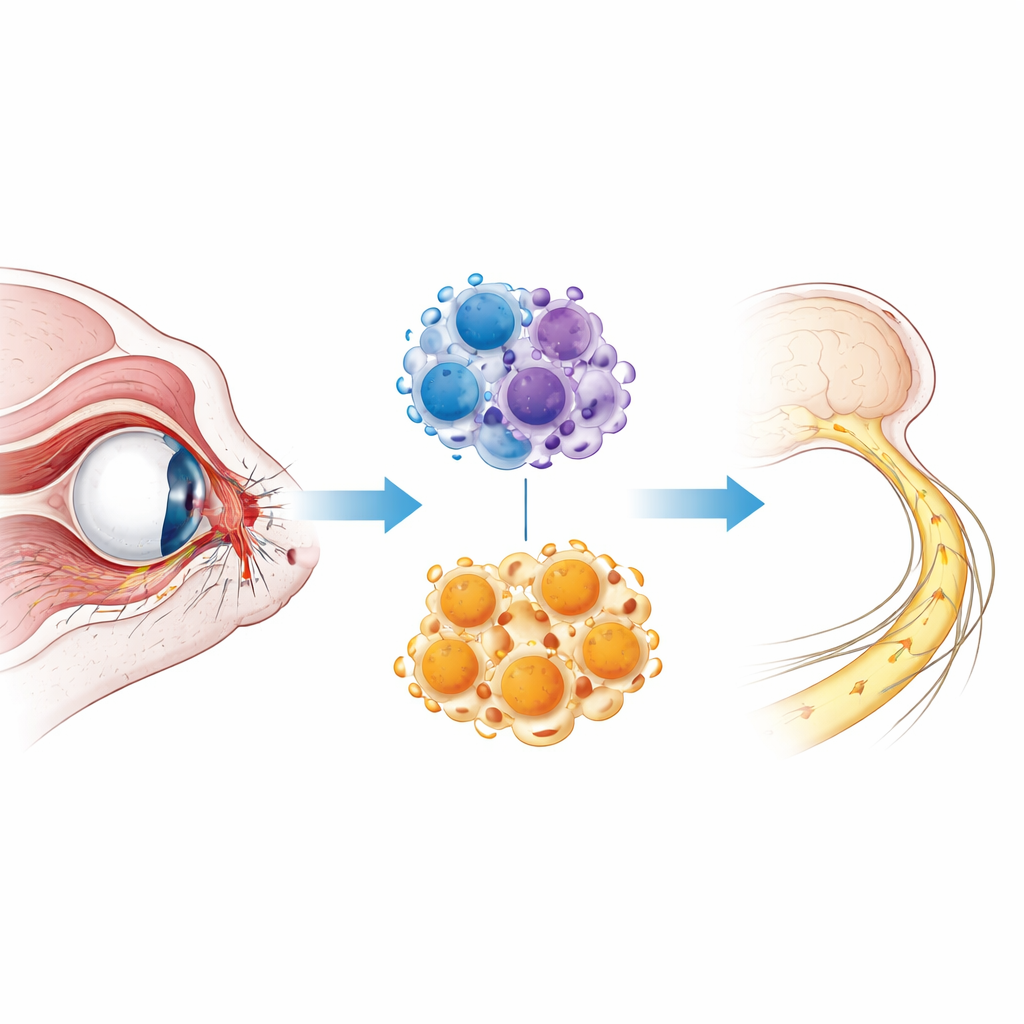
Quand le câblage de l’œil est endommagé
Le nerf optique est un faisceau serré de fibres issues des cellules ganglionnaires rétiniennes, les neurones de sortie de l’œil. Lorsque ce faisceau est écrasé ou étiré lors d’un traumatisme, de nombreuses fibres nerveuses meurent immédiatement, tandis que d’autres dégénèrent lentement sur plusieurs jours à semaines. L’œdème, l’inflammation et l’accumulation de débris cellulaires et de myéline aggravent la lésion et rendent plus difficile la repousse des fibres nerveuses survivantes. Les soins actuels se concentrent sur la stabilisation du patient, car nous manquons encore de moyens pour arrêter cette vague de dégénérescence. Pour étudier ces événements en détail, les chercheurs utilisent souvent un modèle murin dans lequel le nerf optique est brièvement pincé, reproduisant les caractéristiques fondamentales de la neuropathie optique traumatique.
Le pouvoir surprenant des cellules nettoyeuses
Après la blessure, des cellules immunitaires spécialisées appelées microglies et macrophages affluent vers le nerf et la rétine endommagés. Ces « équipes de nettoyage », collectivement désignées sous le terme de cellules myéloïdes, peuvent jouer un rôle ambivalent : elles peuvent alimenter l’inflammation, mais elles peuvent aussi effectuer l’éfferocytose — englober et digérer les cellules mortes et les débris pour permettre la réparation tissulaire. Les auteurs se sont focalisés sur un commutateur moléculaire à l’intérieur de ces cellules, une enzyme appelée HDAC3 qui aide à contrôler l’activation des gènes. Des travaux antérieurs montraient que bloquer HDAC3 directement dans les cellules nerveuses pouvait réduire la mort cellulaire. Ici, l’équipe s’est posé une question différente : que se passe-t-il si HDAC3 est supprimée spécifiquement dans les cellules myéloïdes ?
Basculer les cellules myéloïdes en mode réparation
À l’aide de souris génétiquement modifiées, les chercheurs ont éliminé HDAC3 uniquement dans les cellules myéloïdes en la laissant intacte ailleurs. Après l’écrasement du nerf optique, ces souris ont conservé davantage de neurones rétiniens et ont montré des signaux électriques rétiniens plus forts que les souris normales, indiquant une meilleure fonction visuelle. Elles présentaient également plus de fibres nerveuses en régénération dépassant le site de la lésion. La microscopie a révélé que les cellules myéloïdes dépourvues de HDAC3 étaient plus actives pour engloutir les cellules mourantes dans la rétine et éliminer les débris de myéline du nerf optique. Lorsque des fragments de myéline ont été proposés à des macrophages en culture, les cellules sans HDAC3 ont ingéré beaucoup plus de ce matériel, confirmant que l’enzyme freine normalement leur capacité de nettoyage.
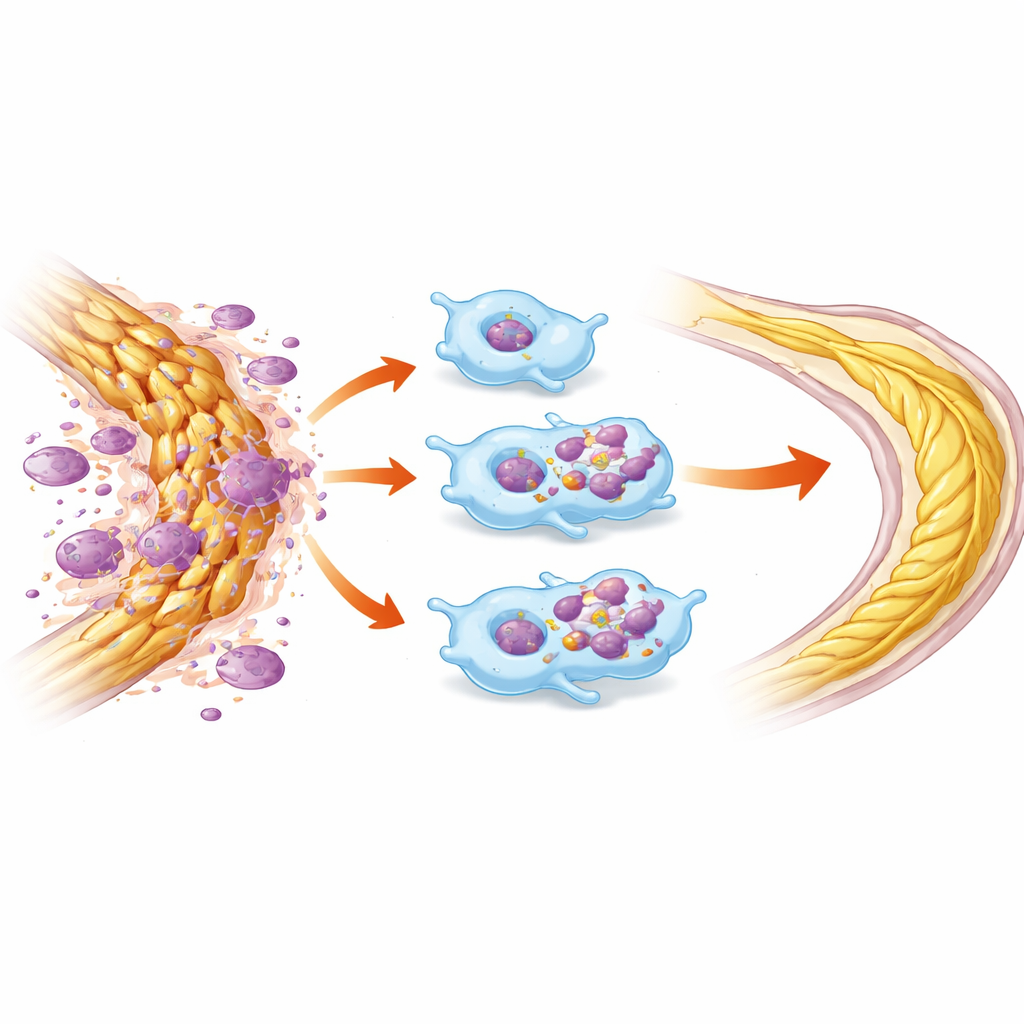
Un récepteur clé favorise l’élimination des débris
Pour comprendre comment HDAC3 contrôle ce comportement, les chercheurs ont examiné des molécules impliquées dans l’éfferocytose. Ils ont constaté que les macrophages déficients en HDAC3 augmentaient la production de MerTK, un récepteur de surface connu pour reconnaître et ingérer les cellules mortes et la myéline, ainsi que des facteurs associés qui favorisent la résolution de l’inflammation. Le blocage de MerTK par un inhibiteur de petite molécule annulait en grande partie l’avantage d’ingestion de myéline, suggérant que la suppression de HDAC3 agit en libérant MerTK et ses partenaires pour fonctionner de manière plus efficace. Fait intéressant, lorsque HDAC3 était supprimée uniquement dans les microglies de longue durée de vie mais pas dans les macrophages infiltrants, l’effet protecteur sur les cellules rétiniennes et la fonction a disparu, désignant les macrophages comme les principaux moteurs de ce programme de réparation dans ce modèle de lésion.
Ce que cela pourrait signifier pour les traitements futurs
En termes simples, ce travail montre que réduire l’activité de HDAC3 dans certaines cellules immunitaires les transforme en agents d’entretien plus efficaces : elles éliminent plus rapidement les cellules mortes et l’isolation des nerfs, apaisent l’inflammation et créent un environnement plus propice à la repousse des fibres du nerf optique endommagées. Bien que des recherches supplémentaires soient nécessaires pour comprendre précisément comment HDAC3 contrôle MerTK et pour concevoir des médicaments sûrs agissant sélectivement sur les cellules myéloïdes, le concept est clair. En apprenant aux équipes de nettoyage de l’organisme à mieux faire leur travail, nous pourrions un jour protéger la vision et favoriser la réparation nerveuse après des blessures graves à l’œil et à la tête.
Citation: Shahror, R.A., Morris, C.A., Cunningham, A. et al. Myeloid HDAC3 deletion protects against traumatic optic injury. Cell Death Discov. 12, 163 (2026). https://doi.org/10.1038/s41420-026-03030-0
Mots-clés: neuropathie optique traumatique, lésion du nerf optique, macrophages, HDAC3, éfferocytose