Clear Sky Science · nl
Verwijdering van HDAC3 in myeloïde cellen beschermt tegen traumatisch optisch letsel
Het gezichtsvermogen beschermen na hoofd- en oogletsel
Stootwonden aan het hoofd of gezicht veroorzaken niet alleen een blauwe plek — ze kunnen ook onopgemerkt schade toebrengen aan de oogzenuw die visuele informatie van het oog naar de hersenen vervoert. Deze aandoening, traumatische optische neuropathie genoemd, leidt vaak tot blijvend verlies van gezichtsvermogen en heeft momenteel geen betrouwbare behandeling. De hier samengevatte studie onderzoekt een nieuwe strategie: het herprogrammeren van bepaalde immuuncellen zodat ze beschadigd weefsel efficiënter opruimen en de oogzenuw helpen zich te herstellen, waardoor het gezichtsvermogen na een verwonding mogelijk behouden kan blijven.
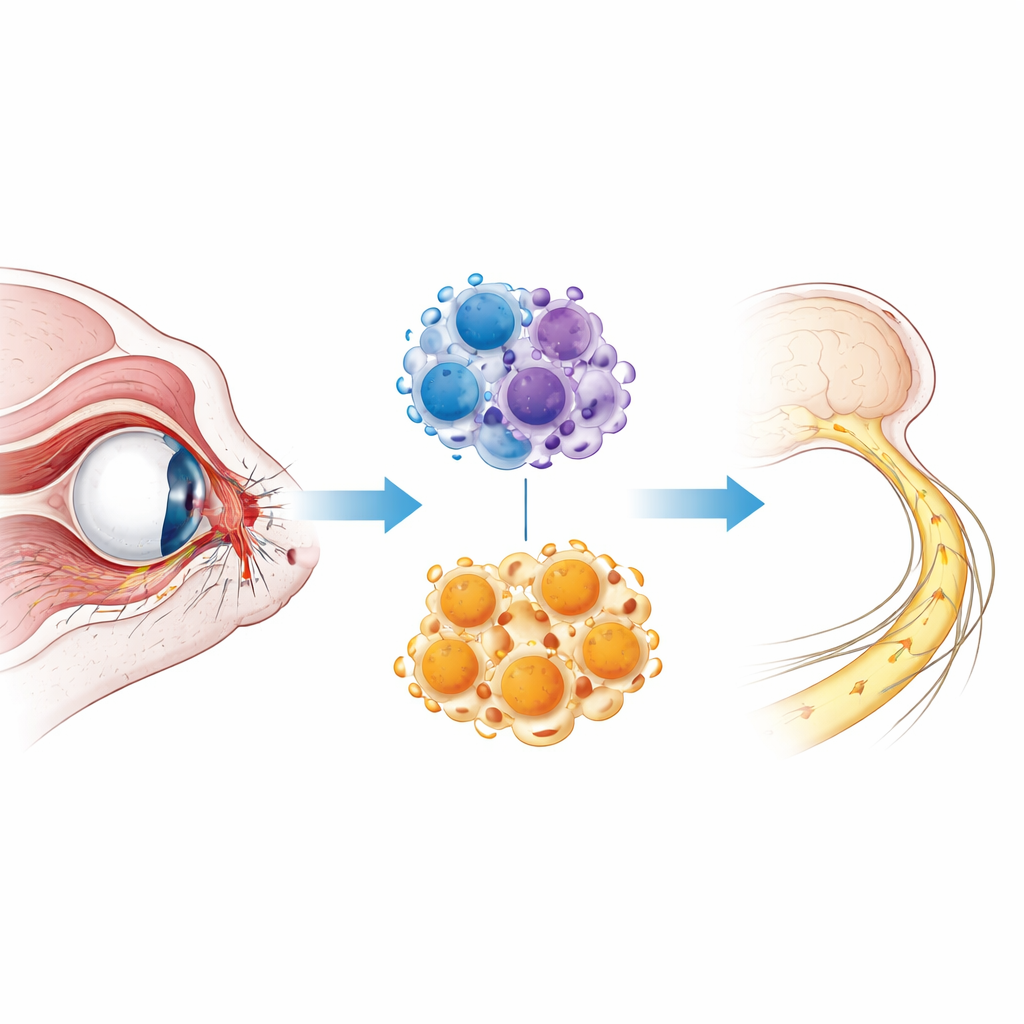
Wanneer de bedrading van het oog beschadigd raakt
De oogzenuw is een compacte bundel vezels van retinale ganglioncellen, de uitvoerende neuronen van het oog. Wanneer deze bundel tijdens een trauma wordt geknepen of uitgerekt, sterven veel van deze zenuwvezels onmiddellijk, terwijl andere langzaam degenereren over dagen tot weken. Zwelling, ontsteking en een ophoping van cellulaire en myeline-debris verergeren het letsel en bemoeilijken het herstel en de herkroning van overlevende vezels. De huidige zorg richt zich op het stabiliseren van de patiënt, omdat we nog altijd geen methoden hebben om deze golf van degeneratie te stoppen. Om deze processen in detail te bestuderen gebruiken wetenschappers vaak een muismodel waarbij de oogzenuw kort wordt geknepen, wat de kernkenmerken van traumatische optische neuropathie nabootst.
De verrassende kracht van opruimcellen
Na een verwonding haasten gespecialiseerde immuuncellen, microglia en macrofagen, zich naar de beschadigde zenuw en het netvlies. Deze "opruimploegen", gezamenlijk bekend als myeloïde cellen, kunnen een dubbelzinnig effect hebben: ze kunnen ontsteking aanwakkeren, maar ze kunnen ook efferocytose uitvoeren — het omhullen en verteren van dode cellen en debris zodat het weefsel kan genezen. De onderzoekers richtten zich op een moleculaire schakelaar in deze cellen, een enzym genaamd HDAC3 dat helpt bepalen welke genen aan- of uitgezet worden. Eerder werk toonde aan dat het blokkeren van HDAC3 direct in zenuwcellen celsterfte kan verminderen. Hier stelden de onderzoekers een andere vraag: wat gebeurt er als HDAC3 specifiek uit myeloïde cellen wordt verwijderd?
Myeloïde cellen overschakelen naar herstelmodus
Met behulp van genetisch gemodificeerde muizen verwijderden de wetenschappers HDAC3 alleen in myeloïde cellen, terwijl het elders intact bleef. Na het kneuzen van de oogzenuw behielden deze muizen meer retinale neuronen en vertoonden ze sterkere elektrische signalen uit het netvlies vergeleken met normale muizen, wat duidt op beter visueel functioneren. Ze hadden ook meer zenuwvezels die voorbij de letselplek groeiden. Microscopie toonde dat myeloïde cellen zonder HDAC3 actiever waren in het opnemen van stervende cellen in het netvlies en in het opruimen van myeline-debris uit de oogzenuw. Wanneer myelineschilfers aan macrofagen in een kweek werden aangeboden, slikten cellen zonder HDAC3 veel meer van dit materiaal, wat bevestigt dat het enzym normaal gesproken hun opruimcapaciteit remt.
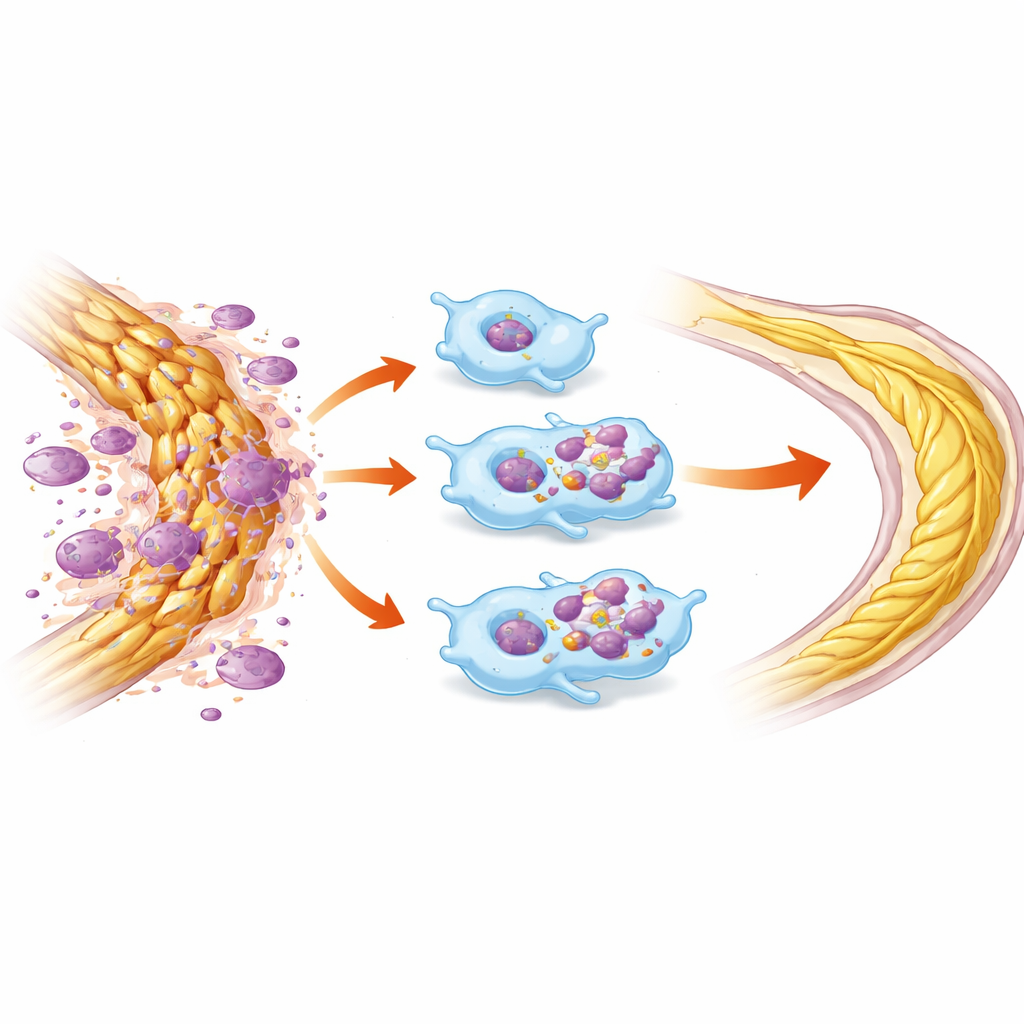
Een belangrijke receptor helpt bij het opruimen van debris
Om te begrijpen hoe HDAC3 dit gedrag reguleert, onderzochten de onderzoekers moleculen die bij efferocytose betrokken zijn. Ze vonden dat HDAC3-deficiënte macrofagen de productie van MerTK verhoogden, een oppervlaktereceptor die dode cellen en myeline herkent en opneemt, samen met gerelateerde factoren die de resolutie van ontsteking bevorderen. Het blokkeren van MerTK met een kleinmolecuulremmer maakte het voordeel in myeline-opname grotendeels ongedaan, wat suggereert dat het verwijderen van HDAC3 helpt door MerTK en zijn partners sterker te laten werken. Interessant was dat, wanneer HDAC3 alleen uit de langlevende microglia maar niet uit binnenvallende macrofagen werd verwijderd, het beschermende effect op retinale cellen en functie verdween, wat wijst op macrofagen als de belangrijkste aanjagers van dit herstelprogramma in dit letselmodel.
Wat dit kan betekenen voor toekomstige behandelingen
In eenvoudige bewoordingen toont dit werk aan dat het terugschakelen van HDAC3 in bepaalde immuuncellen ze verandert in efficiëntere huismeesters: ze ruimen dode cellen en zenuwisolatie sneller op, temperen ontsteking en creëren een gunstiger omgeving voor beschadigde oogzenuwvezels om opnieuw te groeien. Hoewel meer onderzoek nodig is om precies te begrijpen hoe HDAC3 MerTK aanstuurt en om veilige medicijnen te ontwerpen die selectief op myeloïde cellen werken, is het concept helder. Door de eigen opruimploegen van het lichaam beter te leren werken, kunnen we mogelijk op een dag het gezichtsvermogen beschermen en zenuwherstel bevorderen na verwoestende oog- en hoofdletsel.
Bronvermelding: Shahror, R.A., Morris, C.A., Cunningham, A. et al. Myeloid HDAC3 deletion protects against traumatic optic injury. Cell Death Discov. 12, 163 (2026). https://doi.org/10.1038/s41420-026-03030-0
Trefwoorden: traumatische optische neuropathie, letsel van de oogzenuw, macrofagen, HDAC3, efferocytose