Clear Sky Science · de
Myeloide HDAC3-Deletion schützt vor traumatischen Sehnervenverletzungen
Sehschutz nach Kopf- und Augenverletzungen
Stumpfe Schläge gegen Kopf oder Gesicht erzeugen nicht nur Prellungen – sie können stillschweigend den Sehnerv schädigen, der visuelle Informationen vom Auge zum Gehirn leitet. Diese Erkrankung, traumatische optische Neuropathie genannt, führt häufig zu bleibendem Sehverlust und ist derzeit nicht zuverlässig behandelbar. Die hier zusammengefasste Studie untersucht eine neue Strategie: bestimmte Immunzellen so umzuprogrammieren, dass sie Schäden effizienter beseitigen und dem Sehnerv bei der Reparatur helfen, wodurch das Sehvermögen nach einer Verletzung erhalten werden könnte.
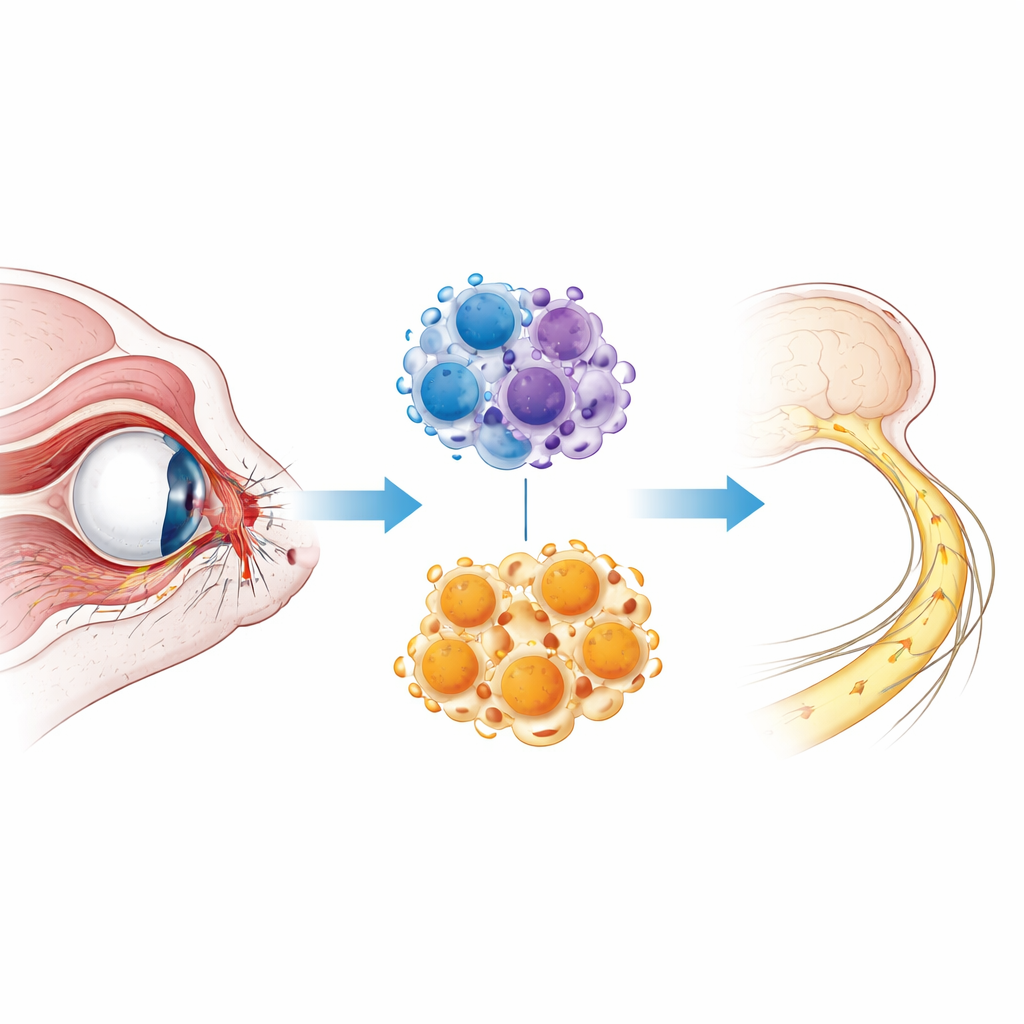
Wenn die Verschaltung des Auges verletzt ist
Der Sehnerv ist ein dichtes Bündel von Fasern der retinalen Ganglienzellen, den Ausgangsneuronen des Auges. Wird dieses Bündel bei einem Trauma gequetscht oder gedehnt, sterben viele dieser Nervenfasern sofort, andere degenerieren langsam über Tage bis Wochen. Schwellungen, Entzündungen und die Anhäufung von zellulären und Myelin-Trümmern verschlimmern die Schädigung und erschweren das Nachwachsen überlebender Fasern. Die bisherige Versorgung konzentriert sich auf die Stabilisierung der Patientinnen und Patienten, weil wir noch keine Möglichkeiten haben, diese Degenerationswelle aufzuhalten. Um diese Vorgänge detailliert zu untersuchen, verwenden Wissenschaftler oft ein Mausmodell, bei dem der Sehnerv kurzzeitig eingeklemmt wird und so die zentralen Merkmale der traumatischen Optikusneuropathie nachbildet.
Die überraschende Kraft der Aufräumzellen
Nach einer Verletzung strömen spezialisierte Immunzellen, sogenannte Mikroglia und Makrophagen, zum geschädigten Nerv und zur Netzhaut. Diese „Aufräumtrupps“, zusammengefasst als myeloide Zellen, sind zweischneidig: Sie können Entzündungen anheizen, aber sie können auch Efferocytose ausführen – das Aufnehmen und Verdauen abgestorbener Zellen und Trümmer, sodass Gewebe heilen kann. Die Forscher richteten ihr Augenmerk auf einen molekularen Schalter in diesen Zellen, ein Enzym namens HDAC3, das mitsteuert, welche Gene ein- oder ausgeschaltet werden. Frühere Arbeiten zeigten, dass die Blockade von HDAC3 direkt in Nervenzellen den Zelltod verringern kann. Hier stellten die Autorinnen und Autoren eine andere Frage: Was passiert, wenn HDAC3 speziell in myeloiden Zellen entfernt wird?
Myeloide Zellen in den Reparaturmodus schalten
Mit genetisch veränderten Mäusen entfernten die Wissenschaftler HDAC3 nur in myeloiden Zellen, während es sonst erhalten blieb. Nach einer Sehnervenquetschung behielten diese Mäuse mehr retinale Neurone und zeigten stärkere elektrische Signale aus der Netzhaut im Vergleich zu normalen Mäusen, was auf eine bessere visuelle Funktion hindeutet. Zudem wuchsen mehr regenerierende Nervenfasern am Verletzungsbereich vorbei. Die Mikroskopie zeigte, dass myeloide Zellen ohne HDAC3 aktiver darin waren, sterbende Zellen in der Netzhaut zu verschlingen und Myelin-Trümmer aus dem Sehnerv zu entfernen. Als Makrophagen im Reagenzglas Mylinfragmente angeboten wurden, fraßen Zellen ohne HDAC3 deutlich mehr von diesem Material, was bestätigt, dass das Enzym normalerweise ihre Aufräumfähigkeit bremst.
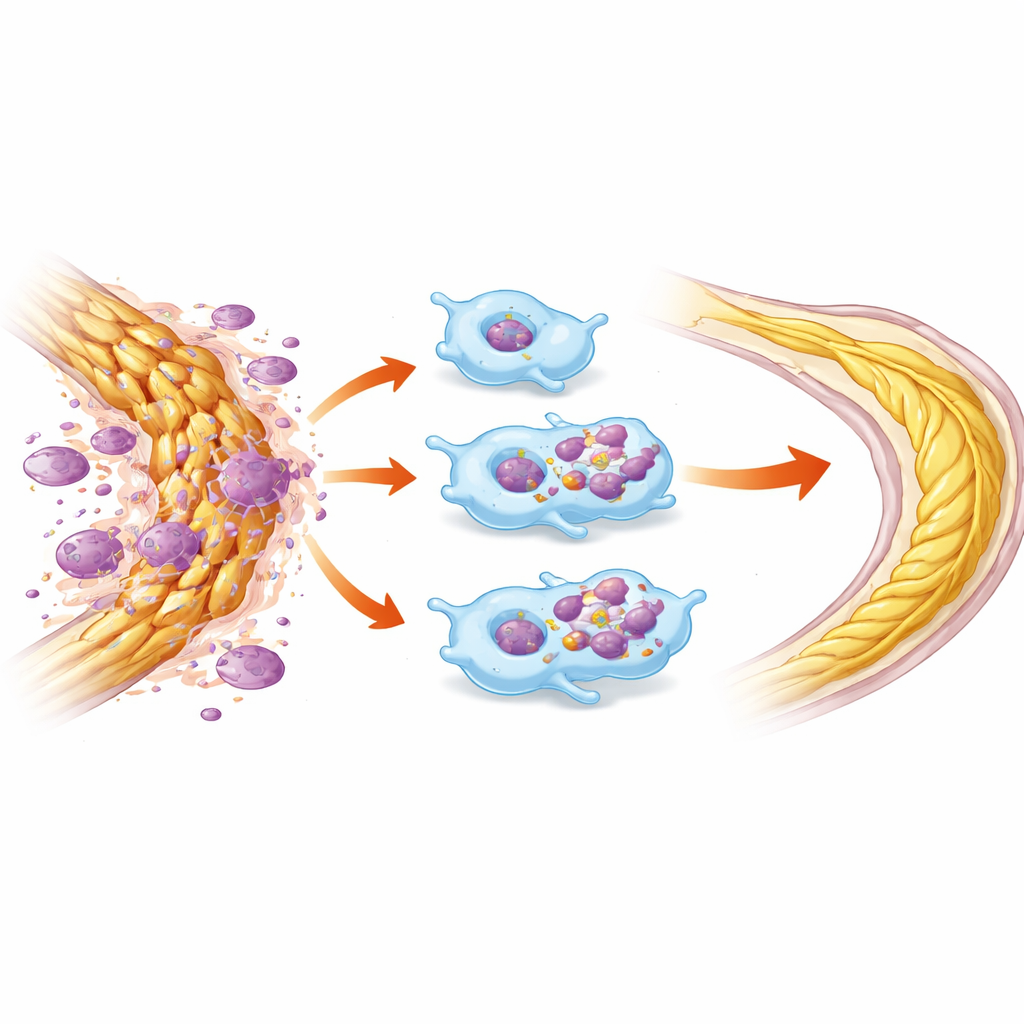
Ein Schlüsselrezeptor fördert die Trümmerbeseitigung
Um zu verstehen, wie HDAC3 dieses Verhalten steuert, untersuchten die Forschenden Moleküle, die an der Efferocytose beteiligt sind. Sie fanden, dass HDAC3-defiziente Makrophagen die Produktion von MerTK erhöhten, einem Oberflächenrezeptor, der dafür bekannt ist, tote Zellen und Myelin zu erkennen und aufzunehmen, zusammen mit verwandten Faktoren, die die Auflösung von Entzündungen fördern. Das Blockieren von MerTK mit einem kleinen Molekülinhibitor tilgte weitgehend den Vorteil bei der Myelinaufnahme, was darauf hindeutet, dass die HDAC3-Deletion hilft, indem sie MerTK und seine Partner stärker zur Wirkung kommen lässt. Interessanterweise verschwand der schützende Effekt auf Retinazellen und Funktion, wenn HDAC3 nur in langlebigen Mikroglia, jedoch nicht in einströmenden Makrophagen entfernt wurde – das deutet darauf hin, dass Makrophagen in diesem Verletzungsmodell die Haupttreiber dieses Reparaturprogramms sind.
Was das für künftige Therapien bedeuten könnte
Kurz gesagt zeigt diese Arbeit, dass das Herunterregeln von HDAC3 in bestimmten Immunzellen sie zu effizienteren Reinigungskräften macht: Sie räumen tote Zellen und Nervenisolierung schneller weg, dämpfen Entzündungen und schaffen ein günstigeres Umfeld für das Nachwachsen geschädigter Sehnervenfasern. Obwohl weitere Forschung nötig ist, um genau zu verstehen, wie HDAC3 MerTK steuert und wie man sichere Wirkstoffe entwickelt, die selektiv auf myeloide Zellen wirken, ist das Konzept klar. Indem man die körpereigenen Aufräumtrupps besser arbeiten lehrt, könnten wir eines Tages das Sehen schützen und die Nervenreparatur nach schweren Augen- und Kopfverletzungen fördern.
Zitation: Shahror, R.A., Morris, C.A., Cunningham, A. et al. Myeloid HDAC3 deletion protects against traumatic optic injury. Cell Death Discov. 12, 163 (2026). https://doi.org/10.1038/s41420-026-03030-0
Schlüsselwörter: traumatische optische Neuropathie, Sehnervenverletzung, Makrophagen, HDAC3, Efferocytose