Clear Sky Science · ru
Лигаза убиквитина Deltex E3 2 усиливает STING-опосредованный ответ типа I интерферона через связывание K63-цепочками убиквитина
Как клетки распознают опасную ДНК
Наш организм постоянно ищет вирусных захватчиков и сбившиеся с пути опухолевые клетки. Одной из ключевых систем тревоги для этой ранней защиты является белок STING, который обнаруживает чужеродную ДНК в неподходящем месте внутри клеток и запускает мощные противовирусные и противоопухолевые ответы. В этой работе описан ранее недооценённый вспомогательный белок DTX2, который действует как молекулярный усилитель для STING, делая эту систему сигнализации громче и эффективнее против инфекций и опухолей.
Клеточная сигнализация о присутствии ДНК
Когда проникают вирусы, такие как вирус простого герпеса, или повреждённые клетки выплёскивают свою ДНК, фрагменты двуспиральной ДНК появляются в тех местах внутри клетки, где их не должно быть. Сенсорный фермент cGAS распознаёт эту постороннюю ДНК и вырабатывает небольшой сигнальный молекулу, которая активирует STING — белок, находящийся на внутренних мембранах. После активации STING перемещается в другой компартмент, известный как аппарат Гольджи, и запускает каскад сигналов, который в итоге приводит к выработке интерферонов типа I и провоспалительных молекул. Эти вещества действуют как химические сирены, привлекая и активируя иммунные клетки для борьбы с вирусами и во многих случаях для распознавания и атаки опухолей. 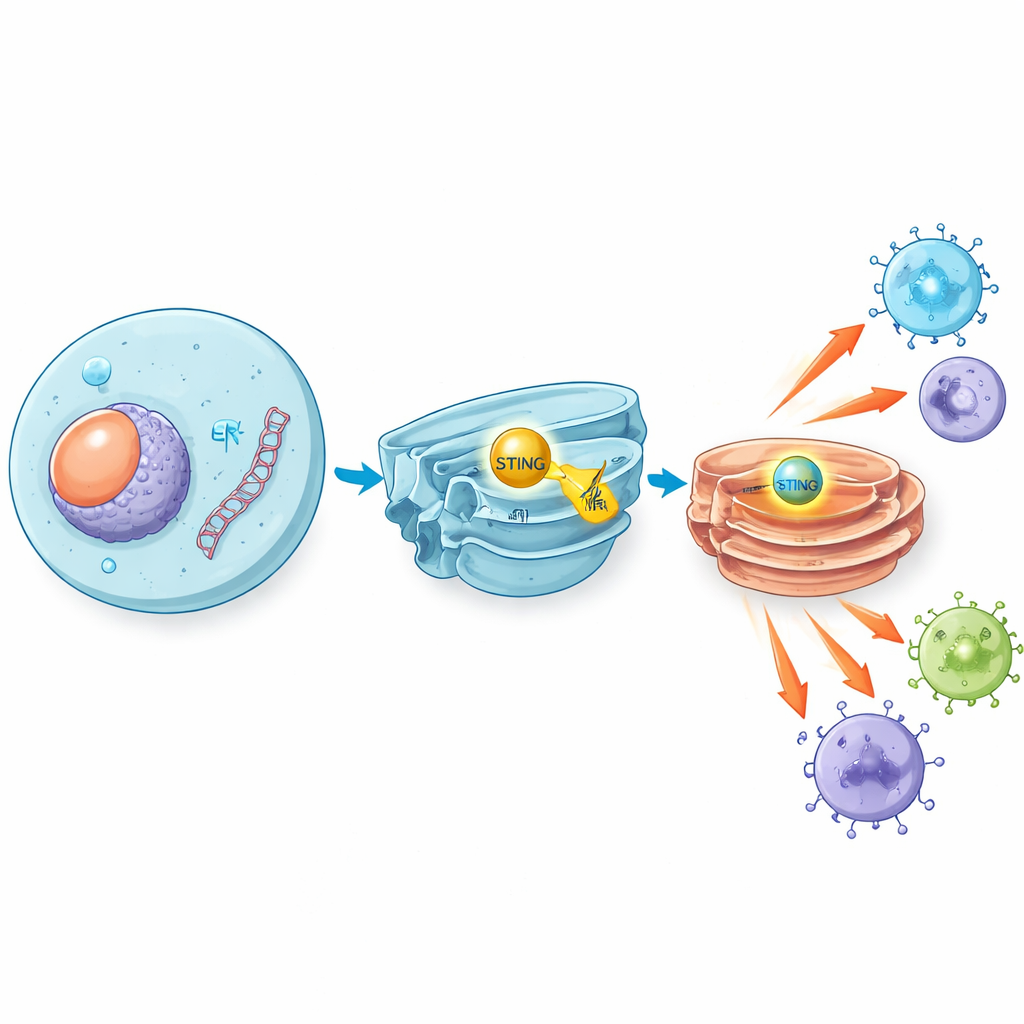
Открытие нового помощника для пути STING
Чтобы выяснить, какие ферменты могут тонко регулировать эту систему тревоги, исследователи инфицировали иммунные клетки мышей вирусом герпеса и измеряли, какие гены усилили или ослабили свою экспрессию. Среди сотен ферментов выделился один: DTX2, E3-лигаза убиквитина, то есть белок, способный прикреплять маленькие цепочки убиквитина к другим белкам и изменять их поведение. Учёные получили мышей с удалённым геном Dtx2 и обнаружили, что их иммунные клетки вырабатывают значительно меньше интерферона и противовирусных сигналов при воздействии вирусной ДНК, синтетической ДНК или прямого активатора STING. Это снижение наблюдалось не только в иммунных клетках, таких как макрофаги, но и в неиммунных клетках, и было специфично для ответов, вызванных ДНК, а не РНК-вирусами, что указывает на целенаправленную роль DTX2 в пути распознавания ДНК.
Как DTX2 усиливает сигнал STING
Вскрыв механизм, учёные показали, что DTX2 физически связывается со STING и добавляет к нему особую форму убиквитиновых цепочек, известную как K63-связанные цепочки, на двух конкретных участках STING. В отличие от других меток убиквитина, направляющих белки на разрушение, эти цепочки действуют скорее как функциональные модификаторы, меняющие локализацию белка и его сигнализацию. При отсутствии DTX2 уровень STING оставался нормальным, но его способность перемещаться от исходной мембраны к аппарату Гольджи и привлекать следующий сигнальный фермент TBK1 была значительно снижена. Команда определила два ключевых аминокислотных остатка на STING — K236 и K370 — как точки присоединения этих цепочек. При мутациях в этих местах, препятствующих формированию цепочек, STING не мог правильно перемещаться, TBK1 не эффективно привлекался, и последующий интерфероновый ответ был подавлен.
Защита от вирусов и поддержка противораковой иммунности
Последствия такого молекулярного усиления были очевидны в животных. Мыши без Dtx2 более легко поддавались инфекции вирусом герпеса, демонстрировали более тяжёлые повреждения лёгких, более высокие вирусные нагрузки в нескольких органах и более низкие уровни защитных интерферонов и провоспалительных сигналов в крови. В моделях рака картина была обратной: более высокие уровни DTX2 коррелировали с более выраженными сигнатурами интерферонов типа I и повышенным инфильтрированием ключевых иммунных эффекторов, таких как дендритные клетки, цитотоксические Т-клетки и естественные киллеры, в анализах данных человека. В мышиных моделях рака головы и шеи опухоли, генетически модифицированные для повышенной экспрессии DTX2, лучше реагировали на препарат-активатор STING и на иммунотерапию блокаторами контрольных точек, уменьшаясь в размерах и содержащие больше иммунных клеток по сравнению с контрольными опухолями. 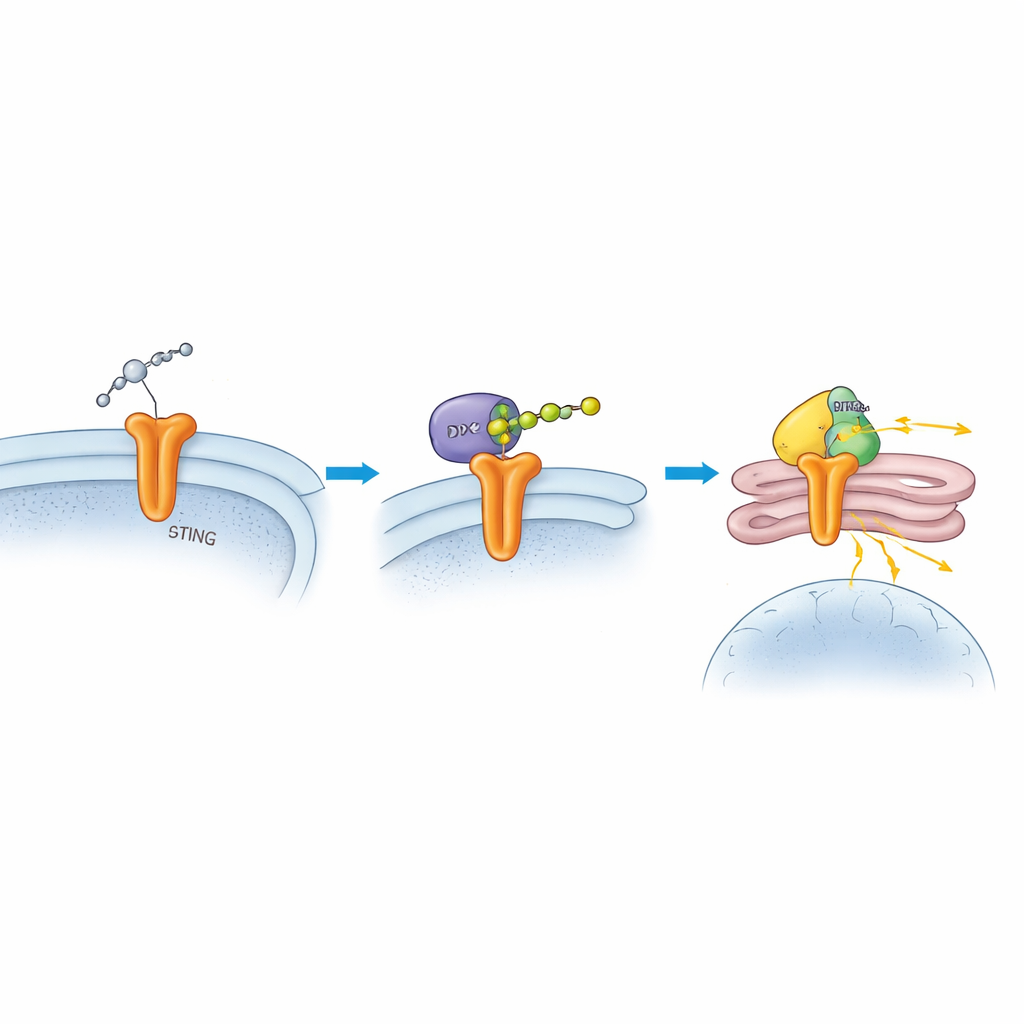
Почему этот молекулярный усилитель важен
Для неспециалиста главное послание состоит в том, что DTX2 функционирует как критический усилитель одного из самых ранних сигналов системы иммунитета. Украшая STING подходящими молекулярными метками в нужных местах, DTX2 помогает STING добраться до нужной внутриклеточной локализации и полностью включить противовирусные и противоопухолевые защиты. При отсутствии DTX2 или блокировке его действия сигнал ослабляется: вирусы распространяются легче, а опухолям может быть проще уклоняться от иммунной атаки. Это делает DTX2 перспективной целью для новых терапий, которые могли бы усилить наши естественные механизмы защиты от инфекций и повысить эффективность иммунотерапии рака.
Цитирование: Liu, Z., Li, R., Fan, C. et al. Deltex E3 ubiquitin ligase 2 potentiates STING-mediated type I interferon response by K63-linked ubiquitination. Cell Death Dis 17, 424 (2026). https://doi.org/10.1038/s41419-026-08659-4
Ключевые слова: врожденный иммунитет, путь STING, сигнализация интерферонов, иммунотерапия рака, вирусная инфекция