Clear Sky Science · fr
La ligase E3 Deltex 2 potentialise la réponse interferon de type I médiée par STING par ubiquitination liée en K63
Comment les cellules détectent l’ADN dangereux
Nos organismes sont constamment à l’affût des envahisseurs viraux et des cellules tumorales indésirables. L’un des systèmes d’alarme clés de cette défense précoce est une protéine appelée STING, qui détecte l’ADN errant au mauvais endroit à l’intérieur des cellules et déclenche de puissantes réponses antivirales et antitumorales. Cet article met en lumière une protéine d’assistance jusque-là négligée, DTX2, qui agit comme un amplificateur moléculaire pour STING, rendant ce système d’alarme plus fort et plus efficace contre les infections et les tumeurs.
Une alarme anti-intrus pour l’ADN
Lorsque des virus tels que l’herpès simplex envahissent, ou lorsque des cellules endommagées libèrent leur ADN, des fragments d’ADN double brin apparaissent là où ils n’ont rien à faire à l’intérieur de nos cellules. Une enzyme détectrice appelée cGAS reconnaît cet ADN errant et produit une petite molécule messagère qui active STING, une protéine localisée sur une membrane interne. Une fois activé, STING se déplace vers un autre compartiment connu sous le nom d’appareil de Golgi et déclenche une cascade de signalisation qui aboutit à la production d’interférons de type I et de molécules inflammatoires. Ces substances font office de sirènes chimiques, alertant et activant les cellules immunitaires pour combattre les virus et, dans de nombreux cas, reconnaître et attaquer les tumeurs. 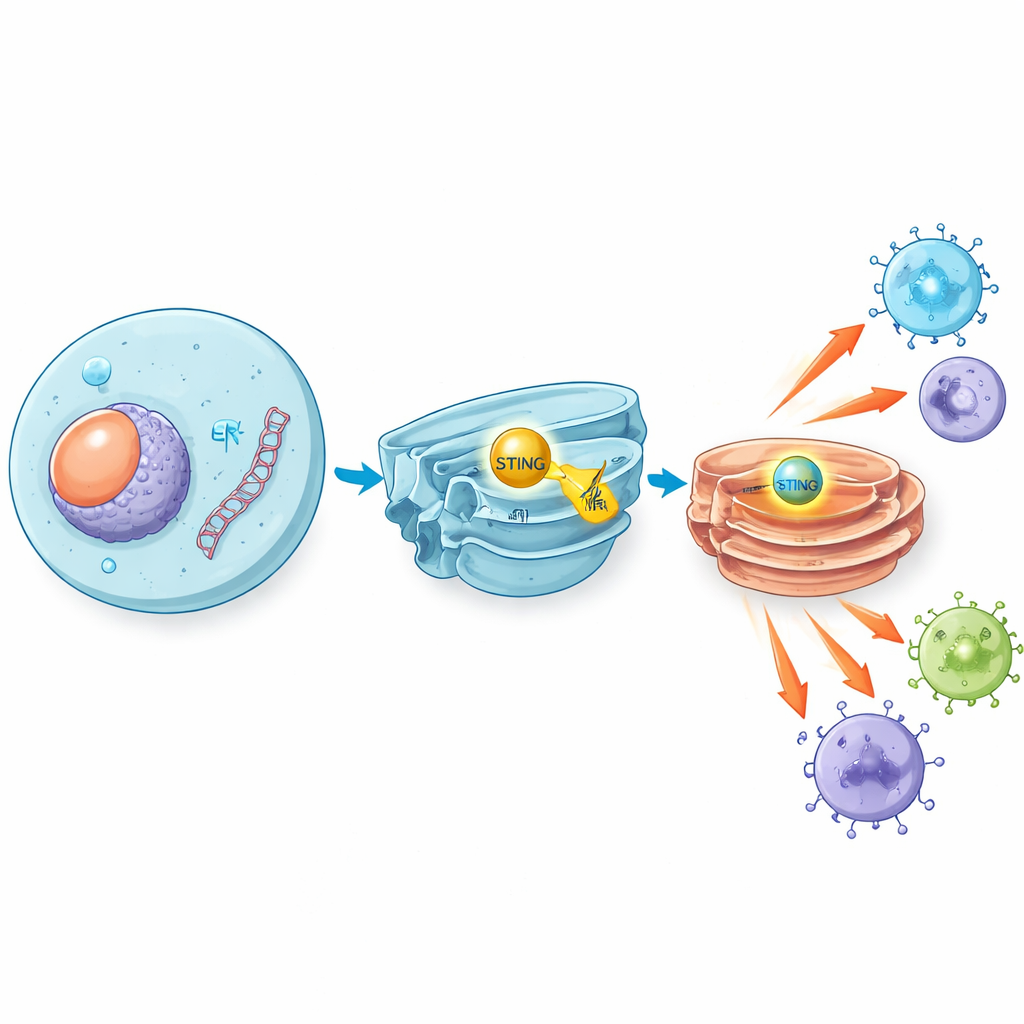
Découverte d’un nouvel assistant pour la voie STING
Pour identifier les enzymes susceptibles d’ajuster ce système d’alarme de l’ADN, les chercheurs ont infecté des cellules immunitaires de souris par l’herpès et mesuré les gènes dont l’expression variait. Parmi des centaines d’enzymes, une a émergé : DTX2, une ligase ubiquitine E3, c’est‑à‑dire capable d’ajouter de petites chaînes d’ubiquitine à d’autres protéines pour modifier leur comportement. L’équipe a généré des souris dépourvues du gène Dtx2 et a constaté que leurs cellules immunitaires produisaient beaucoup moins d’interféron et d’autres signaux antiviraux lorsqu’elles étaient exposées à de l’ADN viral, à de l’ADN synthétique ou à un activateur direct de STING. Cette baisse a été observée non seulement dans les cellules immunitaires comme les macrophages, mais aussi dans des cellules non immunitaires, et elle était spécifique aux réponses déclenchées par l’ADN plutôt qu’aux virus à ARN, ce qui indique un rôle ciblé de DTX2 dans la voie de détection de l’ADN.
Comment DTX2 renforce le signal STING
En creusant davantage, les scientifiques ont montré que DTX2 se lie physiquement à STING et ajoute une forme particulière de chaînes d’ubiquitine, connues sous le nom de chaînes liées en K63, sur deux sites spécifiques de STING. Contrairement à d’autres étiquettes ubiquitine qui marquent les protéines pour leur destruction, ces chaînes agissent plutôt comme des modificateurs fonctionnels qui changent la localisation d’une protéine et la manière dont elle signale. En l’absence de DTX2, les niveaux de STING restaient normaux, mais sa capacité à migrer de sa membrane d’origine vers le Golgi et à recruter l’enzyme de signalisation suivante, TBK1, était fortement réduite. L’équipe a identifié deux acides aminés clés sur STING, K236 et K370, comme points d’attachement pour ces chaînes. Lorsqu’ils ont muté ces sites de manière à empêcher la formation des chaînes, STING n’a pas pu se déplacer correctement, TBK1 n’a pas été recruté efficacement, et la réponse en interféron en aval a été atténuée.
Protection contre les virus et soutien à l’immunité anticancéreuse
Les conséquences de ce réglage moléculaire étaient visibles in vivo. Les souris dépourvues de Dtx2 succombaient plus facilement à l’infection par l’herpès, présentaient des lésions pulmonaires plus sévères, des charges virales plus élevées dans plusieurs organes, et des niveaux plus faibles d’interférons protecteurs et de signaux inflammatoires dans le sang. Dans des modèles de cancer, le phénomène s’inverse : des niveaux élevés de DTX2 étaient associés à des signatures renforcées d’interféron de type I et à une infiltration accrue de cellules immunitaires clés telles que les cellules dendritiques, les lymphocytes T cytotoxiques et les cellules NK dans des jeux de données tumoraux humains. Dans des modèles de cancer de la tête et du cou chez la souris, des tumeurs génétiquement modifiées pour surexprimer DTX2 répondaient mieux à un médicament activateur de STING et à une immunothérapie par inhibiteur de checkpoints, rétrécissant davantage et contenant plus de cellules immunitaires que les tumeurs témoins. 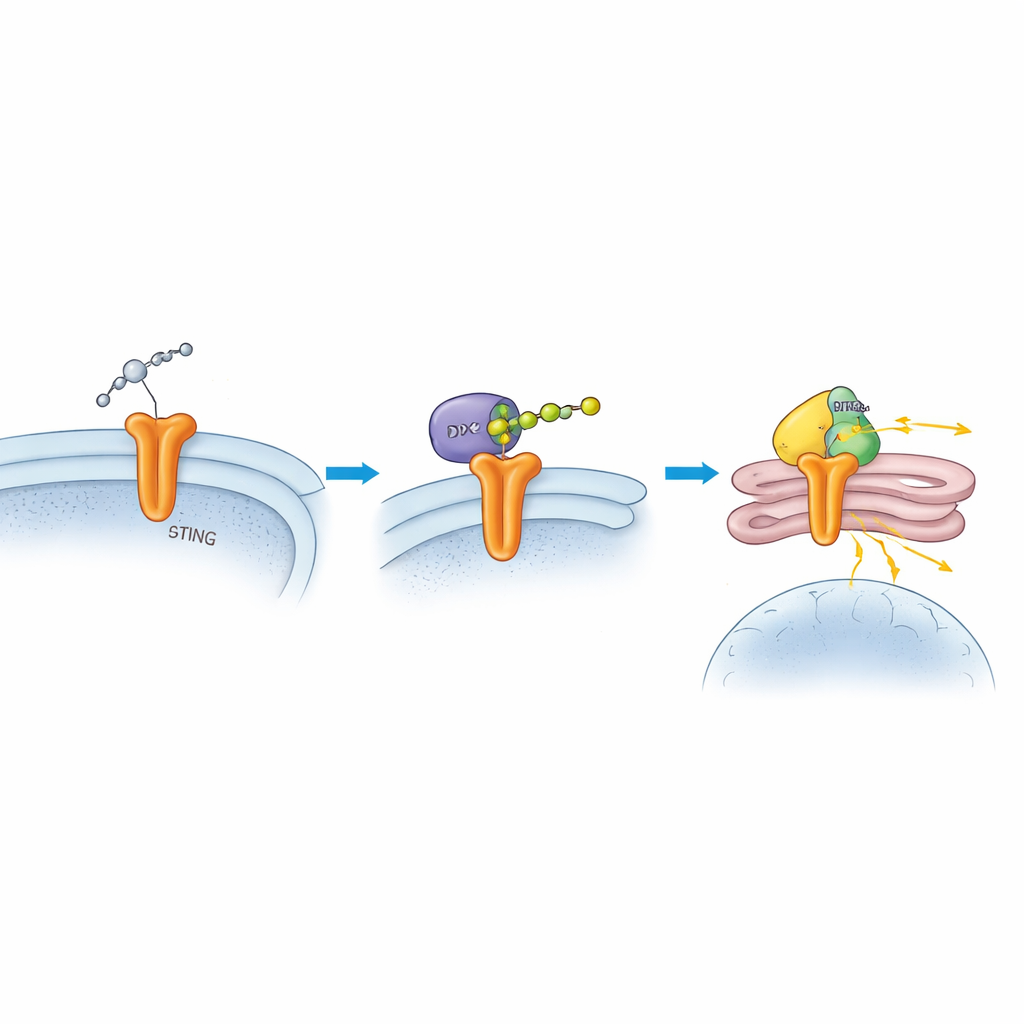
Pourquoi cet amplificateur moléculaire est important
Pour un non-spécialiste, le message principal est que DTX2 agit comme un amplificateur crucial d’une des voies d’alerte les plus précoces du système immunitaire. En décorant STING avec le bon type d’étiquettes moléculaires aux endroits appropriés, DTX2 aide STING à se rendre là où il doit être dans la cellule et à activer pleinement les défenses antivirales et antitumorales. Lorsque DTX2 est absent ou que son action est bloquée, l’alarme est étouffée : les virus se propagent plus facilement et les tumeurs peuvent mieux échapper à l’attaque immunitaire. Cela fait de DTX2 une cible prometteuse pour de nouvelles thérapies pouvant renforcer nos défenses naturelles contre les infections et améliorer le succès des immunothérapies anticancéreuses.
Citation: Liu, Z., Li, R., Fan, C. et al. Deltex E3 ubiquitin ligase 2 potentiates STING-mediated type I interferon response by K63-linked ubiquitination. Cell Death Dis 17, 424 (2026). https://doi.org/10.1038/s41419-026-08659-4
Mots-clés: immunité innée, voie STING, signalisation par interféron, immunothérapie du cancer, infection virale