Clear Sky Science · es
La ligasa de ubiquitina Deltex E3 2 potencia la respuesta de interferón tipo I mediada por STING mediante ubiquitinación enlazada a K63
Cómo las células detectan el ADN peligroso
Nuestros cuerpos están constantemente vigilando la presencia de virus invasores y de células tumorales descontroladas. Uno de los sistemas de alarma clave de esta defensa temprana es una proteína llamada STING, que detecta ADN fuera de lugar dentro de las células y desencadena potentes respuestas antivirales y anticancerígenas. Este artículo descubre una proteína auxiliar previamente desapercibida, DTX2, que actúa como un potenciador molecular de STING, haciendo que este sistema de alarma sea más fuerte y eficaz contra infecciones y tumores.
Una alarma celular contra el ADN
Cuando virus como el herpes simple invaden, o cuando las células dañadas liberan su ADN, fragmentos de ADN de doble hebra aparecen donde no deben dentro de nuestras células. Una enzima sensora llamada cGAS detecta este ADN errante y produce una pequeña molécula mensajera que activa a STING, una proteína situada en una membrana interna. Una vez activado, STING se desplaza a otro compartimento conocido como el aparato de Golgi y desencadena una cascada de señalización que culmina con la producción de interferones tipo I y moléculas inflamatorias. Estas sustancias actúan como sirenas químicas, alertando y activando a las células inmunitarias para combatir virus y, en muchos casos, reconocer y atacar tumores. 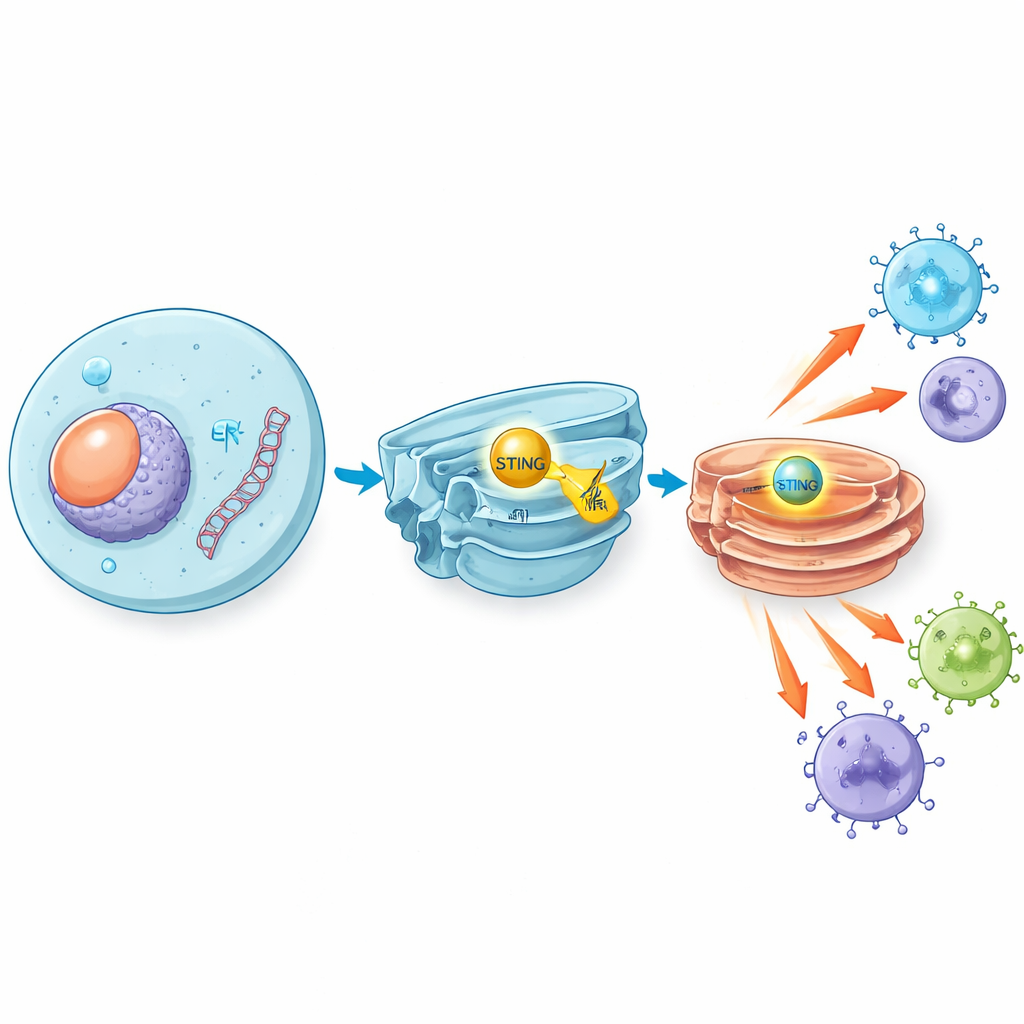
Descubriendo un nuevo ayudante para la vía STING
Para identificar qué enzimas podrían ajustar este sistema de alarma ante el ADN, los investigadores infectaron células inmunes de ratón con el virus del herpes y midieron qué genes aumentaban o disminuían su expresión. Entre cientos de enzimas, una destacó: DTX2, una ligasa E3 de ubiquitina, lo que significa que puede añadir pequeñas cadenas de ubiquitina a otras proteínas para modificar su comportamiento. El equipo generó ratones carentes del gen Dtx2 y observó que sus células inmunes producían mucho menos interferón y menos señales antivirales cuando se exponían a ADN viral, ADN sintético o a un activador directo de STING. Esta disminución se observó no solo en células inmunes como los macrófagos, sino también en células no inmunes, y fue específica de las respuestas desencadenadas por ADN en lugar de virus de ARN, lo que apunta a un papel focalizado de DTX2 en la vía de detección del ADN.
Cómo DTX2 ajusta la señal de STING
Al profundizar, los científicos demostraron que DTX2 se une físicamente a STING y añade una forma particular de cadena de ubiquitina, conocida como cadenas enlazadas a K63, en dos sitios específicos de STING. A diferencia de otras marcas de ubiquitina que dirigen proteínas a la degradación, estas cadenas actúan más bien como modificaciones funcionales que cambian la localización de una proteína y cómo señaliza. Cuando faltaba DTX2, los niveles totales de STING se mantenían normales, pero su capacidad para desplazarse desde su membrana de origen al aparato de Golgi y reclutar la siguiente enzima de señalización, TBK1, se vio muy reducida. El equipo identificó dos aminoácidos clave en STING, K236 y K370, como los puntos de unión para estas cadenas. Cuando mutaron estos sitios para impedir la formación de las cadenas, STING no viajó correctamente, TBK1 no fue reclutado de forma eficiente y la respuesta de interferón aguas abajo se vio atenuada.
Protección frente a virus y apoyo a la inmunidad antitumoral
Las consecuencias de este ajuste molecular fueron claras en animales vivos. Los ratones sin Dtx2 sucumbieron más fácilmente a la infección por el virus del herpes, mostraron daños pulmonares más graves, cargas virales mayores en varios órganos y niveles más bajos de interferones protectores y señales inflamatorias en sangre. En modelos de cáncer, la historia fue la contraria: niveles más altos de DTX2 se asociaron con firmas de interferón tipo I más fuertes e incremento de la infiltración de células inmunitarias clave como células dendríticas, linfocitos T citotóxicos y células NK en conjuntos de datos tumorales humanos. En modelos murinos de cáncer de cabeza y cuello, los tumores diseñados para expresar más DTX2 respondieron mejor a un fármaco activador de STING y a terapia con inhibidores de puntos de control inmunitario, reduciéndose más y albergando más células inmunes que los tumores control.
Por qué importa este potenciador molecular
Para un no especialista, el mensaje principal es que DTX2 actúa como un amplificador crucial de una de las vías de aviso más tempranas del sistema inmunitario. Al decorar a STING con el tipo adecuado de marcas moleculares en los lugares apropiados, DTX2 ayuda a que STING se desplace a donde debe estar dentro de la célula y active plenamente las defensas antivirales y antitumorales. Cuando DTX2 está ausente o su acción está bloqueada, la alarma se atenúa: los virus se propagan con mayor facilidad y los tumores pueden encontrar más opciones para evadir el ataque inmunitario. Esto convierte a DTX2 en un objetivo prometedor para nuevas terapias que podrían potenciar nuestras defensas naturales contra infecciones y aumentar el éxito de las inmunoterapias contra el cáncer.
Cita: Liu, Z., Li, R., Fan, C. et al. Deltex E3 ubiquitin ligase 2 potentiates STING-mediated type I interferon response by K63-linked ubiquitination. Cell Death Dis 17, 424 (2026). https://doi.org/10.1038/s41419-026-08659-4
Palabras clave: inmunidad innata, vía STING, señalización de interferón, inmunoterapia contra el cáncer, infección viral