Clear Sky Science · ar
يقوّي لِيغاز E3 يوبكويتين Deltex E3 2 استجابة الإنترفيرون من النوع الأول المتوسِّطة بواسطة STING عن طريق البلمرة باليوبيكويتين المرتبط بـ K63
كيف تكشف الخلايا الحمض النووي الخطِر
أجسامنا في حالة تأهب دائمة ضد الغزاة الفيروسيين وخلايا الورم الشاذة. أحد أنظمة الإنذار الأساسية لهذه الحماية المبكرة هو بروتين يُدعى STING، الذي يكشف الحمض النووي المتواجد في أماكن غير صحيحة داخل الخلايا ويطلق استجابات قوية مضادة للفيروسات والسرطان. تكشف هذه الورقة عن بروتين مساعد كان مهملًا سابقًا، DTX2، الذي يعمل كمقوٍّ جزيئي لـ STING، جاعلاً نظام الإنذار هذا أعلى وأكثر فعالية ضد العدوى والأورام.
جهاز إنذار خلوي للحمض النووي
عند غزو فيروسات مثل فيروس الهربس البسيط، أو عندما تتسرّب خلايا تالفة حمضها النووي، تظهر شظايا من الحمض النووي مزدوج الشريطة في أماكن لا تنتمي داخل خلايانا. إنزيم مستشعر يُسمى cGAS يكتشف هذا الحمض النووي المتشرد ويُنتج رسالة جزيئية صغيرة تُفعّل STING، وهو بروتين جالس على حُجرة غشائية داخلية. بعد تنشيطه، ينتقل STING إلى حجرة أخرى معروفة بالجولجي ويشغّل سلسلة إشارات تنتهي بإنتاج إنترفيرونات من النوع الأول وجزيئات التهابية. تعمل هذه المواد كأبواق كيميائية، تنبه وتفعّل الخلايا المناعية لمكافحة الفيروسات، وفي كثير من الحالات للتعرّف على الأورام ومهاجمتها. 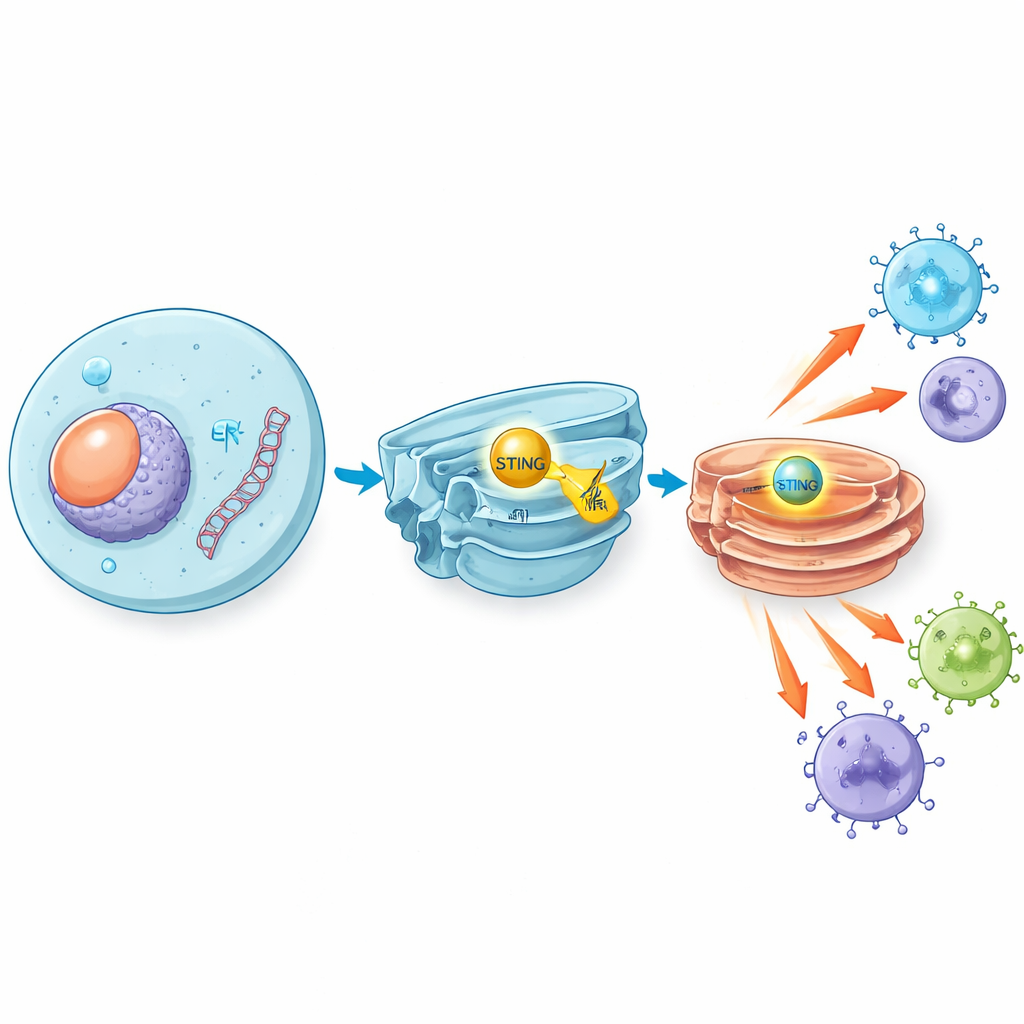
اكتشاف مساعد جديد لمسار STING
لكي يكتشف الباحثون أي الإنزيمات قد تضبط هذا النظام الإنذاري للحمض النووي، عرّضوا خلايا مناعية فأرية لعدوى فيروس الهربس وقاسوا أي الجينات ارتفعت أو انخفض تعبيرها. من بين مئات الإنزيمات، برز واحد: DTX2، وهو ليغاز E3 لليوبكويتين، ما يعني أنه قادر على إلحاق سلاسل صغيرة من اليوبكويتين ببروتينات أخرى لتغيير سلوكها. أنشأ الفريق فئرانًا تفتقر إلى جين Dtx2 ووجدوا أن خلاياها المناعية أنتجت كمية أقل بكثير من الإنترفيرون وإشارات مضادة للفيروسات عند تعرّضها للحمض النووي الفيروسي أو الحمض النووي الاصطناعي أو منشّط مباشر لـ STING. لوحظ هذا الانخفاض ليس فقط في الخلايا المناعية مثل البلعمات بل أيضًا في خلايا غير مناعية، وكان مخصصًا للاستجابات المحفزة بالحمض النووي بدلاً من فيروسات الـ RNA، مما يشير إلى دور مركّز لـ DTX2 في مسار كشف الحمض النووي.
كيف يضبط DTX2 إشارة STING
بتعمق أكثر، أظهر العلماء أن DTX2 يرتبط ماديًا بـ STING ويضيف شكلًا خاصًا من سلاسل اليوبكويتين، المعروفة بالسلاسل المرتبطة بـ K63، على نقطتين محددتين في STING. على عكس علامات اليوبكويتين الأخرى التي توصم البروتينات للتدمير، تعمل هذه السلاسل كملحقات وظيفية تغيّر مكان البروتين وكيفية إشارته. عندما غاب DTX2، بقيت مستويات STING طبيعية، لكن قدرته على الانتقال من غشاء البداية إلى الجولجي وتجميع إنزيم الإشارة التالي TBK1 تراجعت كثيرًا. حدّد الفريق حمضين أمينيين رئيسيين على STING، K236 وK370، كنقاط إلحاق لهذه السلاسل. عندما عدّلوا هذين الموقعين بحيث لا يمكن لتلك السلاسل أن تتكوّن، فشل STING في الانتقال بشكل صحيح، ولم يتم تجنيد TBK1 بكفاءة، وتباطأت استجابة الإنترفيرون المتأخرة.
الحماية من الفيروسات ودعم المناعة ضد السرطان
كانت عواقب هذا الضبط الجزيئي واضحة في الحيوانات الحية. الفئران التي تفتقر إلى Dtx2 ماتت بسهولة أكبر جراء عدوى فيروس الهربس، وأظهرت تلفًا رئويًا أشد، وحمولات فيروسية أعلى في أعضاء متعددة، ومستويات أقل من الإنترفيرونات والحالات الالتهابية الواقية في دمها. في نماذج السرطان، انقلبت الصورة: ارتبطت مستويات أعلى من DTX2 بتوقيعات إنترفيرون من النوع الأول أقوى وبزيادة تسلل خلايا مناعية محورية مثل الخلايا الشجرية، وخلايا T القاتلة، والخلايا القاتلة الطبيعية في مجموعات بيانات أورام بشرية. في نماذج سرطان الرأس والرقبة لدى الفئران، استجابت الأورام المهندسة لإنتاج المزيد من DTX2 بشكل أفضل لعقار منشط لـ STING ولعلاج نقاط التفتيش المناعي، إذ تقلصت أكثر وحوت خلايا مناعية أكثر من الأورام الضابطة. 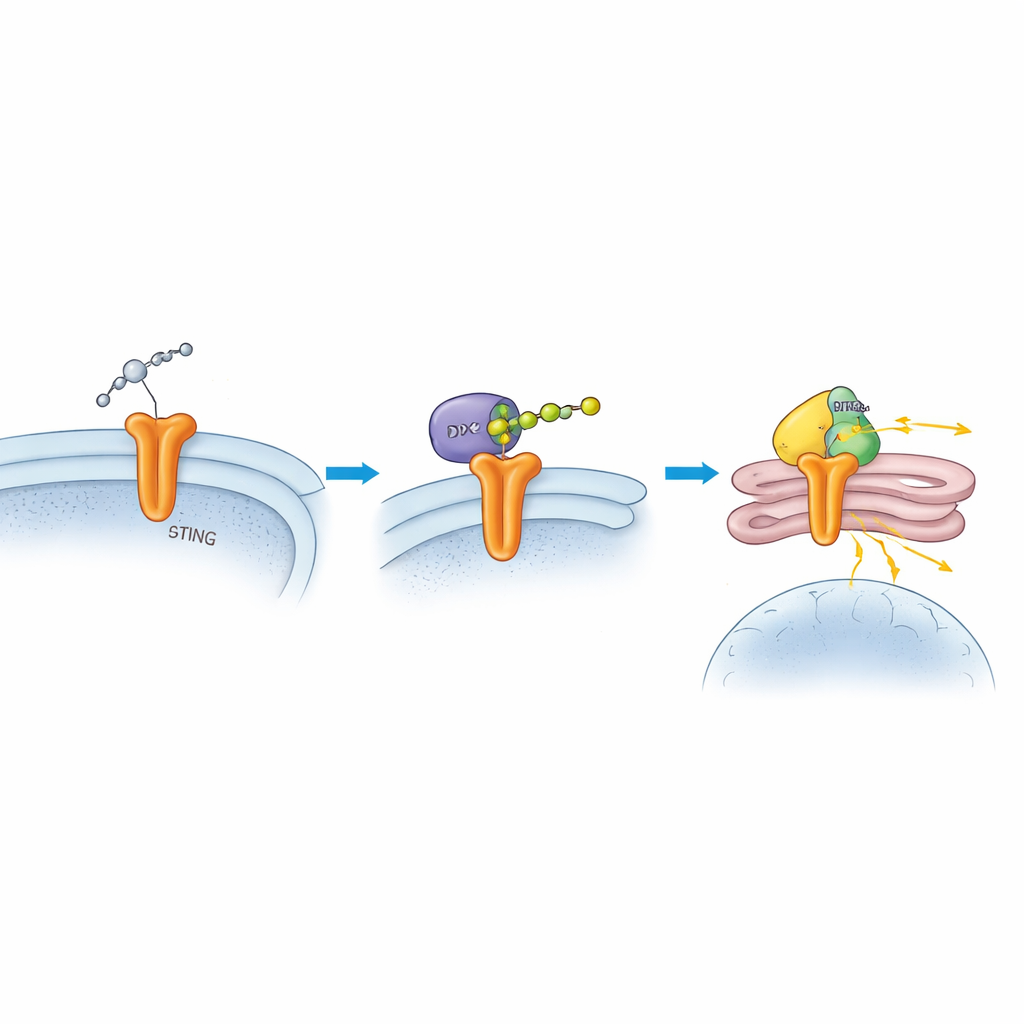
لماذا يهم هذا المقوٍّ الجزيئي
بالنسبة لغير المتخصصين، الرسالة الرئيسية هي أن DTX2 يعمل كمكبر حاسم لأحد أقدم مسارات الإنذار في الجهاز المناعي. عبر تزيين STING بالنوع الصحيح من العلامات الجزيئية في الأماكن المناسبة، يساعد DTX2 STING على الانتقال إلى الموضع المناسب داخل الخلية وتشغيل دفاعات مضادة للفيروسات ومضادة للأورام بكامل طاقتها. عندما يغيب DTX2 أو يُعطَّل عمله، يصبح الإنذار مكتومًا: تنتشر الفيروسات بسهولة أكبر وقد تَجد الأورام سبيلاً أكبر للتهرب من هجوم المناعة. يجعل هذا من DTX2 هدفًا واعدًا لعلاجات جديدة قد تعزّز دفاعاتنا الطبيعية ضد العدوى وتزيد من نجاح العلاجات المناعية للسرطان.
الاستشهاد: Liu, Z., Li, R., Fan, C. et al. Deltex E3 ubiquitin ligase 2 potentiates STING-mediated type I interferon response by K63-linked ubiquitination. Cell Death Dis 17, 424 (2026). https://doi.org/10.1038/s41419-026-08659-4
الكلمات المفتاحية: المناعة الفطرية, مسار STING, إشارة الإنترفيرون, العلاج المناعي للسرطان, العدوى الفيروسية