Clear Sky Science · de
Der Ubiquitin-Ligase Deltex E3 2 verstärkt die STING-vermittelte Typ-I-Interferon-Antwort durch K63-verknüpfte Ubiquitinierung
Wie Zellen gefährliche DNA erkennen
Unser Körper ist ständig auf der Suche nach viralen Eindringlingen und entarteten Tumorzellen. Eines der wichtigsten Alarmsysteme in dieser Früherkennung ist ein Protein namens STING, das fehlplatziertes DNA innerhalb der Zelle erkennt und starke antivirale sowie antitumorale Reaktionen auslöst. Diese Arbeit beschreibt ein bislang wenig beachtetes Hilfsprotein, DTX2, das als molekularer Verstärker für STING fungiert und dieses Alarmsystem lauter und effektiver gegen Infektionen und Tumore macht.
Ein zellulärer Einbruchsalarm für DNA
Wenn Viren wie das Herpes-simplex-Virus eindringen oder beschädigte Zellen DNA freisetzen, erscheinen Fragmente doppelsträngiger DNA an Orten innerhalb der Zelle, an denen sie nicht hingehören. Ein Sensorenzym namens cGAS erkennt diese fremde DNA und erzeugt ein kleines Botenmolekül, das STING aktiviert, ein Protein, das an einer inneren Membrankompartiment sitzt. Nach der Aktivierung wandert STING zum Golgi-Apparat und startet eine Signalkaskade, die schließlich zur Produktion von Typ-I-Interferonen und entzündungsfördernden Molekülen führt. Diese Substanzen wirken wie chemische Sirenen: Sie alarmieren und aktivieren Immunzellen, um Viren zu bekämpfen und in vielen Fällen Tumore zu erkennen und anzugreifen. 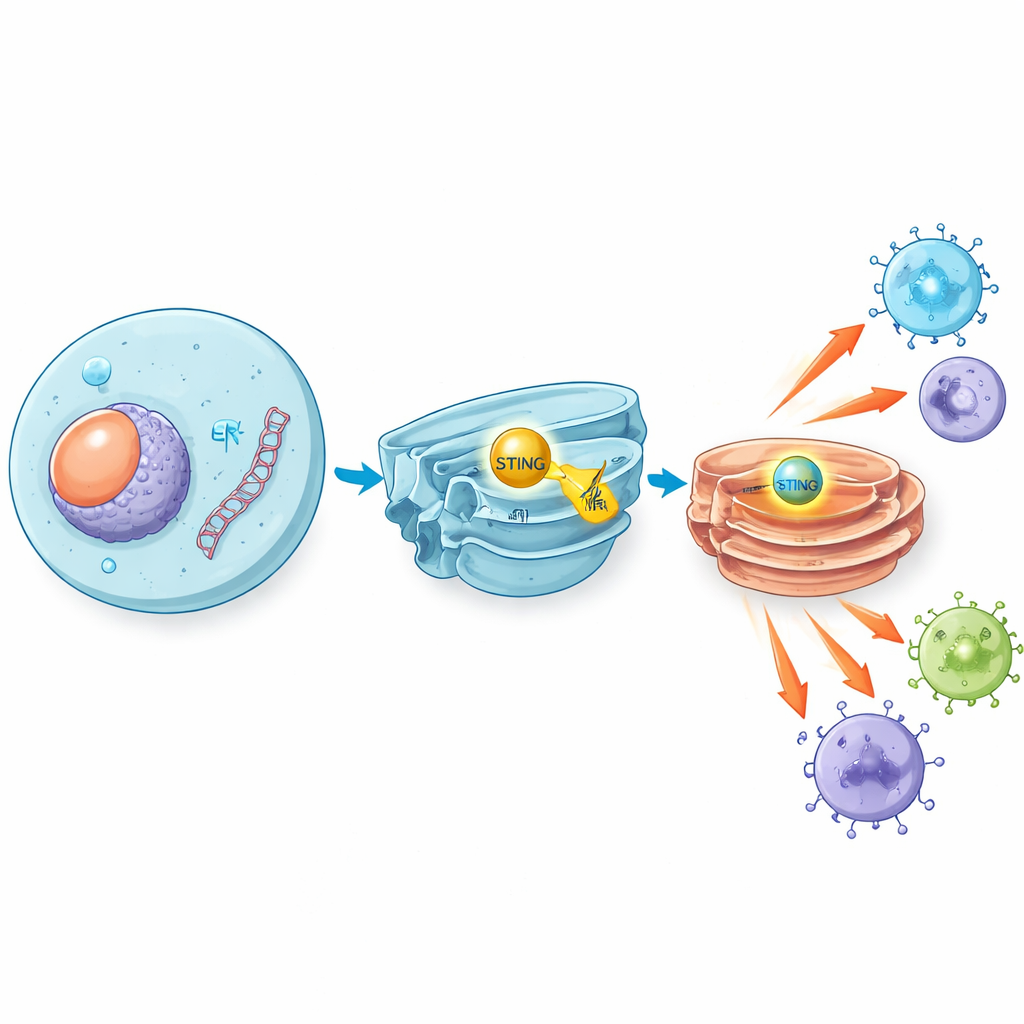
Entdeckung eines neuen Helfers im STING-Weg
Um herauszufinden, welche Enzyme dieses DNA-Alarmsystem feinabstimmen könnten, infizierten die Forschenden murine Immunzellen mit Herpesvirus und bestimmten, welche Gene hoch- oder runterreguliert wurden. Unter Hunderten von Enzymen stach eines hervor: DTX2, eine E3-Ubiquitin-Ligase, das heißt ein Enzym, das kleine Ubiquitinketten an andere Proteine anheften kann, um deren Verhalten zu verändern. Das Team erzeugte Mäuse ohne das Dtx2-Gen und stellte fest, dass ihre Immunzellen deutlich weniger Interferon und weniger antivirale Signale produzierten, wenn sie viraler DNA, synthetischer DNA oder einem direkten STING-Aktivator ausgesetzt waren. Dieser Rückgang war nicht nur in Immunzellen wie Makrophagen zu beobachten, sondern auch in nicht-immunen Zellen und betraf spezifisch DNA-ausgelöste Reaktionen, nicht RNA-Viren, was auf eine fokussierte Rolle von DTX2 im DNA-Erkennungsweg hinweist.
Wie DTX2 das STING-Signal verstärkt
Tiefergehende Untersuchungen zeigten, dass DTX2 physisch an STING bindet und eine bestimmte Form von Ubiquitinketten, bekannt als K63-verknüpfte Ketten, an zwei spezifische Stellen von STING anbringt. Im Gegensatz zu anderen Ubiquitinmarkierungen, die Proteine für den Abbau kennzeichnen, wirken diese Ketten eher wie funktionelle Anhängsel, die beeinflussen, wohin ein Protein gelangt und wie es signalisiert. Fehlt DTX2, bleiben die Gesamtmengen an STING zwar unverändert, doch seine Fähigkeit, von seiner Ausgangsmembran zum Golgi zu wandern und dort das nächste Signalenzym TBK1 zu rekrutieren, war deutlich reduziert. Das Team identifizierte zwei Schlüsselaminosäuren auf STING, K236 und K370, als Anheftungsstellen für diese Ketten. Mutierten sie diese Stellen so, dass die Ketten nicht mehr angebracht werden konnten, gelang STING die richtige Wanderung nicht, TBK1 wurde nicht effizient rekrutiert und die nachgeschaltete Interferonantwort war abgeschwächt.
Schutz gegen Viren und Unterstützung der Krebsimmunität
Die Konsequenzen dieser molekularen Feinabstimmung zeigten sich deutlich im Organismus. Mäuse ohne Dtx2 erlagen Herpesvirus-Infektionen leichter, wiesen schwerere Lungenschäden, höhere Viruslasten in mehreren Organen sowie geringere Spiegel schützender Interferone und entzündlicher Signale im Blut auf. In Krebsmodellen kehrte sich das Bild um: Höhere DTX2-Werte korrelierten mit stärkeren Typ-I-Interferon-Signaturen und einer vermehrten Infiltration wichtiger Immunakteure wie dendritischen Zellen, zytotoxischen T-Zellen und natürlichen Killerzellen in humanen Tumordatensätzen. In Mausmodellen für Kopf-Hals-Tumoren sprachen Tumore, die mehr DTX2 produzierten, besser auf ein STING-aktivierendes Medikament und auf Immun-Checkpoint-Therapie an, schrumpften stärker und enthielten mehr Immunzellen als Kontrolltumore. 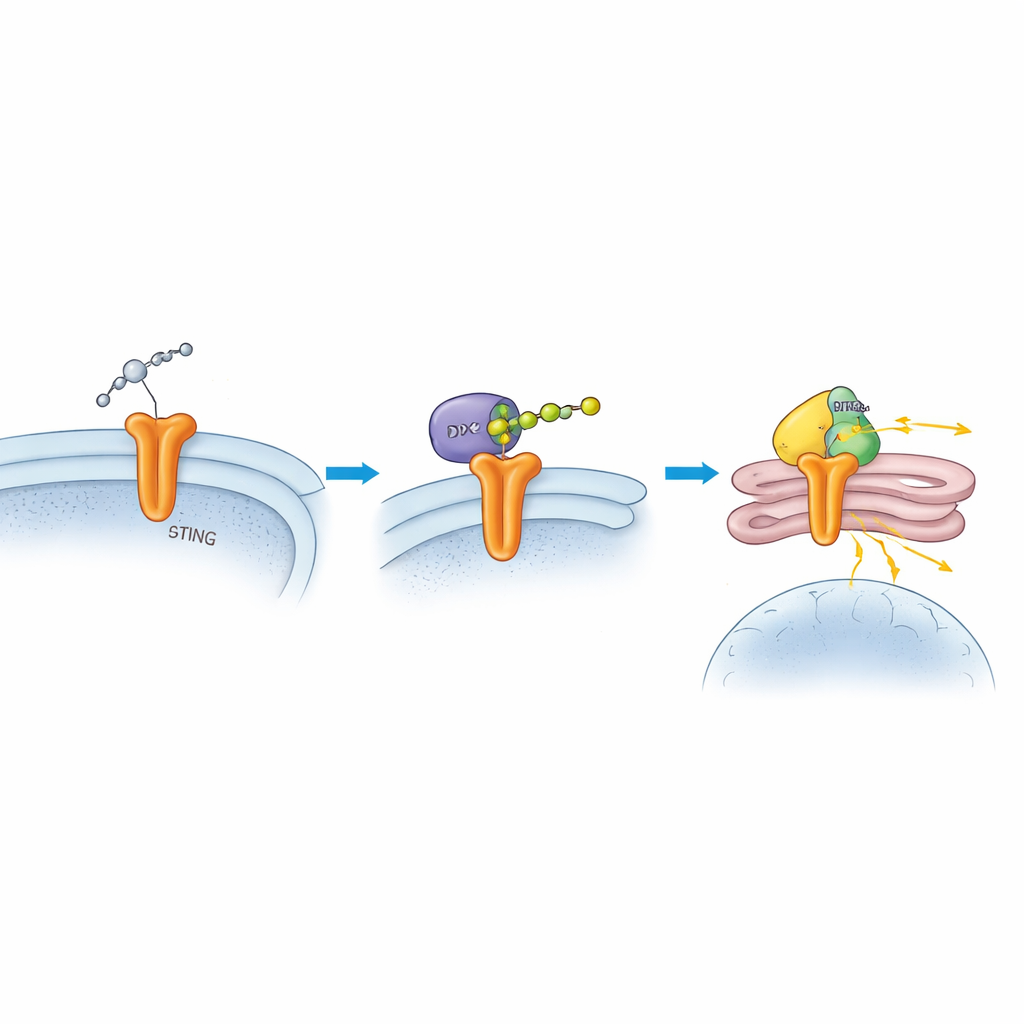
Warum dieser molekulare Verstärker wichtig ist
Für Nichtfachleute lautet die zentrale Botschaft: DTX2 fungiert als entscheidender Verstärker eines der frühesten Warnwege des Immunsystems. Indem es STING an den richtigen Stellen mit geeigneten molekularen Markierungen versieht, hilft DTX2 STING, an den richtigen Ort innerhalb der Zelle zu gelangen und antivirale sowie antitumorale Abwehrmechanismen vollständig einzuschalten. Fehlt DTX2 oder wird seine Funktion blockiert, wird der Alarm gedämpft: Viren verbreiten sich leichter und Tumoren können der Immunüberwachung eher entgehen. Das macht DTX2 zu einem vielversprechenden Ziel für neue Therapien, die unsere natürlichen Abwehrkräfte gegen Infektionen stärken und den Erfolg von Krebsimmuntherapien verbessern könnten.
Zitation: Liu, Z., Li, R., Fan, C. et al. Deltex E3 ubiquitin ligase 2 potentiates STING-mediated type I interferon response by K63-linked ubiquitination. Cell Death Dis 17, 424 (2026). https://doi.org/10.1038/s41419-026-08659-4
Schlüsselwörter: angeborene Immunität, STING-Signalweg, Interferon-Signalgebung, Krebsimmuntherapie, Virusinfektion