Clear Sky Science · ru
AKT1 фосфорилирует PRMT7, способствуя метилированию GLUD1 и прогрессированию рака желудка
Почему это важно для лечения рака
Клетки рака известны своей ненасытностью: они перестраивают метаболизм, чтобы расти и распространяться. В этом исследовании обнаружена ранее не выявленная молекулярная цепочка, которая помогает клеткам рака желудка использовать питательный глутамин при колебаниях запасов сахара. Расшифровав, как эта схема сохраняет ключевой метаболический фермент живым и активным, авторы указывают на новую уязвимость, которая может сделать существующие химиотерапевтические препараты более эффективными против рака желудка.
Переключатель топлива, помогающий опухолям выживать
Многие слышали о «любви» рака к сахару, часто описываемой как эффект Варбурга. Но опухолевые клетки также опираются на глутамин — обильную аминокислоту, которая снабжает их энергетические станции и предоставляет строительные блоки для ДНК и других молекул. В центре этого процесса находится фермент GLUD1, превращающий глутамин-опосредованный глутамат в молекулу, питающую основной энергетический цикл клетки. Уровень GLUD1 часто повышен во многих злокачественных новообразованиях, включая опухоли желудка; ранние работы показали, что блокада GLUD1 может замедлить рост опухоли и повысить эффективность химиотерапии. До сих пор учёные не понимали, как клетки рака тонко регулируют количество и активность GLUD1 при изменении условий питания.
Химический «ярлык», защищающий ключевой фермент
Авторы показали, что GLUD1 контролируется небольшой химической меткой на одном из его аминокислотных остатков — аргинине на позиции 76. Эта метка, метильная группа, добавляется ферментом PRMT7. С помощью специально созданного антитела, которое распознаёт GLUD1 только при метилировании этого аргинина, они продемонстрировали, что это место является крупной и высококонсервативной модификацией. Когда метилирование блокировали лекарствами или путём мутации этого аргинина, препятствующей модификации, уровень GLUD1 быстро падал при неизменной генетической информации. Объяснение простое: без метилирования GLUD1 сильнее помечался убиквитином — сигналом на утилизацию белка клеточными механизмами удаления. Иными словами, метилирование действует как защитный щит, предотвращающий разрушение GLUD1.
Как здесь связаны уровень сахара в крови и ростовые сигналы
Затем команда изучила, как внешние условия питания влияют на эту защитную метилизацию внутри клетки. Они обнаружили, что высокий уровень глюкозы снижает уровень белка GLUD1, тогда как низкая глюкоза, инсулин или противодиабетический препарат метформин способствуют накоплению GLUD1. Эти эффекты связываются с путем PI3K/Akt — ключевой сигнальной линией, контролирующей ответ клеток на факторы роста и использование глюкозы. При ингибировании этого пути, и особенно фермента AKT1, GLUD1 становился менее метилированным и более убиквитинированным, что стимулировало его деградацию. Дальнейшие эксперименты показали, что AKT1 не модифицирует GLUD1 напрямую; вместо этого он связывается с PRMT7 и фосфорилирует его в специфическом треонине (T73). Эта фосфорилирование усиливает активность PRMT7 и его способность метилировать GLUD1, тем самым стабилизируя GLUD1 и поддерживая метаболизм глутамина при стрессe из‑за низкой глюкозы.
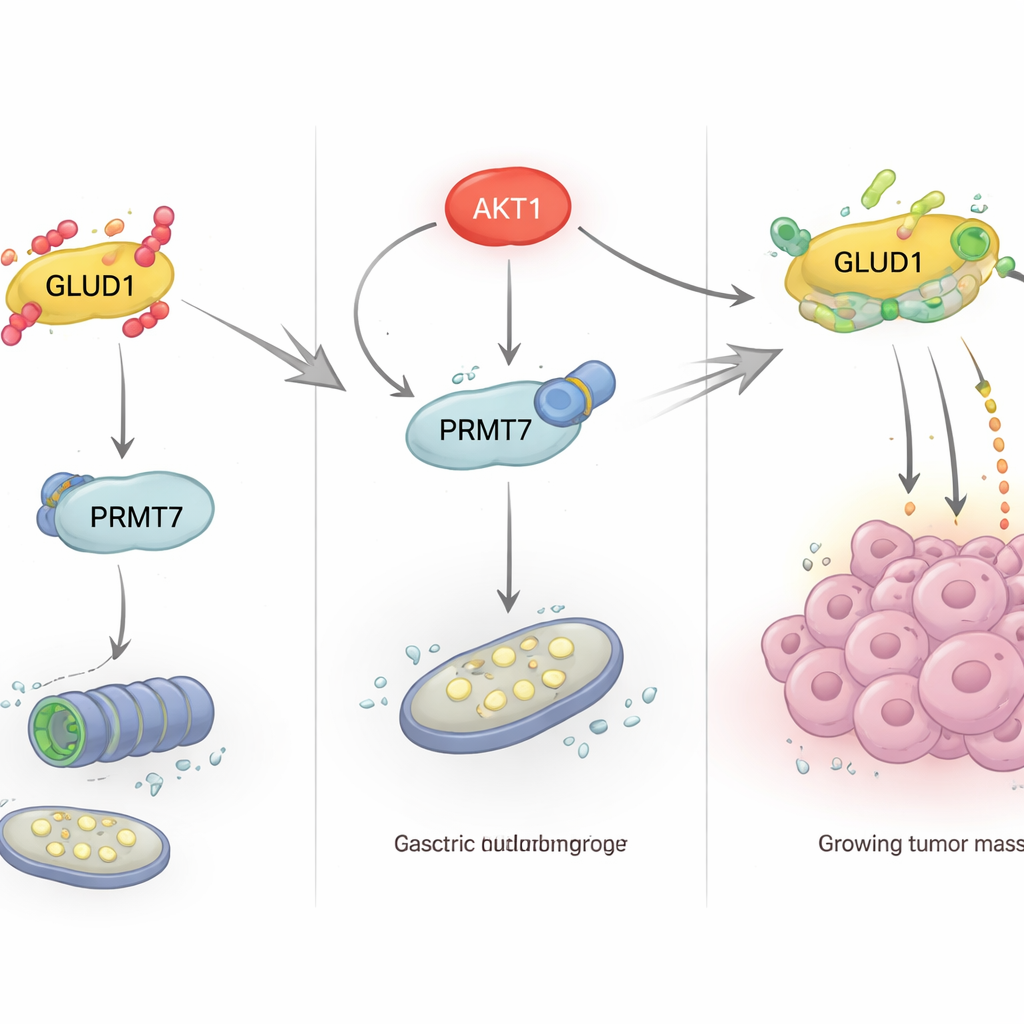
От молекулярного переключателя к росту опухоли
Стабилизация GLUD1 — это не просто биохимическая любопытность; она имеет ощутимые последствия для поведения опухоли. Когда исследователи заменили нормальный GLUD1 на версию, неспособную к метилированию, в клетках рака желудка снизилась ферментативная активность GLUD1, ослабли энергетическое и строительно‑блоковое обеспечение глутамином, а клетки меньше пролиферировали и мигрировали. Блокада PRMT7 генетическими методами или селективным препаратом SGC3027 воспроизводила этот эффект: снижалось метилирование GLUD1, падал уровень белка GLUD1 и замедлялся рост и подвижность раковых клеток. В образцах тканей пациентов с раком желудка опухоли демонстрировали более высокие уровни GLUD1, метилированного GLUD1 и PRMT7 по сравнению с близкими нормальными тканями, и эти маркеры росли и падали синхронно, что подтверждает активность этой оси при человеческом заболевании.
Новая надежда на усиление химиотерапии
Поскольку GLUD1 уже связывали с устойчивостью к химиопрепарату доцетакселу (DTX), авторы проверили, может ли таргетирование PRMT7 улучшить лечение. В культуре клеток SGC3027 замедлял рост клеток рака желудка, а сочетание с DTX давало более сильное подавление, чем каждый препарат по отдельности. Опухоли, выращенные в мышах, сокращались значительно сильнее при совместном применении двух препаратов — примерно на 80% по весу по сравнению с контрольной группой, получавшей никакого лечения, и наблюдалось заметное снижение маркера клеточного деления. Примечательно, что опухоли и клеточные линии, устойчивые к DTX, демонстрировали более высокое метилирование GLUD1, что говорит о том, что блокада этой модификации может помочь преодолеть устойчивость. Проще говоря, исследование выявляет релейную цепочку AKT1–PRMT7–GLUD1, которая позволяет клеткам рака желудка адаптировать использование топлива и выживать, и показывает, что разрыв этой цепочки может ослабить опухоли и усилить эффект существующей химиотерапии.
Цитирование: Cui, Z., Li, H., Liang, X. et al. AKT1 phosphorylates PRMT7 to promote GLUD1 methylation and gastric cancer progression. Cell Death Dis 17, 363 (2026). https://doi.org/10.1038/s41419-026-08601-8
Ключевые слова: рак желудка, метаболизм опухоли, глутамин, метилирование белков, таргетная терапия