Clear Sky Science · pt
Abordagens biotecnológicas para produzir peptídeos terapêuticos em plantas
Transformando Folhas Verdes em Medicamentos Curativos
A maioria dos medicamentos modernos, especialmente fármacos proteicos e peptídicos complexos, é produzida em tanques de aço preenchidos com bactérias ou células animais. Esta revisão explora uma ideia diferente: usar as próprias plantas vivas como minifábricas de peptídeos terapêuticos—cadeias curtas de aminoácidos que podem combater infecções, tratar câncer ou modular um sistema imune hiperativo. Os autores explicam por que as plantas podem tornar esses medicamentos mais acessíveis e seguros, e como os cientistas estão aprendendo a induzir folhas, sementes e até culturas de células vegetais a produzir de modo confiável peptídeos potentes e estáveis.
Por que as Plantas São Atraentes como Fábricas de Medicamentos
Plataformas tradicionais de produção, como bactérias, leveduras e células de mamíferos, são poderosas, mas caras, exigem know‑how técnico elevado e podem apresentar riscos de contaminação por patógenos humanos. Em contraste, as plantas crescem com luz solar, água e nutrientes simples, escalam facilmente de estufas a campos e não hospedam vírus humanos ou animais. Nas últimas duas décadas, parentes do tabaco e culturas alimentares como arroz, milho, batata e tomate produziram com sucesso vacinas, anticorpos, hormônios e enzimas—alguns já testados em humanos ou aprovados para uso. Essa experiência mostra que plantas podem manejar produtos biológicos sofisticados e prepara o caminho para ampliar o uso a fármacos à base de peptídeos, que são menores, mas frequentemente mais difíceis de fabricar e estabilizar.
Aumentando a Quantidade de Peptídeo que as Plantas Podem Produzir
Fazer uma planta produzir quantidades úteis de um peptídeo terapêutico exige ajustar cuidadosamente cada etapa, do gene ao produto final. Pesquisadores escolhem interruptores genéticos fortes ou específicos de tecido (promotores) para que o peptídeo seja produzido principalmente em locais seguros, como sementes, que naturalmente acumulam grandes quantidades de proteína e mantêm produtos estáveis por longos períodos. Também se usam ferramentas de DNA inspiradas em vírus que copiam temporariamente o gene terapêutico muitas vezes dentro das células das folhas, proporcionando picos rápidos e elevados de produção. Ajustar o código genético para combinar com as preferências da planta pode elevar ainda mais a produção, embora seja preciso fazê‑lo de forma ponderada para que o RNA resultante continue a dobrar e a funcionar bem. Em conjunto, essas estratégias podem transformar uma planta de produtora relutante em uma biofábrica de alto rendimento.
Protegendo Peptídeos Frágeis Dentro da Planta
Uma vez produzidos, os peptídeos precisam sobreviver aos próprios sistemas de manutenção da planta, que continuamente degradam proteínas, respondem ao estresse e removem moléculas danificadas. A revisão destaca várias formas de proteger produtos valiosos desse desgaste interno. Uma é co produzir inibidores de proteases naturais ou desativar seletivamente as proteases vegetais mais problemáticas, reduzindo a degradação indesejada. Outra é direcionar peptídeos para compartimentos celulares mais seguros, como o retículo endoplasmático, vacúolos, cloroplastos ou o apoplasto fora da membrana celular, onde há menos enzimas destrutivas ou onde as modificações químicas necessárias são adicionadas. Uma abordagem particularmente poderosa é incentivar as plantas a formar peptídeos cíclicos—moléculas em loop fechadas encontradas em algumas espécies selvagens—que resistem às enzimas digestivas e permanecem estáveis o suficiente para administração oral.
Truques de Design para Reduzir Estresse e Toxicidade nas Plantas
Muitos peptídeos terapêuticos são projetados para perfurar membranas microbianas ou interferir em sinalizações, o que significa que também podem prejudicar células vegetais se produzidos no local errado ou no momento errado. Para evitar isso, os cientistas usam interruptores indutíveis que mantêm os genes silenciados até que um gatilho externo, como uma pulverização, os ative depois que a planta tenha crescido. Confinam a expressão a sementes, tubérculos ou compartimentos celulares específicos onde os peptídeos têm menos probabilidade de danificar tecidos vitais. Parceiros de fusão especiais podem mascarar temporariamente a atividade do peptídeo, ajudar no dobramento correto, formar corpos proteicos densos para armazenamento e simplificar a purificação. Os autores também descrevem como tratamentos térmicos suaves e químicos antioxidantes podem acalmar respostas de estresse durante a entrega de genes, aumentando a eficiência de transformação e a expressão transitória.
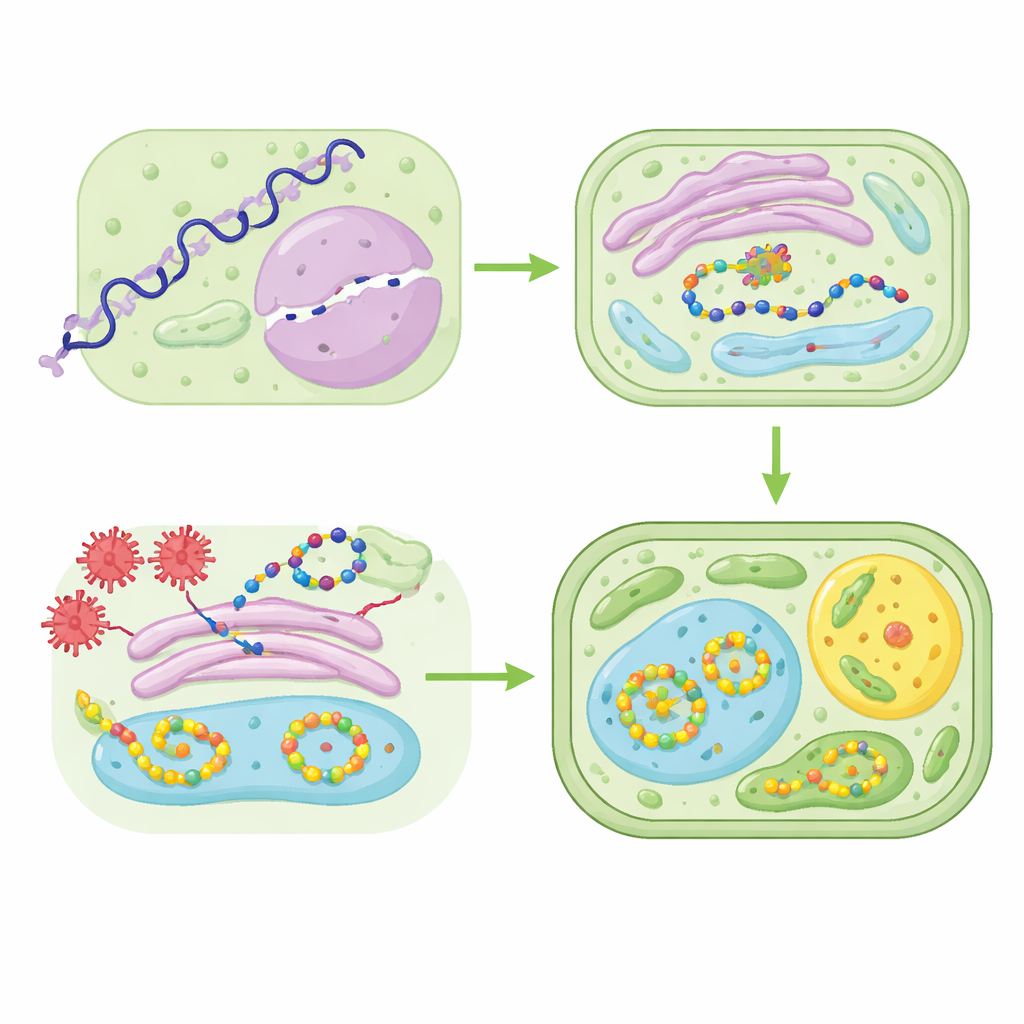
Engenharia do Metabolismo e Superando Obstáculos do Mundo Real
Além do próprio peptídeo, o metabolismo vegetal deve fornecer os blocos de construção corretos sem ficar sobrecarregado. A engenharia metabólica permite aos pesquisadores adicionar genes biossintéticos ausentes, bloquear reações colaterais que criam subprodutos indesejados e ajustar os níveis de expressão para que as plantas permaneçam saudáveis enquanto produzem compostos de alto valor, como precursores anticâncer ou feromônios de insetos. Ao mesmo tempo, o campo precisa navegar por desafios práticos: manter a qualidade do produto consistente entre lotes, alinhar a produção em campo aberto ou em estufa com padrões de fabricação farmacêutica e reduzir os custos de extração e purificação de medicamentos a partir de tecidos vegetais complexos. Culturas controladas de células vegetais e sistemas de raízes pilosas oferecem uma via para cadeias de produção mais padronizadas e compatíveis com GMP.
De Parâmetros Experimentais a Terapias do Dia a Dia
A revisão conclui que as plantas estão preparadas para desempenhar um papel importante na próxima geração de medicamentos peptídicos, mas que o sucesso dependerá de adaptar estratégias para cada molécula individual. Fatores como a necessidade de ligações dissulfeto, ciclação, anexos de açúcares especiais ou proteção rigorosa contra degradação ditarão a melhor escolha de espécie vegetal, tecido, compartimento celular e sistema de controle genético. Combinando avanços em desenho de genes, biologia celular, engenharia metabólica e manejo de estresse, os pesquisadores visam construir plataformas vegetais robustas e escaláveis capazes de fornecer peptídeos terapêuticos estáveis e potentes a menor custo e com alcance global.
Citação: Thanthrige, N., Lawrence, N. & Craik, D.J. Biotechnological approaches for producing therapeutic peptides in plants. npj Sci. Plants 2, 12 (2026). https://doi.org/10.1038/s44383-026-00021-z
Palavras-chave: agricultura molecular vegetal, peptídeos terapêuticos, fármacos produzidos em plantas, produção de proteínas recombinantes, engenharia metabólica em plantas