Clear Sky Science · fr
Approches biotechnologiques pour produire des peptides thérapeutiques dans les plantes
Transformer des feuilles vertes en remèdes
La plupart des médicaments modernes, en particulier les protéines et peptides thérapeutiques complexes, sont fabriqués dans des cuves d’acier contenant des bactéries ou des cellules animales. Cette revue explore une idée différente : utiliser les plantes vivantes elles‑mêmes comme de petites usines pour produire des peptides thérapeutiques — de courtes chaînes d’acides aminés capables de combattre des infections, traiter le cancer ou apaiser un système immunitaire hyperactif. Les auteurs expliquent pourquoi les plantes pourraient rendre ces médicaments plus abordables et plus sûrs, et comment les scientifiques apprennent à convaincre les feuilles, les graines et même les cultures de cellules végétales de produire de manière fiable des peptides puissants et stables.
Pourquoi les plantes sont des usines attrayantes pour les médicaments
Les plateformes de production traditionnelles comme les bactéries, les levures et les cellules de mammifères sont performantes mais coûteuses, techniquement exigeantes et peuvent présenter des risques de contamination par des agents pathogènes humains. En revanche, les plantes se nourrissent de lumière, d’eau et d’éléments simples, se dimensionnent facilement de la serre au champ et n’hébergent pas les virus humains ou animaux. Au cours des deux dernières décennies, des espèces proches du tabac et des cultures alimentaires comme le riz, le maïs, la pomme de terre et la tomate ont produit avec succès des vaccins, des anticorps, des hormones et des enzymes — certains testés chez l’homme ou approuvés. Cette expérience montre que les plantes peuvent gérer des produits biologiques sophistiqués et ouvre la voie à l’extension aux médicaments à base de peptides, plus petits mais souvent plus difficiles à produire et à stabiliser.
Augmenter la quantité de peptide produite par les plantes
Obtenir d’une plante des quantités utiles d’un peptide thérapeutique exige d’ajuster soigneusement chaque étape, du gène au produit final. Les chercheurs choisissent des interrupteurs génétiques puissants ou spécifiques à un tissu (promoteurs) pour que le peptide soit principalement synthétisé dans des zones sûres comme les graines, qui stockent naturellement de grandes quantités de protéines et conservent les produits longtemps. Ils utilisent également des outils d’ADN inspirés des virus qui copient temporairement le gène thérapeutique de nombreuses fois à l’intérieur des cellules foliaires, produisant des pics rapides et élevés de production. L’adaptation du code génétique aux préférences de la plante peut encore augmenter le rendement, bien que cela doive être fait judicieusement pour que l’ARN résultant se replie et fonctionne correctement. Ensemble, ces stratégies peuvent transformer une plante d’un producteur réticent en une bio‑usine à haut rendement.
Protéger les peptides fragiles à l’intérieur de la plante
Une fois synthétisés, les peptides doivent survivre aux systèmes d’entretien de la plante, qui dégradent en continu les protéines, réagissent au stress et éliminent les molécules endommagées. La revue met en lumière plusieurs moyens de protéger ces produits précieux contre cette usure interne. L’un d’eux consiste à coproduire des inhibiteurs de protéases naturels ou à désactiver sélectivement les protéases végétales les plus problématiques, réduisant ainsi la dégradation indésirable. Une autre stratégie consiste à diriger les peptides vers des compartiments cellulaires plus sûrs comme le réticulum endoplasmique, les vacuoles, les chloroplastes ou l’apoplasme hors de la membrane plasmique, où sont présents moins d’enzymes destructrices ou où s’ajoutent les modifications chimiques nécessaires. Une approche particulièrement puissante consiste à encourager les plantes à former des peptides cycliques — des molécules en boucle fermée présentes chez certaines espèces sauvages — qui résistent aux enzymes digestives et restent suffisamment stables pour être administrées par voie orale.
Astuces de conception pour réduire le stress et la toxicité chez la plante
Beaucoup de peptides thérapeutiques sont conçus pour perforer les membranes microbiennes ou perturber des voies de signalisation, ce qui signifie qu’ils peuvent aussi endommager les cellules végétales s’ils sont produits au mauvais endroit ou au mauvais moment. Pour éviter cela, les scientifiques utilisent des interrupteurs inductibles qui maintiennent les gènes silencieux jusqu’à un déclencheur externe, comme une pulvérisation, qui les active après la croissance de la plante. Ils confinent l’expression aux graines, tubercules ou compartiments cellulaires spécifiques où les peptides sont moins susceptibles d’endommager les tissus vitaux. Des partenaires de fusion spéciaux peuvent masquer temporairement l’activité du peptide, faciliter son repliement correct, former des corps protéiques denses pour le stockage et simplifier la purification. Les auteurs décrivent aussi comment des traitements thermiques doux et des antioxydants chimiques peuvent apaiser les réponses au stress lors du transfert de gènes, améliorant l’efficacité de la transformation et l’expression transitoire.
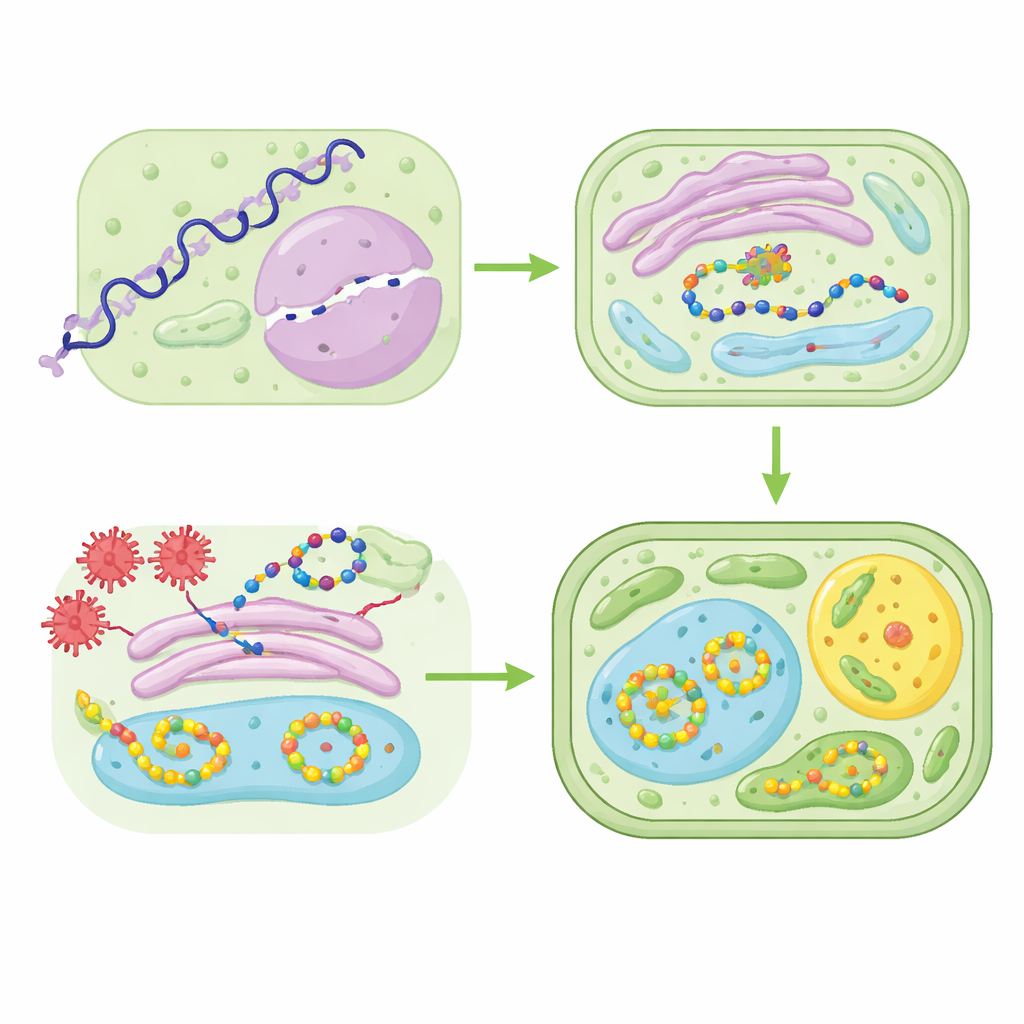
Ingénierie du métabolisme et surmonter les obstacles pratiques
Au‑delà du peptide lui‑même, le métabolisme de la plante doit fournir les bons éléments de construction sans être saturé. Le génie métabolique permet aux chercheurs d’ajouter des gènes biosynthétiques manquants, de bloquer des réactions secondaires qui créent des sous‑produits indésirables et d’ajuster finement les niveaux d’expression pour que les plantes restent en bonne santé tout en produisant des composés de grande valeur comme des précurseurs anticancéreux ou des phéromones d’insectes. Parallèlement, le domaine doit composer avec des obstacles pratiques : maintenir la qualité du produit d’un lot à l’autre, concilier la production en champ ouvert ou en serre avec les normes de fabrication pharmaceutique, et réduire les coûts d’extraction et de purification des médicaments à partir de tissus végétaux complexes. Les cultures cellulaires végétales contrôlées et les systèmes de racines « poilues » offrent une voie vers des chaînes de production plus standardisées et compatibles GMP.
Des parcelles expérimentales aux thérapies courantes
La revue conclut que les plantes sont prêtes à jouer un rôle majeur dans la prochaine génération de médicaments peptidiques, mais que le succès dépendra d’une adaptation des stratégies à chaque molécule. Des facteurs tels que la nécessité de liaisons disulfure, la cyclisation, des attaches glycosidiques particulières ou une protection stricte contre la dégradation dicteront le meilleur choix d’espèce végétale, de tissu, de compartiment cellulaire et de système de contrôle génétique. En combinant les avancées en conception de gènes, biologie cellulaire, génie métabolique et gestion du stress, les chercheurs visent à bâtir des plateformes végétales robustes et évolutives capables de fournir des peptides thérapeutiques stables et puissants à moindre coût et avec une portée mondiale.
Citation: Thanthrige, N., Lawrence, N. & Craik, D.J. Biotechnological approaches for producing therapeutic peptides in plants. npj Sci. Plants 2, 12 (2026). https://doi.org/10.1038/s44383-026-00021-z
Mots-clés: production moléculaire végétale, peptides thérapeutiques, médicaments produits par les plantes, production de protéines recombinantes, génie métabolique chez les plantes