Clear Sky Science · de
Biotechnologische Ansätze zur Herstellung therapeutischer Peptide in Pflanzen
Grüne Blätter in heilende Arzneien verwandeln
Die meisten modernen Arzneimittel, insbesondere komplexe Protein- und Peptidpräparate, werden in Stahltanks mit Bakterien- oder tierischen Zellkulturen hergestellt. Diese Übersicht untersucht eine andere Idee: lebende Pflanzen selbst als miniaturisierte Fabriken für therapeutische Peptide zu nutzen — kurze Aminosäureketten, die Infektionen bekämpfen, Krebs behandeln oder ein überaktives Immunsystem dämpfen können. Die Autoren erläutern, warum Pflanzen diese Medikamente erschwinglicher und sicherer machen könnten und wie Wissenschaftler lernen, Blätter, Samen und sogar Pflanzenzellkulturen so zu steuern, dass sie zuverlässig wirksame, stabile Peptidwirkstoffe produzieren.
Warum Pflanzen attraktive Arzneifabriken sind
Traditionelle Produktionsplattformen wie Bakterien, Hefen und Säugetierzellen sind leistungsfähig, aber teuer, technisch anspruchsvoll und können Risiken durch Kontamination mit humanen Krankheitserregern bergen. Im Gegensatz dazu wachsen Pflanzen mit Sonnenlicht, Wasser und einfachen Nährstoffen, lassen sich leicht vom Gewächshaus auf das Feld skalieren und beherbergen keine humanen oder tierischen Viren. In den letzten zwei Jahrzehnten haben Tabakverwandte und Nahrungspflanzen wie Reis, Mais, Kartoffel und Tomate erfolgreich Impfstoffe, Antikörper, Hormone und Enzyme produziert — einige bereits am Menschen getestet oder zugelassen. Diese Erfahrungen zeigen, dass Pflanzen komplexe biologische Produkte verarbeiten können und bereiten den Weg für eine Ausweitung auf peptidbasierte Medikamente, die zwar kleiner, aber oft schwieriger herzustellen und zu stabilisieren sind.
Die Ausbeute an Peptiden in Pflanzen steigern
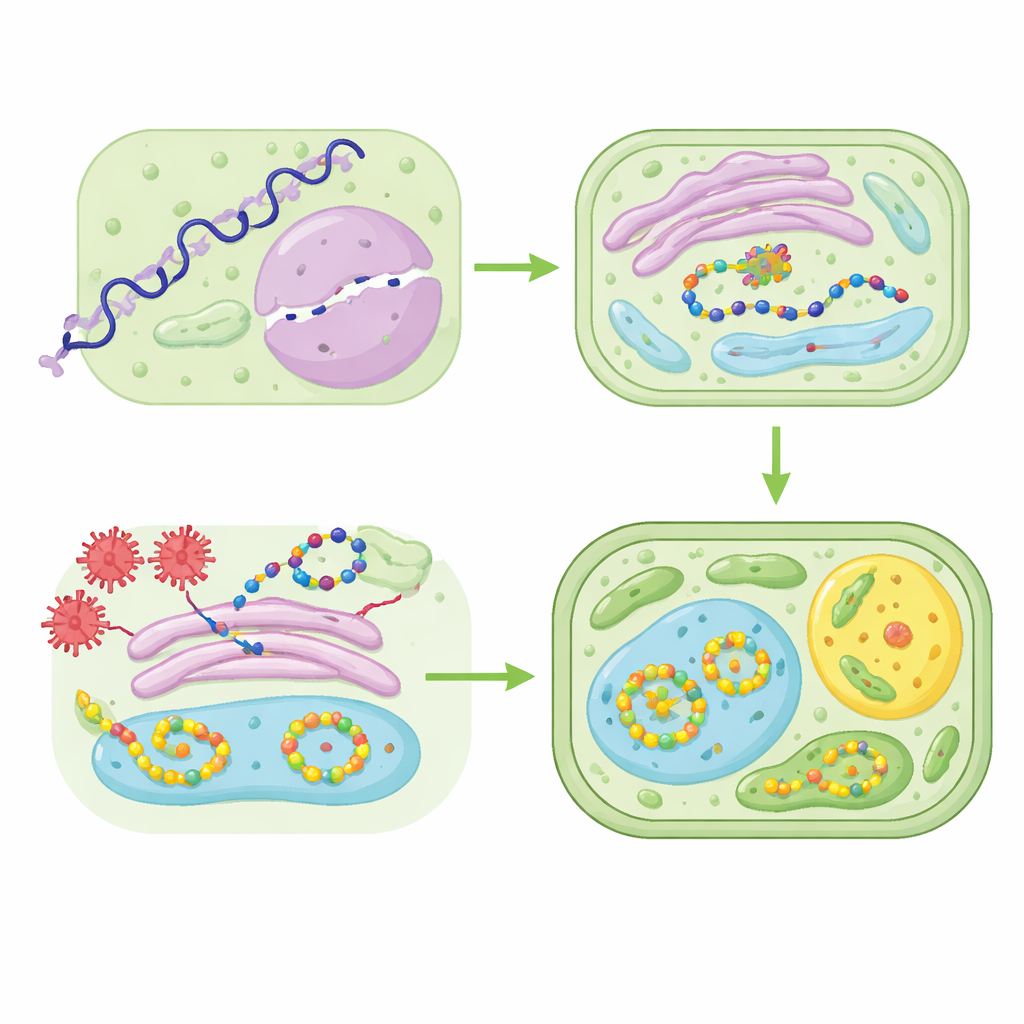
Damit eine Pflanze nützliche Mengen eines therapeutischen Peptids produziert, muss jeder Schritt vom Gen bis zum Endprodukt sorgfältig abgestimmt werden. Forschende wählen starke oder gewebespezifische genetische Schalter (Promotoren), sodass das Peptid vorwiegend an sicheren Orten wie Samen produziert wird, die von Natur aus große Proteinmengen speichern und Produkte über lange Zeit stabil halten. Sie nutzen auch von Viren inspirierte DNA‑Werkzeuge, die das Therapiegen vorübergehend vielfach in Blattzellen kopieren und so schnelle, hohe Produktionsspitzen ermöglichen. Die Anpassung des genetischen Codes an pflanzliche Präferenzen kann die Ausbeute weiter erhöhen, muss jedoch so erfolgen, dass die resultierende RNA weiterhin korrekt faltet und funktioniert. Zusammen können diese Strategien eine Pflanze von einem widerwilligen Produzenten in eine ertragreiche Biofabrik verwandeln.
Fragile Peptide in der Pflanze schützen
Nach der Synthese müssen Peptide die eigenen zellulären Aufräummechanismen der Pflanze überdauern, die kontinuierlich Proteine abbauen, auf Stress reagieren und beschädigte Moleküle entfernen. Die Übersicht hebt mehrere Methoden hervor, um wertvolle Produkte vor diesem internen Verschleiß zu schützen. Eine Möglichkeit ist die Koexpression natürlicher Proteaseinhibitoren oder das gezielte Abschalten der problematischsten pflanzlichen Proteasen, um unerwünschten Abbau zu reduzieren. Eine andere Strategie besteht darin, Peptide in sicherere Zellräume wie das endoplasmatische Retikulum, Vakuolen, Chloroplasten oder das Apoplast außerhalb der Zellmembran zu lenken, wo weniger zerstörerische Enzyme lauern oder notwendige chemische Modifikationen vorgenommen werden. Besonders wirkungsvoll ist die Förderung der Bildung zyklischer Peptide — geschlossene Moleküle, wie sie in einigen Wildarten vorkommen — die gegenüber Verdauungsenzymen resistent sind und stabil genug, um oral verabreicht zu werden.
Designtricks, um Pflanzensress und Toxizität zu reduzieren
Viele therapeutische Peptide sind so entworfen, dass sie Löcher in mikrobiellen Membranen schlagen oder Signalwege stören, weshalb sie Pflanzenzellen schädigen können, wenn sie am falschen Ort oder zur falschen Zeit produziert werden. Um dies zu umgehen, verwenden Wissenschaftler induzierbare Schalter, die Gene stumm halten, bis ein äußerer Auslöser, etwa ein Spray, sie nach dem Pflanzenwachstum aktiviert. Sie beschränken die Expression auf Samen, Knollen oder bestimmte zelluläre Kompartimente, in denen Peptide weniger wahrscheinlich lebenswichtige Gewebe schädigen. Spezielle Fusionspartner können die Peptidaktivität vorübergehend maskieren, das richtige Falten unterstützen, dichte Proteinkörper zur Lagerung bilden und die Aufreinigung vereinfachen. Die Autoren beschreiben außerdem, wie milde Hitzebehandlungen und Antioxidantien Stressreaktionen während der Genübertragung dämpfen und so die Transformations‑Effizienz und die transiente Expression erhöhen können.
Stoffwechselengineering und Bewältigung praktischer Hindernisse
Über das Peptid hinaus muss der pflanzliche Stoffwechsel die richtigen Bausteine liefern, ohne überfordert zu werden. Metabolisches Engineering erlaubt es Forschern, fehlende biosynthetische Gene hinzuzufügen, Nebenreaktionen zu blockieren, die unerwünschte Nebenprodukte erzeugen, und die Expressionsniveaus so fein abzustimmen, dass Pflanzen gesund bleiben und gleichzeitig hochpreisige Verbindungen wie Krebsvorläufer oder Insektenpheromone produzieren. Gleichzeitig muss das Feld praktische Hürden meistern: gleichbleibende Produktqualität von Charge zu Charge, die Angleichung von Freiland- oder Gewächshausproduktion an pharmazeutische Standards und die Senkung der Kosten für Extraktion und Reinigung aus komplexem Pflanzenmaterial. Kontrollierte Pflanzenzellkulturen und Haarwurzel‑Systeme bieten einen Weg zu standardisierteren, GMP‑kompatiblen Produktionsketten.
Von Versuchsfeldern zu alltäglichen Therapien
Die Übersicht schließt mit der Einschätzung, dass Pflanzen bereit sind, eine wichtige Rolle in der nächsten Generation von Peptidmedikamenten zu spielen, dass der Erfolg aber davon abhängt, Strategien an jedes einzelne Molekül anzupassen. Faktoren wie das Vorhandensein von Disulfidbrücken, Cyclisierung, spezielle Zuckeranhängsel oder strenger Schutz vor Abbau bestimmen die beste Wahl von Pflanzenart, Gewebe, zellulärem Kompartiment und genetischem Kontrollsystem. Durch die Kombination von Fortschritten in Gentwurf, Zellbiologie, Stoffwechselengineering und Stressmanagement wollen Forschende robuste, skalierbare pflanzenbasierte Plattformen aufbauen, die stabile, wirksame therapeutische Peptide zu geringeren Kosten und mit globaler Reichweite liefern können.
Zitation: Thanthrige, N., Lawrence, N. & Craik, D.J. Biotechnological approaches for producing therapeutic peptides in plants. npj Sci. Plants 2, 12 (2026). https://doi.org/10.1038/s44383-026-00021-z
Schlüsselwörter: Pflanzen-Molekularfarming, therapeutische Peptide, Pflanzenbasierte Arzneimittel, rekombinante Proteinsynthese, metabolische Optimierung in Pflanzen