Clear Sky Science · es
Aproximaciones biotecnológicas para producir péptidos terapéuticos en plantas
Convertir hojas verdes en medicinas curativas
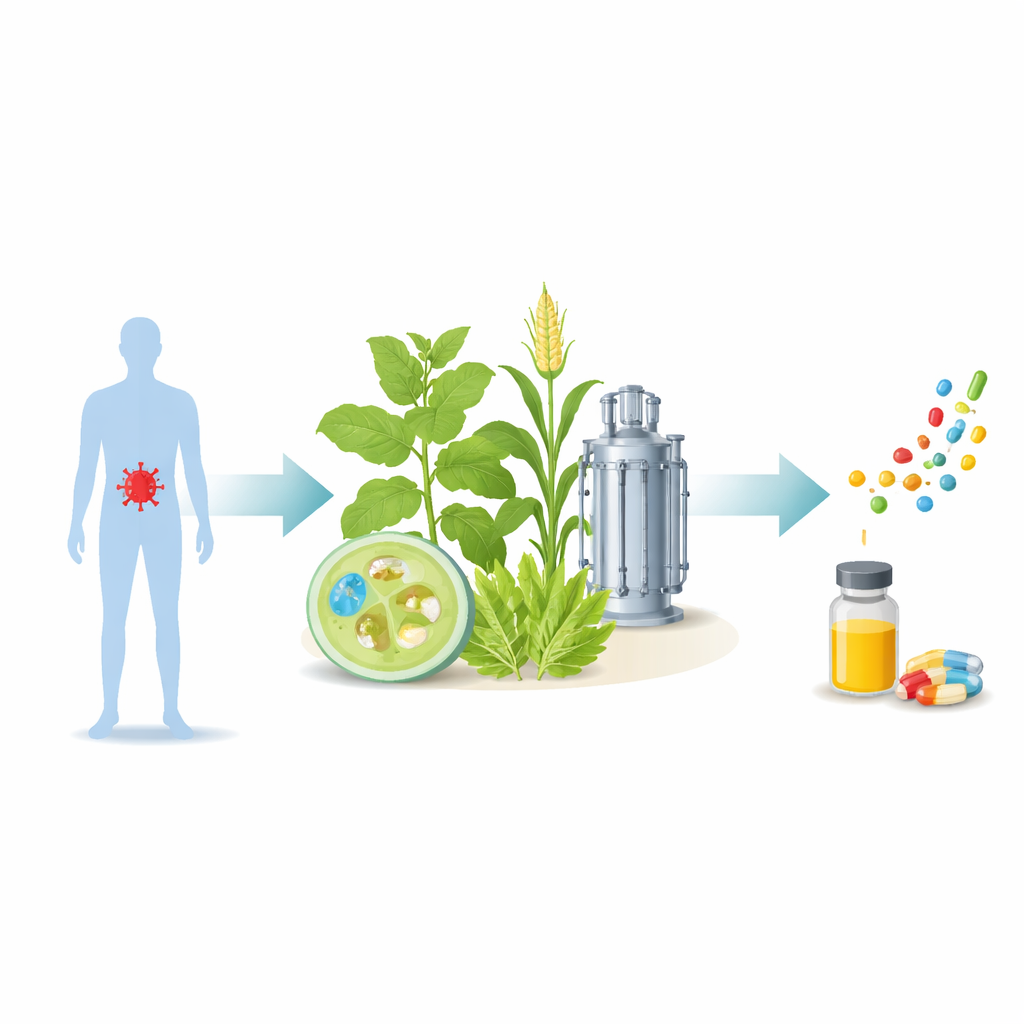
La mayoría de los medicamentos modernos, en especial los fármacos complejos de proteínas y péptidos, se fabrican en tanques de acero llenos de bacterias o células animales. Esta revisión explora una idea distinta: usar las propias plantas vivas como pequeñas fábricas de péptidos terapéuticos —cadenas cortas de aminoácidos que pueden combatir infecciones, tratar el cáncer o moderar un sistema inmunitario hiperactivo. Los autores explican por qué las plantas podrían hacer estos medicamentos más asequibles y seguros, y cómo los científicos están aprendiendo a inducir a las hojas, semillas e incluso cultivos celulares vegetales para que produzcan de forma fiable péptidos potentes y estables.
Por qué las plantas son atractivas como factorías de medicamentos
Las plataformas de producción tradicionales, como bacterias, levaduras y células de mamífero, son potentes pero caras, técnicamente exigentes y pueden conllevar riesgos de contaminación por patógenos humanos. En contraste, las plantas crecen con luz solar, agua y nutrientes simples, escalan fácilmente de invernaderos a campos y no albergan virus humanos o animales. En las últimas dos décadas, parientes del tabaco y cultivos alimentarios como arroz, maíz, patata y tomate han producido con éxito vacunas, anticuerpos, hormonas y enzimas —algunos ya probados en personas o aprobados para su uso. Esta experiencia demuestra que las plantas pueden manejar productos biológicos sofisticados y allana el camino para ampliar su uso a fármacos basados en péptidos, que son más pequeños pero a menudo más complicados de fabricar y estabilizar.
Incrementar la cantidad de péptido que pueden producir las plantas
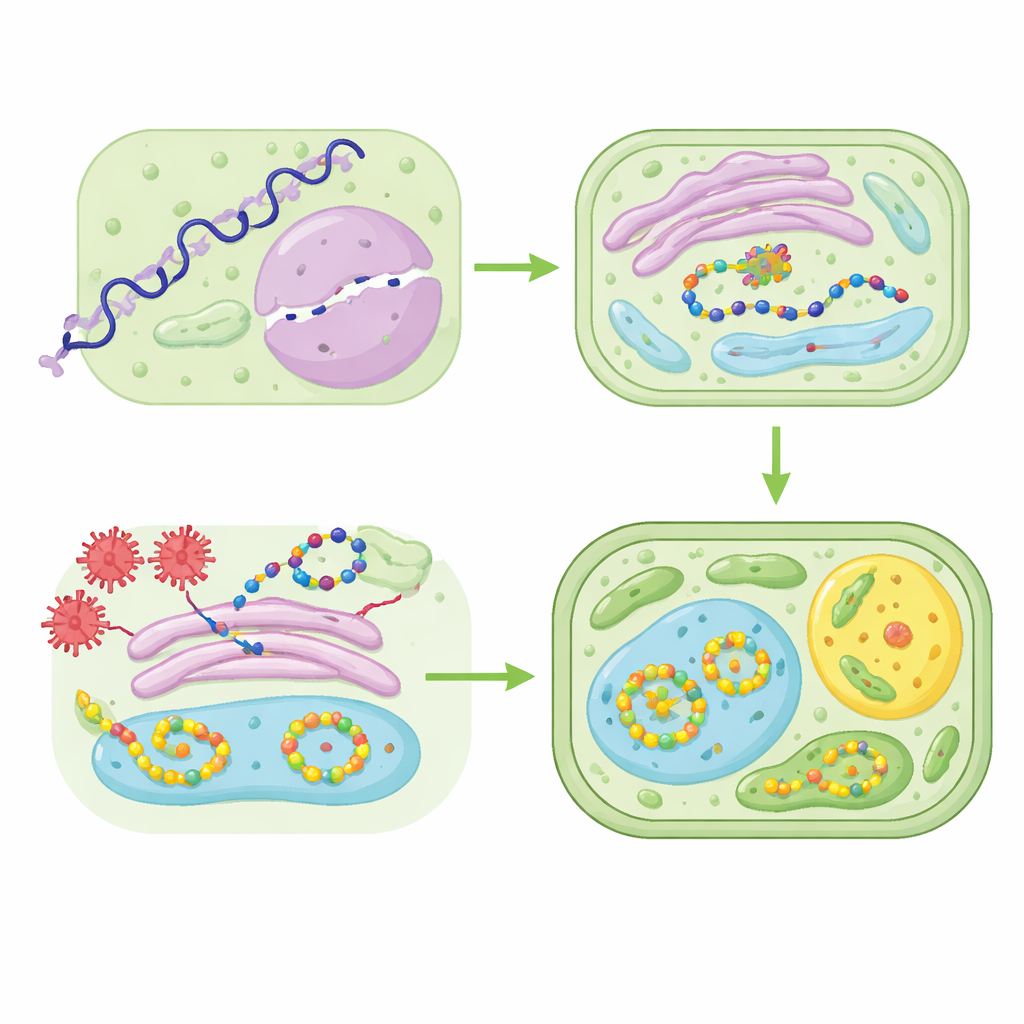
Conseguir que una planta produzca cantidades útiles de un péptido terapéutico requiere afinar con cuidado cada paso, desde el gen hasta el producto final. Los investigadores eligen interruptores genéticos fuertes o específicos de tejidos (promotores) para que el péptido se sintetice principalmente en lugares seguros como las semillas, que almacenan grandes cantidades de proteína y mantienen los productos estables durante largos periodos. También emplean herramientas de ADN inspiradas en virus que copian temporalmente el gen terapéutico muchas veces dentro de las células de las hojas, generando picos de producción rápidos y elevados. Ajustar el código genético para adaptarlo a las preferencias de la planta puede aumentar aún más el rendimiento, aunque debe hacerse con cuidado para que el ARN resultante siga plegándose y funcionando correctamente. En conjunto, estas estrategias pueden transformar una planta de productora renuente en una biofactoría de alto rendimiento.
Proteger los péptidos frágiles dentro de la planta
Una vez sintetizados, los péptidos deben sobrevivir a los sistemas de mantenimiento de la propia planta, que permanentemente degradan proteínas, responden al estrés y eliminan moléculas dañadas. La revisión destaca varias formas de proteger productos valiosos frente a ese desgaste interno. Una consiste en co-producir inhibidores naturales de proteasas o desactivar selectivamente las proteasas vegetales más problemáticas, reduciendo la degradación no deseada. Otra es dirigir los péptidos hacia espacios celulares más seguros, como el retículo endoplásmico, las vacuolas, los cloroplastos o el apoplasto fuera de la membrana celular, donde hay menos enzimas destructivas o donde se añaden las modificaciones químicas necesarias. Un enfoque particularmente poderoso es inducir a las plantas a formar péptidos cíclicos —moléculas de anillo presentes en algunas especies silvestres— que resisten las enzimas digestivas y permanecen lo bastante estables como para administrarse por vía oral.
Trucos de diseño para reducir el estrés y la toxicidad en la planta
Muchos péptidos terapéuticos están diseñados para perforar membranas microbianas o interferir en la señalización, lo que significa que también pueden dañar células vegetales si se producen en el lugar o momento equivocados. Para evitarlo, los científicos usan interruptores inducibles que mantienen los genes silenciosos hasta que un desencadenante externo, como un spray, los activa una vez que la planta ha crecido. Confinan la expresión a semillas, tubérculos o compartimentos celulares específicos donde los péptidos son menos propensos a dañar tejidos vitales. Asociar los péptidos a compañeros de fusión especiales puede enmascarar temporalmente su actividad, ayudarles a plegarse correctamente, formar cuerpos proteicos densos para su almacenamiento y simplificar la purificación. Los autores también describen cómo tratamientos suaves de calor y químicos antioxidantes pueden moderar las respuestas al estrés durante la entrega genética, aumentando la eficiencia de la transformación y la expresión transitoria.
Ingeniería del metabolismo y superación de obstáculos del mundo real
Más allá del péptido en sí, el metabolismo vegetal debe suministrar los bloques de construcción adecuados sin saturarse. La ingeniería metabólica permite a los investigadores añadir genes biosintéticos faltantes, bloquear reacciones secundarias que crean subproductos indeseados y afinar los niveles de expresión para que las plantas se mantengan saludables mientras producen compuestos de alto valor, como precursores anticancerígenos o feromonas de insectos. Al mismo tiempo, el campo debe sortear obstáculos prácticos: mantener la calidad del producto constante entre lotes, alinear la producción en campo abierto o invernadero con estándares de fabricación farmacéutica y reducir los costes de extracción y purificación de fármacos a partir de tejidos vegetales complejos. Los cultivos de células vegetales controlados y los sistemas de raíces peludas ofrecen una vía hacia procesos de producción más estandarizados y compatibles con BPM (GMP).
De parcelas experimentales a terapias de uso cotidiano
La revisión concluye que las plantas están preparadas para desempeñar un papel importante en la próxima generación de medicamentos peptídicos, pero que el éxito dependerá de adaptar las estrategias a cada molécula concreta. Factores como si un péptido necesita enlaces disulfuro, ciclización, azúcares específicos o protección estricta contra la degradación dictarán la mejor elección de especie vegetal, tejido, compartimento celular y sistema de control genético. Combinando avances en diseño genético, biología celular, ingeniería metabólica y manejo del estrés, los investigadores aspiran a construir plataformas vegetales robustas y escalables que puedan suministrar péptidos terapéuticos estables y potentes a menor coste y con alcance global.
Cita: Thanthrige, N., Lawrence, N. & Craik, D.J. Biotechnological approaches for producing therapeutic peptides in plants. npj Sci. Plants 2, 12 (2026). https://doi.org/10.1038/s44383-026-00021-z
Palabras clave: agricultura molecular vegetal, péptidos terapéuticos, fármacos fabricados en plantas, producción de proteínas recombinantes, ingeniería metabólica en plantas