Clear Sky Science · it
Approcci biotecnologici per la produzione di peptidi terapeutici nelle piante
Trasformare le foglie verdi in medicine curative
La maggior parte dei farmaci moderni, in particolare quelli a base di proteine e peptidi complessi, viene prodotta in serbatoi d'acciaio pieni di batteri o cellule animali. Questa rassegna esplora un'idea diversa: utilizzare le piante vive come microfabbriche di peptidi terapeutici—brevi catene di amminoacidi in grado di combattere infezioni, trattare il cancro o attenuare un sistema immunitario iperattivo. Gli autori spiegano perché le piante potrebbero rendere questi medicinali più accessibili e sicuri, e come gli scienziati stanno imparando a indurre foglie, semi e persino colture cellulari vegetali a produrre in modo affidabile peptidi farmacologicamente potenti e stabili.
Perché le piante sono attraenti come fabbriche di farmaci
Piattaforme di produzione tradizionali come batteri, lieviti e cellule di mammifero sono potenti ma costose, tecnicamente impegnative e possono comportare rischi di contaminazione da patogeni umani. Al contrario, le piante crescono grazie alla luce solare, acqua e nutrienti semplici, si scalano facilmente da serre a campi e non ospitano virus umani o animali. Negli ultimi vent’anni, parenti del tabacco e colture alimentari come riso, mais, patata e pomodoro hanno prodotto con successo vaccini, anticorpi, ormoni ed enzimi—alcuni già testati sull’uomo o approvati per l’uso. Questa esperienza dimostra che le piante possono gestire prodotti biologici sofisticati e prepara il terreno per espandere l’uso verso farmaci a base di peptidi, che sono più piccoli ma spesso più difficili da produrre e stabilizzare.
Aumentare la quantità di peptidi che le piante possono produrre
Indurre una pianta a generare quantità utili di un peptide terapeutico richiede di ottimizzare con cura ogni passaggio, dal gene al prodotto finale. I ricercatori scelgono interruttori genetici forti o specifici per tessuto (promotori) in modo che il peptide venga prodotto principalmente in sedi sicure come i semi, che immagazzinano naturalmente grandi quantità di proteine e mantengono i prodotti stabili per lunghi periodi. Usano inoltre strumenti di DNA ispirati ai virus che copiano temporaneamente il gene terapeutico molte volte nelle cellule fogliari, ottenendo picchi rapidi e elevati di produzione. L’adattamento del codice genetico alle preferenze della pianta può aumentare ulteriormente la resa, sebbene debba essere fatto con attenzione affinché l’RNA risultante mantenga la corretta struttura e funzione. Nel loro insieme, queste strategie possono trasformare una pianta da produttrice riluttante a biofabbrica ad alto rendimento.
Proteggere i peptidi fragili all’interno della pianta
Una volta sintetizzati, i peptidi devono sopravvivere ai sistemi di manutenzione della pianta, che degradano continuamente le proteine, rispondono allo stress e rimuovono le molecole danneggiate. La rassegna evidenzia diversi modi per proteggere i prodotti preziosi da questo logoramento interno. Uno è la co-produzione di inibitori delle proteasi naturali o la disattivazione selettiva delle proteasi vegetali più problematiche, riducendo la degradazione indesiderata. Un altro è indirizzare i peptidi verso compartimenti cellulari più sicuri come il reticolo endoplasmatico, i vacuoli, i cloroplasti o l'apoplasto esterno alla membrana cellulare, dove sono presenti meno enzimi distruttivi o dove vengono aggiunte decorazioni chimiche necessarie. Un approccio particolarmente efficace è incoraggiare le piante a formare peptidi ciclici—molecole ad anello presenti in alcune specie selvatiche—che resistono agli enzimi digestivi e rimangono sufficientemente stabili da poter essere somministrate per via orale.
Trucchi di progettazione per ridurre stress e tossicità nelle piante
Molti peptidi terapeutici sono progettati per perforare le membrane microbiche o interferire con segnali biologici, il che significa che possono danneggiare anche le cellule vegetali se prodotti nel posto sbagliato o al momento sbagliato. Per evitare ciò, gli scienziati impiegano interruttori inducibili che mantengono i geni silenti fino a quando uno stimolo esterno, come uno spray, li attiva dopo la crescita della pianta. Limitano l’espressione a semi, tuberi o compartimenti cellulari specifici dove i peptidi sono meno propensi a danneggiare tessuti vitali. Partner di fusione speciali possono mascherare temporaneamente l’attività del peptide, favorirne il corretto ripiegamento, formare corpi proteici densi per lo stoccaggio e semplificare la purificazione. Gli autori descrivono anche come trattamenti termici blandi e sostanze antiossidanti possano attenuare le risposte da stress durante la consegna genica, migliorando l’efficienza di trasformazione e l’espressione transitoria.
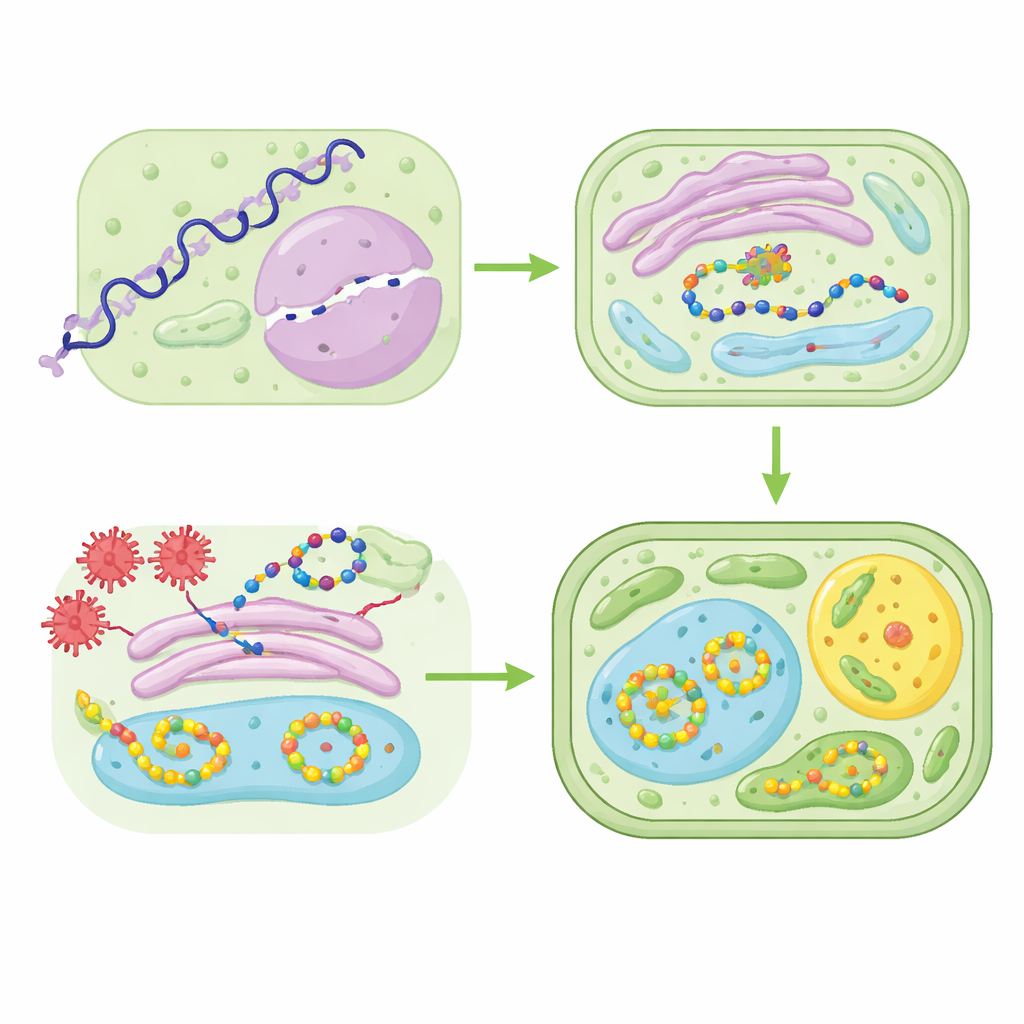
Ingegneria del metabolismo e superamento degli ostacoli pratici
Oltre al peptide stesso, il metabolismo della pianta deve fornire i mattoni giusti senza essere sovraccaricato. L’ingegneria metabolica permette ai ricercatori di aggiungere geni biosintetici mancanti, bloccare reazioni collaterali che creano sottoprodotti indesiderati e calibrare i livelli di espressione in modo che le piante restino sane pur producendo composti di alto valore come precursori anticancro o feromoni per insetti. Contemporaneamente, il campo deve affrontare ostacoli pratici: mantenere la qualità del prodotto costante da lotto a lotto, allineare la produzione in campo aperto o in serra agli standard di produzione farmaceutica e ridurre i costi di estrazione e purificazione da tessuti vegetali complessi. Colture cellulari vegetali controllate e sistemi di radice pelosa offrono una via verso pipeline di produzione più standardizzate e compatibili con le norme GMP.
Dai lotti sperimentali alle terapie di uso quotidiano
La rassegna conclude che le piante sono pronte a svolgere un ruolo importante nella prossima generazione di farmaci peptidici, ma che il successo dipenderà dall’adattare le strategie a ciascuna molecola. Fattori come la necessità di legami disolfuro, ciclizzazione, attacchi zuccherini particolari o una protezione stringente dalla degradazione determineranno la scelta migliore di specie vegetale, tessuto, compartimento cellulare e sistema di controllo genetico. Combinando i progressi nella progettazione genica, biologia cellulare, ingegneria metabolica e gestione dello stress, i ricercatori mirano a costruire piattaforme vegetali robuste e scalabili in grado di fornire peptidi terapeutici stabili e potenti a costi più bassi e con portata globale.
Citazione: Thanthrige, N., Lawrence, N. & Craik, D.J. Biotechnological approaches for producing therapeutic peptides in plants. npj Sci. Plants 2, 12 (2026). https://doi.org/10.1038/s44383-026-00021-z
Parole chiave: agricoltura molecolare vegetale, peptidi terapeutici, farmaci prodotti in piante, produzione di proteine ricombinanti, ingegneria metabolica nelle piante