Clear Sky Science · pt
Epidemiologia molecular da OXA-1054, uma nova β-lactamase Classe D que hidrolisa carbapenêmicos, em Enterobacteriaceae isoladas de águas residuais
Por que os germes em água suja importam
A maioria de nós pensa em resistência a antibióticos como algo que acontece dentro de hospitais. Mas os medicamentos que usamos, e os germes que eles atingem, não permanecem ali. Eles seguem com as águas residuais para estações de tratamento e rios, onde bactérias de muitas origens se misturam e trocam truques genéticos para sobreviver aos nossos melhores remédios. Este estudo acompanha um desses truques — um gene de resistência recém-descoberto — no sistema de águas residuais de Sevilha, Espanha, para entender onde ele vive, como se movimenta e por que isso importa para infecções futuras.
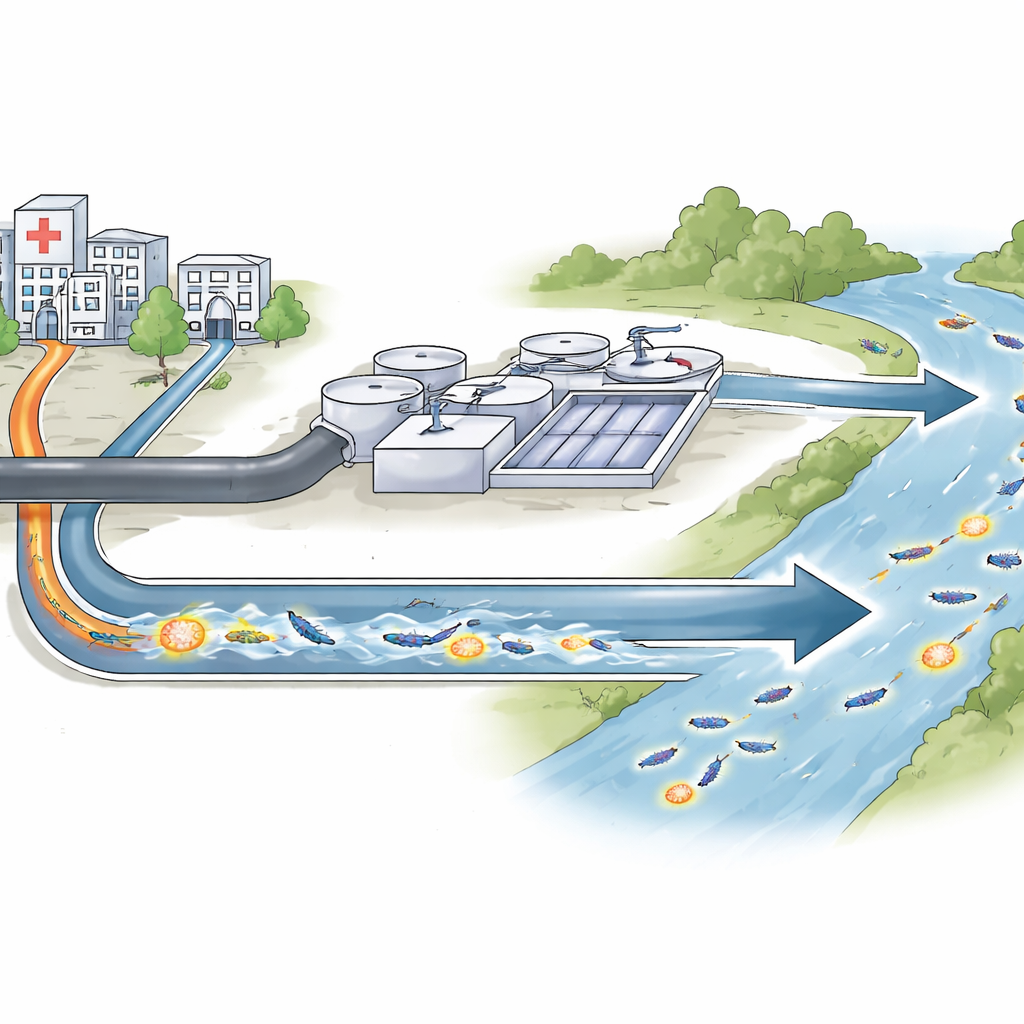
Um novo truque de resistência em bactérias comuns do intestino
Os pesquisadores focaram em um grupo de bactérias chamado Enterobacteriaceae, que inclui muitos micróbios intestinais que podem causar infecções graves. Alguns membros desse grupo aprenderam a degradar carbapenêmicos, uma classe de antibióticos de último recurso. A equipe identificou uma versão até então desconhecida de uma enzima de resistência, denominada OXA-1054, em bactérias coletadas de descargas hospitalares, estações municipais de tratamento de águas residuais e do rio Guadalquivir nas proximidades. Essa enzima pertence a uma linhagem chamada OXA-372, relacionada, mas distinta, da mais conhecida família OXA-48, amplamente disseminada em hospitais. Ao clonar o novo gene em cepas inofensivas de laboratório de Escherichia coli, os cientistas demonstraram que a OXA-1054 pode, de fato, aumentar a resistência a vários medicamentos importantes, incluindo carbapenêmicos.
Águas residuais como tigela de mistura para resistência
A maioria das bactérias portadoras de OXA-1054 foi encontrada em águas residuais brutas que entram nas estações de tratamento, especialmente em uma grande instalação, com alguns isolados na água de descarga hospitalar e no rio a jusante. O gene apareceu em várias espécies diferentes, como Citrobacter, Enterobacter e Raoultella, e em muitos clones não relacionados dentro dessas espécies. Esse padrão sugere que o gene de resistência não está confinado a uma única linhagem bem‑sucedida, mas está se espalhando por bactérias diversas que compartilham o mesmo ambiente aquático. Embora o tratamento tenha reduzido as bactérias detectáveis no efluente tratado, o gene ainda apareceu no rio em momentos diferentes, insinuando que águas ambientais podem atuar como um reservatório de longo prazo.
Um pacote móvel projetado para persistir
Ao observar mais de perto o DNA ao redor do gene blaOXA-1054, a equipe encontrou‑o inserido em um módulo móvel recorrente — essencialmente um pequeno pacote genético portátil. Esse pacote quase sempre continha dois genes de transposição, istA e istB, da família IS21, além de várias cópias de outro tipo de elemento móvel. Em muitos casos, um segundo gene de resistência (ampC) e conjuntos para resistir a metais pesados como arsênico e mercúrio estavam localizados nas proximidades. Esses complementos significam que a poluição por metais ou outros fármacos poderia favorecer indiretamente bactérias que também carregam OXA-1054. Os plasmídeos (pequenos círculos de DNA) que abrigavam esse módulo frequentemente portavam múltiplos sistemas de “toxina‑antitoxina”, armadilhas genéticas que ajudam a garantir que o plasmídeo não seja facilmente perdido quando as bactérias se dividem, mantendo a característica de resistência na população mesmo quando antibióticos não estão presentes.
Como ele se espalha sem transferência clássica
Surpreendentemente, a maioria dos plasmídeos que carregavam OXA-1054 carecia da maquinaria usual para mover‑se entre bactérias por conjugação, e experimentos de conjugação em laboratório falharam em transferir o gene para uma cepa receptora. Isso aponta para um modo diferente de disseminação: em vez de um plasmídeo altamente móvel varrer as comunidades bacterianas, uma plataforma móvel conservada contendo blaOXA-1054 parece pular para vários plasmídeos e às vezes diretamente para cromossomos bacterianos. Genes acessórios extras — como helicases de DNA, metiltransferases de DNA e proteínas de manutenção estrutural — podem ajudar a estabilizar essas plataformas e apoiar seu movimento e sobrevivência em águas poluídas e sujeitas a estresse.
O que isso significa para pessoas e rios
Em termos simples, o estudo mostra que um potente novo gene de resistência já está circulando nas águas residuais da cidade e no rio próximo, embora ainda não tenha se tornado comum em pacientes hospitalares. Ele está presente em um pacote de DNA móvel e robusto que ajuda a persistir e a pegar carona com outros traços de resistência, incluindo defesas contra metais pesados. Essa combinação aumenta a probabilidade de que o gene perdure no ambiente e permaneça pronto para entrar em bactérias associadas a humanos. O trabalho ressalta que proteger nossos antibióticos mais valiosos exige monitorar não apenas clínicas, mas também os mundos microbianos ocultos em canos, estações de tratamento e rios que conectam a atividade humana ao ambiente mais amplo.
Citação: Monge-Olivares, L., González-Pinto, L., Pulido, M.R. et al. Molecular epidemiology of OXA-1054, a novel carbapenem-hydrolysing Class D β-lactamase, in Enterobacteriaceae isolated from wastewaters. npj Antimicrob Resist 4, 36 (2026). https://doi.org/10.1038/s44259-026-00209-4
Palavras-chave: resistência a antibióticos, águas residuais, carbapenemase, elementos genéticos móveis, microbiologia ambiental