Clear Sky Science · es
Epidemiología molecular de OXA-1054, una nueva β-lactamasa de Clase D que hidroliza carbapenemes, en Enterobacteriaceae aisladas de aguas residuales
Por qué importan los gérmenes en el agua sucia
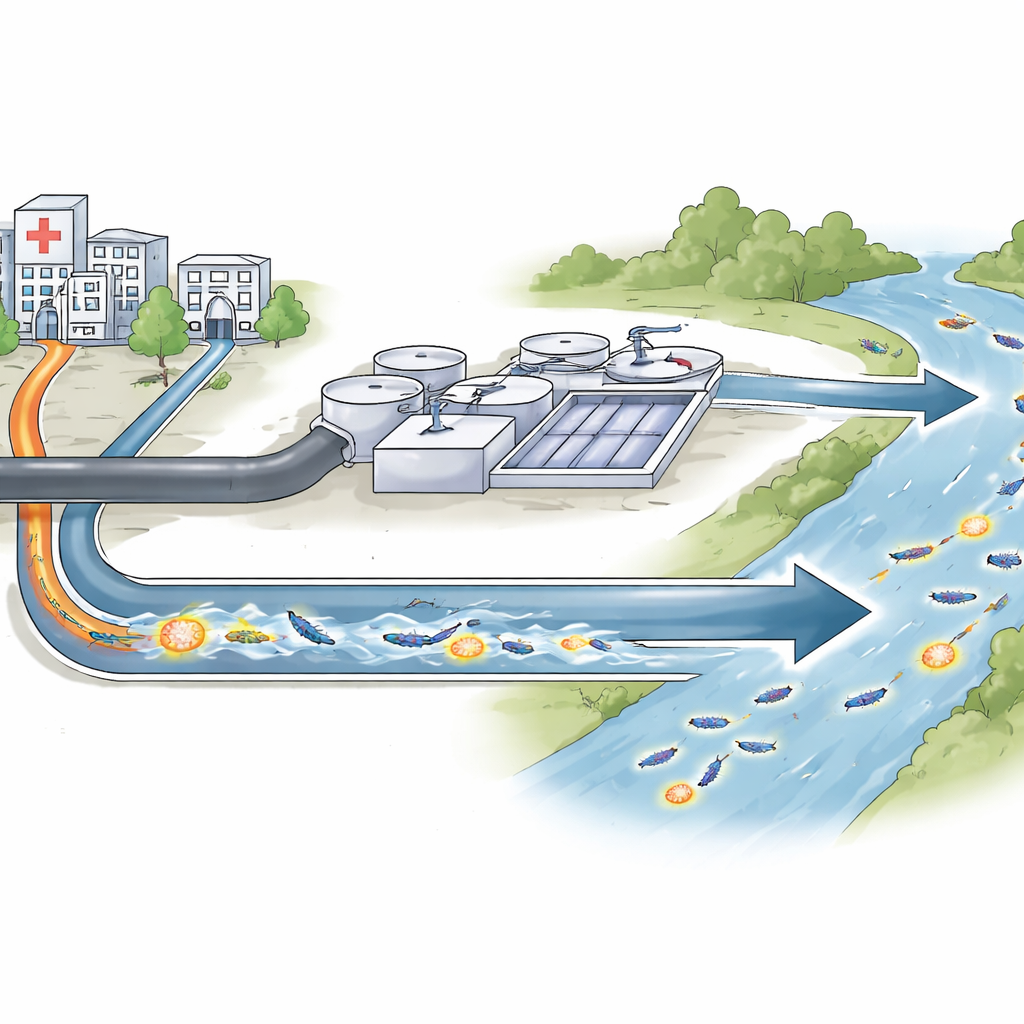
La mayoría de nosotros pensamos en la resistencia a los antibióticos como algo que ocurre dentro de los hospitales. Pero los fármacos que usamos y los gérmenes a los que afectan no se quedan ahí. Salen con las aguas residuales hacia las depuradoras y los ríos, donde bacterias de muchas fuentes se mezclan y se intercambian estrategias genéticas para sobrevivir a nuestros mejores medicamentos. Este estudio rastrea una de esas estrategias—un gen de resistencia recién descubierto—en el sistema de aguas residuales de Sevilla, España, para entender dónde vive, cómo se mueve y por qué eso importa para futuras infecciones.
Una nueva treta de resistencia en bacterias intestinales comunes
Los investigadores se centraron en un grupo de bacterias llamado Enterobacteriaceae, que incluye muchos microbios intestinales que pueden causar infecciones graves. Algunos miembros de este grupo han aprendido a desactivar los carbapenemes, una familia de antibióticos de última instancia. El equipo halló una versión hasta ahora desconocida de una enzima de resistencia, denominada OXA-1054, en bacterias recogidas de tuberías de salida hospitalaria, estaciones depuradoras municipales y el cercano río Guadalquivir. Esta enzima pertenece a una línea evolutiva llamada OXA-372, relacionada con pero distinta de la familia OXA-48, más conocida y extendida en hospitales. Mediante el clonaje del nuevo gen en cepas de laboratorio inocuas de Escherichia coli, los científicos demostraron que OXA-1054 puede aumentar de hecho la resistencia a varios fármacos importantes, incluidos los carbapenemes.
Las aguas residuales como crisol de la resistencia
La mayoría de las bacterias portadoras de OXA-1054 se encontraron en aguas residuales sin tratar que entraban a las depuradoras, especialmente en una instalación principal, con algunos aislados en aguas de salida hospitalaria y en el río aguas abajo. El gen apareció en varias especies diferentes, como Citrobacter, Enterobacter y Raoultella, y en muchos clones no relacionados dentro de esas especies. Este patrón sugiere que el gen de resistencia no está confinado a una sola cepa exitosa, sino que se está difundiendo entre bacterias diversas que comparten el mismo entorno acuático. Aunque el tratamiento redujo las bacterias detectables en el efluente tratado, el gen todavía se detectó en el río en distintos momentos, lo que apunta a que las aguas ambientales pueden actuar como reservorio a largo plazo.
Un paquete móvil diseñado para persistir
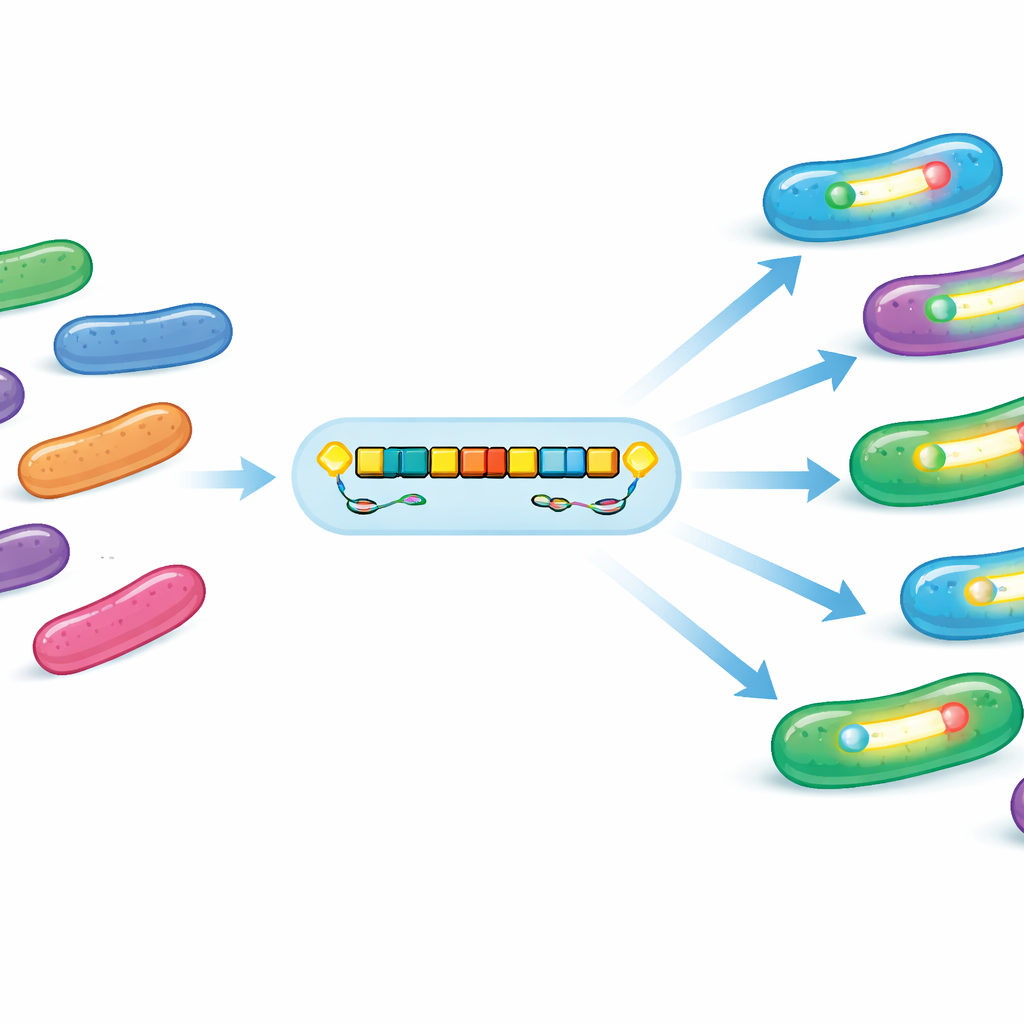
Al mirar de cerca el ADN que rodea al gen blaOXA-1054, el equipo lo encontró incrustado en un módulo móvil recurrente—esencialmente un pequeño paquete genético portátil. Este paquete casi siempre contenía dos genes de transposición, istA e istB, de la familia IS21, además de varias copias de otro tipo de elemento móvil. En muchos casos, un segundo gen de resistencia (ampC) y cúmulos para resistir metales pesados como arsénico y mercurio estaban ubicados cerca. Estos añadidos significan que la contaminación con metales u otros fármacos podría favorecer indirectamente a las bacterias que también portan OXA-1054. Los plásmidos (pequeños círculos de ADN) que albergaban este módulo a menudo llevaban múltiples sistemas “toxina–antitoxina”, trampas genéticas que ayudan a asegurar que el plásmido no se pierda fácilmente cuando las bacterias se dividen, manteniendo el rasgo de resistencia en la población incluso cuando los antibióticos no están presentes.
Cómo se propaga sin el traslado clásico
Sorprendentemente, la mayoría de los plásmidos que llevan OXA-1054 carecían del maquinario habitual para moverse entre bacterias por conjugación, y los experimentos de conjugación en laboratorio no consiguieron transferir el gen a una cepa receptora. Esto apunta a un modo de propagación distinto: en lugar de un plásmido altamente móvil que barre las comunidades bacterianas, una plataforma móvil conservada que contiene blaOXA-1054 parece saltar a distintos plásmidos y, a veces, directamente a cromosomas bacterianos. Genes accesorios adicionales—como helicasas de ADN, metiltransferasas de ADN y proteínas de mantenimiento estructural—pueden ayudar a estabilizar estas plataformas y favorecer su movimiento y supervivencia en aguas estresadas y contaminadas.
Qué significa esto para las personas y los ríos
En términos sencillos, el estudio muestra que un potente gen de resistencia ya circula en las aguas residuales de la ciudad y en el río cercano, aunque aún no se haya vuelto común entre los pacientes hospitalizados. Se encuentra en un paquete de ADN móvil y resistente que le ayuda a persistir y a viajar junto a otros rasgos de resistencia, incluidas defensas contra metales pesados. Esta combinación hace más probable que el gen perdure en el medio ambiente y permanezca listo para entrar en bacterias asociadas a humanos. El trabajo subraya que proteger nuestros antibióticos más valiosos requiere vigilar no solo las clínicas, sino también los mundos microbianos ocultos en tuberías, depuradoras y ríos que conectan la actividad humana con el entorno más amplio.
Cita: Monge-Olivares, L., González-Pinto, L., Pulido, M.R. et al. Molecular epidemiology of OXA-1054, a novel carbapenem-hydrolysing Class D β-lactamase, in Enterobacteriaceae isolated from wastewaters. npj Antimicrob Resist 4, 36 (2026). https://doi.org/10.1038/s44259-026-00209-4
Palabras clave: resistencia a antibióticos, aguas residuales, carbapenemasa, elementos genéticos móviles, microbiología ambiental