Clear Sky Science · de
Molekulare Epidemiologie von OXA-1054, einer neuartigen carbapenem-spaltenden Klasse-D-β-Lactamase, in aus Abwässern isolierten Enterobacteriaceae
Warum Keime in verschmutztem Wasser wichtig sind
Die meisten von uns verbinden Antibiotikaresistenz mit Krankenhäusern. Doch die eingesetzten Medikamente und die von ihnen betroffenen Keime bleiben nicht dort. Sie gelangen mit dem Abwasser in Kläranlagen und Flüsse, wo Bakterien aus vielen Quellen zusammenkommen und genetische Tricks zum Überleben gegen unsere stärksten Medikamente austauschen. Diese Studie verfolgt einen solchen Trick — ein neu entdecktes Resistenzgen — im Abwassersystem von Sevilla, Spanien, um zu verstehen, wo es vorkommt, wie es sich bewegt und warum das für künftige Infektionen relevant ist.
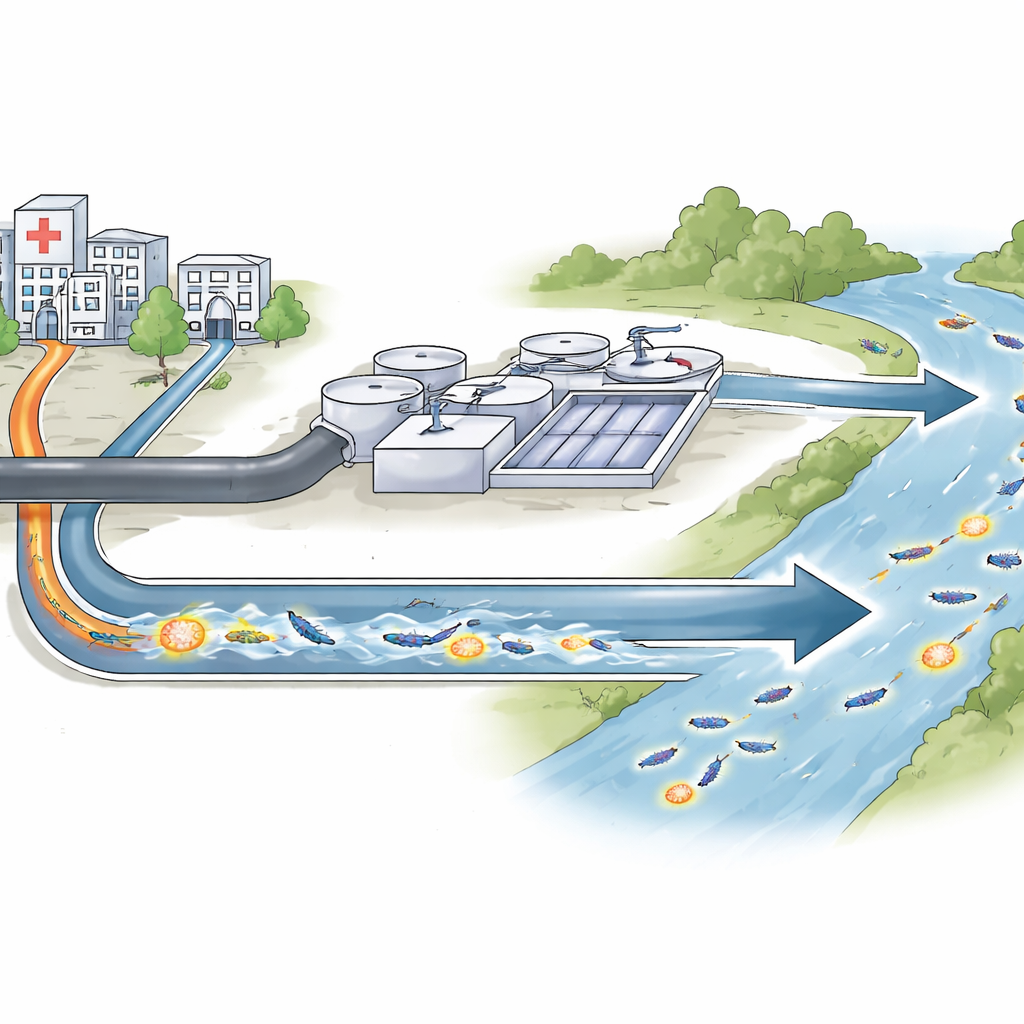
Ein neuer Resistenztrick in verbreiteten Darmbakterien
Die Forschenden konzentrierten sich auf eine Gruppe von Bakterien namens Enterobacteriaceae, zu der viele Darmmikroben gehören, die ernsthafte Infektionen verursachen können. Einige Vertreter dieser Gruppe haben gelernt, Carbapeneme — eine Reserveklasse von Antibiotika — zu spalten. Das Team entdeckte eine zuvor unbekannte Variante eines Resistenzenzyms, OXA-1054 genannt, in Bakterien, die aus Krankenhausabflüssen, städtischen Kläranlagen und dem nahegelegenen Guadalquivir-Fluss isoliert wurden. Dieses Enzym gehört zu einer Linie namens OXA-372, die mit, aber unterscheidbar von der bekannteren OXA-48-Familie ist, die sich weit in Krankenhäusern verbreitet hat. Durch das Klonieren des neuen Gens in harmlose Laborstämme von Escherichia coli zeigten die Wissenschaftler, dass OXA-1054 tatsächlich die Resistenz gegen mehrere wichtige Wirkstoffe, darunter Carbapeneme, erhöhen kann.
Abwasser als Schmelztiegel für Resistenzen
Die meisten OXA-1054-tragenden Bakterien wurden im Rohabwasser gefunden, das in Kläranlagen einströmt, insbesondere in einer großen Anlage; nur wenige Isolate stammten aus Krankenhausabflüssen und dem Flusswasser stromabwärts. Das Gen erschien in mehreren verschiedenen Arten wie Citrobacter, Enterobacter und Raoultella und in vielen nicht verwandten Klonen innerhalb dieser Arten. Dieses Muster legt nahe, dass das Resistenzgen nicht auf einen einzigen erfolgreichen Stamm beschränkt ist, sondern sich über diverse Bakterien verbreitet, die dieselbe aquatische Umgebung teilen. Obwohl die Behandlung die nachweisbare Bakterienlast im gereinigten Ablauf verringerte, tauchte das Gen zu verschiedenen Zeiten im Fluss auf, was darauf hindeutet, dass Gewässer als langfristiges Reservoir wirken können.
Ein mobiles Paket, gebaut zum Verweilen
Bei genauer Betrachtung der DNA um das blaOXA-1054-Gen herum fand das Team es eingebettet in ein wiederkehrendes mobiles Modul — im Wesentlichen ein kleines, tragbares genetisches Paket. Dieses Paket enthielt fast immer zwei Transpositionsgene, istA und istB, aus der IS21-Familie, sowie mehrere Kopien eines anderen Elements. In vielen Fällen befand sich ein zweites Resistenzgen (ampC) und Gencluster für die Resistenz gegen Schwermetalle wie Arsen und Quecksilber in der Nähe. Diese Zusätze bedeuten, dass Verschmutzung mit Metallen oder anderen Wirkstoffen indirekt Bakterien begünstigen könnte, die ebenfalls OXA-1054 tragen. Die Plasmide (kleine DNA-Kreise), die dieses Modul beherbergten, trugen häufig mehrere „Toxin–Antitoxin“-Systeme — genetische Fallen, die verhindern, dass das Plasmid beim Zellteilen leicht verloren geht, und so das Resistenzelement in der Population halten, selbst wenn keine Antibiotika vorhanden sind.
Wie es sich ohne klassischen Transfer ausbreitet
Überraschenderweise fehlte den meisten Plasmiden mit OXA-1054 die übliche Ausrüstung für die Konjugation zwischen Bakterien, und Labormating-Experimente konnten das Gen nicht in einen Empfängerstamm übertragen. Das deutet auf einen anderen Verbreitungsmodus hin: Statt eines hochmobilen Plasmids, das Bakteriengemeinschaften durchdringt, scheint eine konservierte mobile Plattform, die blaOXA-1054 enthält, in verschiedene Plasmide und manchmal direkt in bakterielle Chromosomen zu springen. Zusätzliche Begleitgene — wie DNA-Helikasen, DNA-Methyltransferasen und Proteine zur Erhaltung der Chromosomenstruktur — könnten helfen, diese Plattformen zu stabilisieren und ihre Bewegung und ihr Überleben in belasteten, verschmutzten Gewässern zu unterstützen.
Was das für Menschen und Flüsse bedeutet
Kurz gesagt zeigt die Studie, dass ein mächtiges neues Resistenzgen bereits im städtischen Abwasser und im nahegelegenen Fluss zirkuliert, auch wenn es bislang noch nicht häufig bei Krankenhauspatienten auftritt. Es sitzt auf einem robusten, mobilen DNA-Paket, das ihm hilft, zu bestehen und mit anderen Resistenzmerkmalen mitzufahren, einschließlich Abwehrsystemen gegen Schwermetalle. Diese Kombination erhöht die Wahrscheinlichkeit, dass das Gen in der Umwelt bestehen bleibt und bereit ist, in mit Menschen assoziierte Bakterien überzugehen. Die Arbeit unterstreicht, dass der Schutz unserer wertvollsten Antibiotika nicht nur die Überwachung von Kliniken erfordert, sondern auch der verborgenen mikrobiellen Welten in Rohren, Kläranlagen und Flüssen, die menschliche Aktivitäten mit der weiteren Umwelt verbinden.
Zitation: Monge-Olivares, L., González-Pinto, L., Pulido, M.R. et al. Molecular epidemiology of OXA-1054, a novel carbapenem-hydrolysing Class D β-lactamase, in Enterobacteriaceae isolated from wastewaters. npj Antimicrob Resist 4, 36 (2026). https://doi.org/10.1038/s44259-026-00209-4
Schlüsselwörter: Antibiotikaresistenz, Abwasser, Carbapenemase, mobile genetische Elemente, Umweltmikrobiologie