Clear Sky Science · fr
Épidémiologie moléculaire de OXA-1054, une nouvelle bêta-lactamase de classe D hydrolysant les carbapénèmes, chez des Enterobacteriaceae isolés des eaux usées
Pourquoi les microbes présents dans les eaux polluées comptent
La plupart d’entre nous associent la résistance aux antibiotiques aux hôpitaux. Mais les médicaments que nous utilisons, et les microbes qu’ils ciblent, ne restent pas confinés là‑bas. Ils s’écoulent avec les eaux usées vers les stations d’épuration et les cours d’eau, où des bactéries provenant de sources diverses se rencontrent et échangent des astuces génétiques pour survivre à nos meilleurs traitements. Cette étude suit l’une de ces astuces — un gène de résistance nouvellement découvert — dans le réseau d’eaux usées de Séville, en Espagne, pour comprendre où il se trouve, comment il se déplace et pourquoi cela importe pour les infections futures.
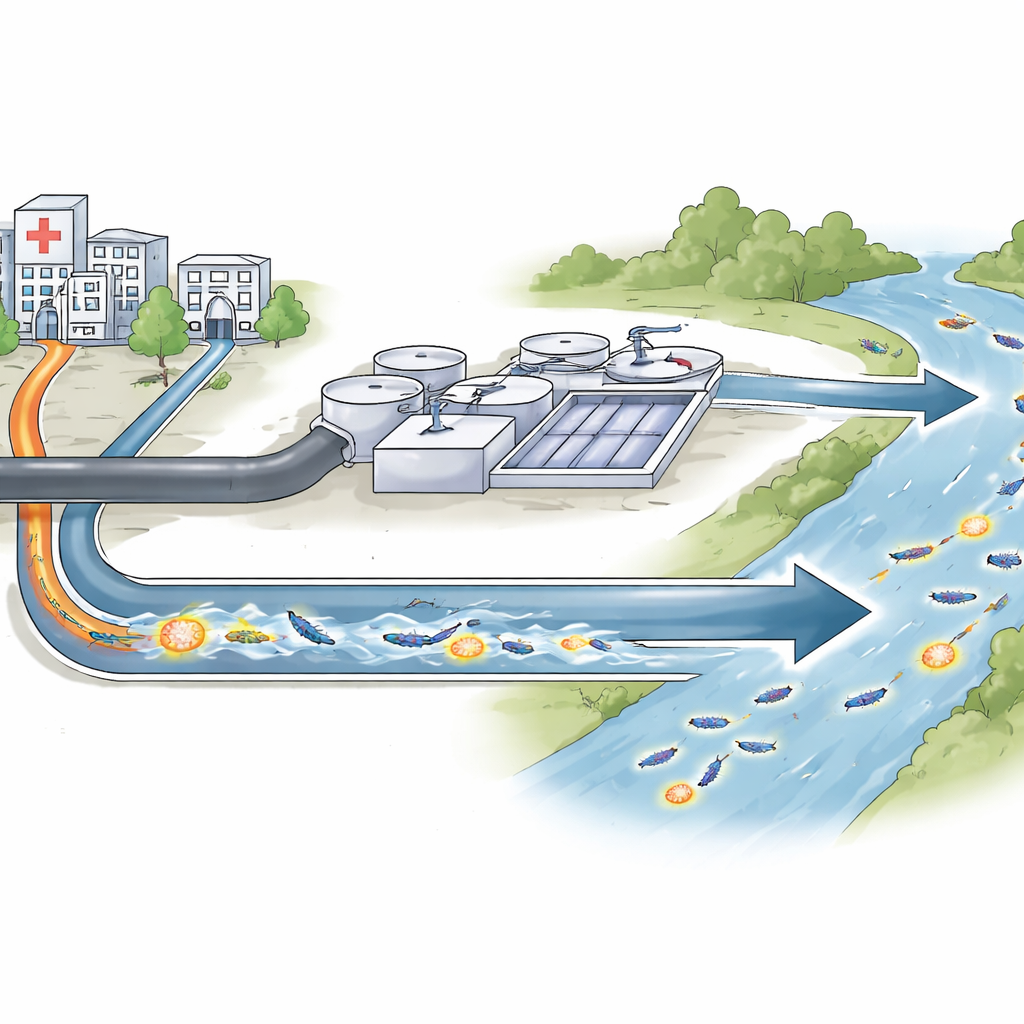
Une nouvelle astuce de résistance dans des bactéries intestinales courantes
Les chercheurs se sont concentrés sur un groupe de bactéries appelé Enterobacteriaceae, qui comprend de nombreux microbes intestinaux susceptibles de provoquer des infections graves. Certains membres de ce groupe ont appris à dégrader les carbapénèmes, une famille d’antibiotiques de dernier recours. L’équipe a identifié une version jusque‑là inconnue d’une enzyme de résistance, nommée OXA‑1054, dans des bactéries prélevées sur des tuyaux d’évacuation d’hôpitaux, dans des stations d’épuration de la ville et dans le fleuve Guadalquivir voisin. Cette enzyme appartient à une lignée appelée OXA‑372, apparentée mais distincte de la famille OXA‑48 mieux connue et largement diffusée en milieu hospitalier. En clonant le nouveau gène dans des souches de laboratoire inoffensives d’Escherichia coli, les scientifiques ont montré que OXA‑1054 peut effectivement augmenter la résistance à plusieurs médicaments importants, y compris les carbapénèmes.
Les eaux usées, un creuset pour la résistance
La plupart des bactéries porteuses de OXA‑1054 ont été trouvées dans les eaux usées brutes entrant dans les stations d’épuration, surtout dans une grande installation, avec quelques isolats provenant des eaux d’évacuation hospitalières et de l’eau du fleuve en aval. Le gène est apparu dans plusieurs espèces différentes, telles que Citrobacter, Enterobacter et Raoultella, et dans de nombreux clones non apparentés au sein de ces espèces. Ce schéma suggère que le gène de résistance n’est pas confiné à une souche unique et performante, mais se propage à travers une diversité de bactéries partageant le même milieu aquatique. Bien que le traitement ait réduit la charge bactérienne détectable dans l’effluent traité, le gène est néanmoins réapparu dans le fleuve à différents moments, laissant entendre que les eaux environnementales peuvent servir de réservoir à long terme.
Un paquet mobile conçu pour persister
En examinant de près l’ADN entourant le gène blaOXA‑1054, l’équipe a constaté qu’il était intégré dans un module mobile récurrent — essentiellement un petit paquet génétique portable. Ce module contenait presque toujours deux gènes de transposition, istA et istB, de la famille IS21, ainsi que plusieurs copies d’un autre type d’élément mobile. Dans de nombreux cas, un second gène de résistance (ampC) et des clusters conférant une résistance aux métaux lourds tels que l’arsenic et le mercure étaient situés à proximité. Ces éléments additionnels signifient que la pollution par les métaux ou par d’autres médicaments pourrait indirectement favoriser les bactéries portant aussi OXA‑1054. Les plasmides (petits cercles d’ADN) qui hébergeaient ce module portaient souvent plusieurs systèmes « toxine–antitoxine », des pièges génétiques qui aident à empêcher la perte du plasmide lors de la division bactérienne, maintenant ainsi le caractère résistant dans la population même en l’absence d’antibiotiques.
Comment il se propage sans transfert classique
De façon surprenante, la plupart des plasmides portant OXA‑1054 étaient dépourvus des machines habituelles de transfert entre bactéries par conjugaison, et des expériences d’accouplement en laboratoire n’ont pas réussi à transférer le gène vers une souche réceptrice. Cela suggère un mode de propagation différent : au lieu d’un plasmide extrêmement mobile balayant les communautés bactériennes, une plateforme mobile conservée contenant blaOXA‑1054 semble sauter dans divers plasmides et parfois directement dans des chromosomes bactériens. Des gènes accessoires supplémentaires — tels que des hélicases d’ADN, des méthyltransférases d’ADN et des protéines de maintien structural — peuvent aider à stabiliser ces plateformes et soutenir leur mouvement et leur survie dans des eaux polluées et stressantes.
Ce que cela signifie pour les personnes et les rivières
En termes simples, l’étude montre qu’un puissant nouveau gène de résistance circule déjà dans les eaux usées de la ville et dans le fleuve voisin, même s’il n’est pas encore devenu fréquent chez les patients hospitalisés. Il repose sur un paquet d’ADN mobile et robuste qui l’aide à persister et à faire du « stop » avec d’autres traits de résistance, y compris des défenses contre les métaux lourds. Cette combinaison augmente la probabilité que le gène perdure dans l’environnement et reste prêt à pénétrer des bactéries associées à l’homme. Le travail souligne que protéger nos antibiotiques les plus précieux exige de surveiller non seulement les cliniques, mais aussi les mondes microbiens cachés dans les canalisations, les stations d’épuration et les rivières qui relient l’activité humaine à l’environnement plus large.
Citation: Monge-Olivares, L., González-Pinto, L., Pulido, M.R. et al. Molecular epidemiology of OXA-1054, a novel carbapenem-hydrolysing Class D β-lactamase, in Enterobacteriaceae isolated from wastewaters. npj Antimicrob Resist 4, 36 (2026). https://doi.org/10.1038/s44259-026-00209-4
Mots-clés: résistance aux antibiotiques, eaux usées, carbapénémase, éléments génétiques mobiles, microbiologie environnementale