Clear Sky Science · pt
Geração de fármacos covalentes de novo com melhor perfil de "drug‑likeness" e segurança
Por que fármacos covalentes mais inteligentes importam
Terapias contra o câncer e antivirais geralmente agem ao se ligarem a proteínas dentro de nossas células. Uma classe poderosa de medicamentos, chamada fármacos covalentes, vai além: eles formam ligações firmes e duradouras com seus alvos, o que pode torná‑los muito efetivos. Mas essa mesma "aderência" também pode causar efeitos colaterais sérios se os medicamentos se ligarem a proteínas erradas. Este estudo apresenta o CovaGEN, um novo sistema de inteligência artificial projetado para inventar candidatos a fármacos covalentes do zero, mantendo em mente tanto a eficácia quanto a segurança.
Do método tentativa‑e‑erro ao desenho inteligente
A descoberta tradicional de fármacos covalentes é lenta e cara. Químicos costumam ou partir de um fármaco existente e acrescentar uma "alça" reativa, ou começar com um fragmento reativo e ajustar laboriosamente o resto da molécula. Métodos auxiliados por computador ajudam ao rastrear grandes bibliotecas de compostos conhecidos, mas ficam limitados ao que já existe. Avanços recentes em aprendizado profundo podem gerar moléculas totalmente novas, porém essas ferramentas geralmente focam em fármacos convencionais, não covalentes, e muitas vezes ignoram características cruciais como facilidade de síntese, semelhança com medicamentos reais ou potencial toxicidade. O CovaGEN busca enfrentar todas essas questões de uma vez só.
Um mapa oculto da química com perfil de fármaco
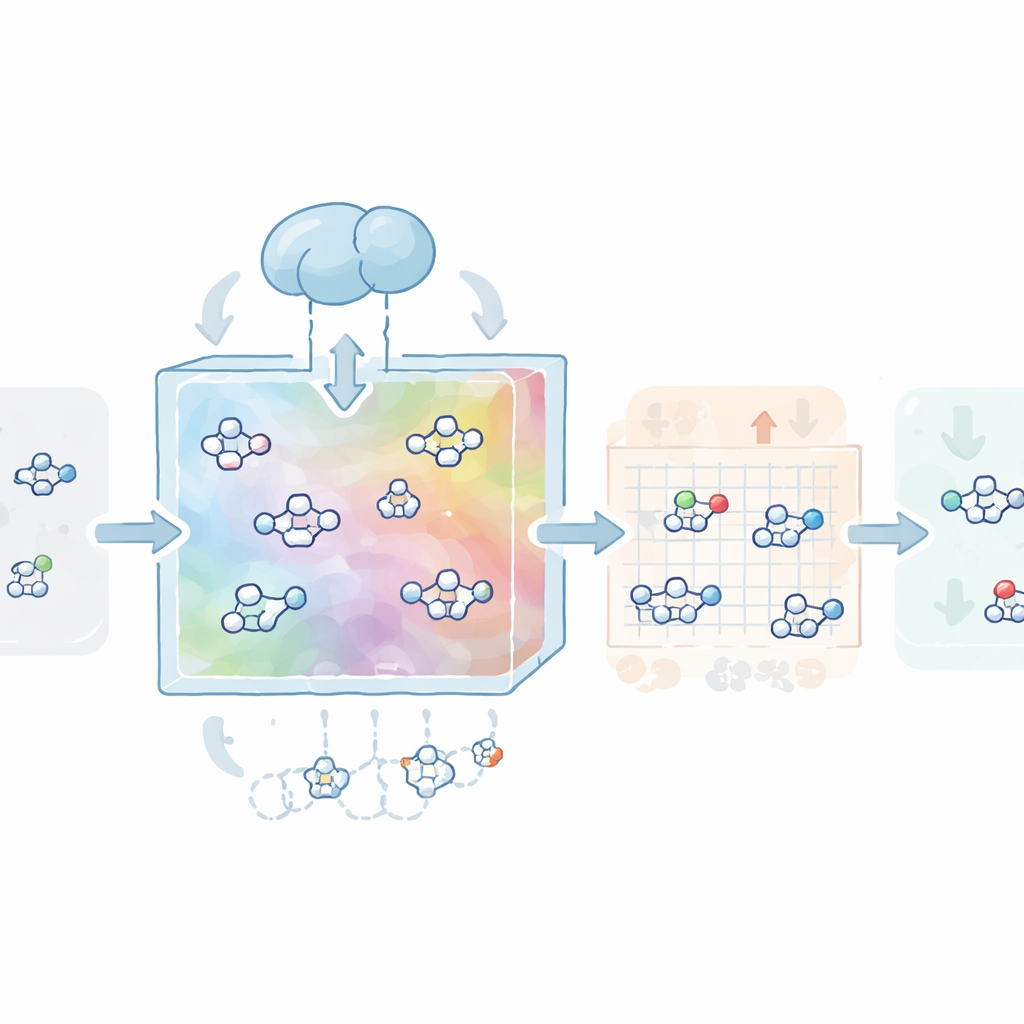
Os autores primeiro construíram um "mapa" do espaço químico usando mais de um milhão de moléculas com perfil de fármaco da base pública ZINC. Eles treinaram um tipo de rede neural chamada autoencoder variacional para comprimir cada molécula em um código numérico compacto, ou vetor latente, e então reconstruí‑la. Essa etapa ensina o modelo a gramática básica da química medicinal: o que parece realista, o que respeita regras comuns para medicamentos orais e o que tende a ser sinteticamente viável. Nesse mapa aprendido, um segundo modelo baseado em difusão — um processo que gradualmente transforma estrutura em ruído e depois aprende a reverter esse processo — foi treinado para vagar e gerar novos vetores latentes que decodificam em moléculas válidas, diversas e realistas.
Ajustando moléculas aos alvos proteicos e aos ganchos reativos
Em seguida, o CovaGEN aprende a projetar moléculas para alvos proteicos específicos. O sistema recebe a sequência de aminoácidos de uma proteína e a codifica com um poderoso modelo de linguagem para proteínas, que captura padrões relacionados à estrutura e função. Durante a difusão, o modelo realiza atenção cruzada a essa representação proteica para que as moléculas geradas sejam predispostas a caber no sítio de ligação do alvo. Em testes em um grande conjunto de referência, essas moléculas sob medida não só obtiveram boas pontuações de afinidade prevista como também mostraram melhor perfil de "drug‑likeness" e acessibilidade sintética que as provenientes de várias ferramentas de desenho 3D de ponta. Para transformar esses ligantes não covalentes em candidatos covalentes, a equipe adicionou um classificador que direciona o processo de difusão para moléculas contendo certos grupos reativos, conhecidos como warheads covalentes, sem sacrificar a qualidade geral.
Incorporando segurança desde o início
Como fármacos covalentes podem causar danos duradouros se atingirem alvos errados, a segurança é uma preocupação central. Os pesquisadores, portanto, trataram a toxicidade como uma quantidade a ser otimizada, não um mero detalhe posterior. Eles treinaram modelos preditivos de toxicidade aguda e de riscos específicos a órgãos, e então aplicaram aprendizado por reforço para ajustar finamente o modelo de difusão para que ele prefira moléculas com toxicidade prevista menor. Após esse treinamento, o CovaGEN gerou compostos que mantiveram boa afinidade prevista e características de fármaco, mas eram menos propensos a conter "sinais vermelhos" estruturais associados a efeitos nocivos. Importante: o método alcançou isso sem colapsar para um conjunto estreito de moléculas semelhantes, preservando a diversidade química.
Colocando o método à prova
Para demonstrar potencial no mundo real, a equipe pediu ao CovaGEN que projetasse inibidores covalentes para dois alvos de alto valor: uma forma mutante da proteína EGFR envolvida em câncer de pulmão resistente a fármacos, e a protease principal do SARS‑CoV‑2, o vírus por trás da COVID‑19. Para cada proteína, o sistema gerou muitos candidatos equipados com os warheads apropriados. Estudos computacionais de docking sugeriram que os desenhos do CovaGEN tinham maior probabilidade de adotar poses capazes de formar ligações covalentes do que compostos onde os warheads foram simplesmente encaixados em desenhos não covalentes. Vários dos principais candidatos também igualaram ou superaram fármacos de referência em medidas combinadas de afinidade prevista, "drug‑likeness" e facilidade sintética.
O que isso significa para medicamentos futuros
O CovaGEN mostra que a IA generativa moderna pode fazer mais do que imaginar moléculas que se ligam fortemente a proteínas. Ao trabalhar num espaço de estruturas inerentemente com perfil de fármaco, guiar a adição de grupos reativos e orientar explicitamente para longe da toxicidade, o sistema move a descoberta de fármacos covalentes para um processo mais holístico e automatizado. Embora sejam necessários testes laboratoriais adicionais para confirmar como essas moléculas virtuais se comportam em sistemas vivos, a abordagem abre um caminho para uma exploração mais rápida e mais ampla de medicamentos covalentes que não sejam apenas potentes, mas também mais seguros para os pacientes.
Citação: Zhang, W., Liu, T., Dong, X. et al. De novo covalent drug generation with enhanced drug-likeness and safety. Commun Biol 9, 446 (2026). https://doi.org/10.1038/s42003-026-09725-5
Palavras-chave: fármacos covalentes, IA generativa, descoberta de fármacos, modelos de difusão, predição de toxicidade